белок теплового шока что это такое
Белок теплового шока что это такое
К.Д. Никитин
«Клиническая онкогематология», апрель 2008
Как и многие другие открытия, белки теплового шока были обнаружены во многом благодаря случайности, когда однажды вечером в одной из итальянских лабораторий кто-то случайно установил слишком высокую температуру в инкубаторе с плодовыми мушками Drosophila. На следующий день при исследовании хромосом из слюнных желез мушек были выявлены интересные изменения, свидетельствующие о необычном характере экспрессии генов. Так было положено начало изучению группы белков, названных белками теплового шока (БТШ).
Название отражает некоторые свойства белков теплового шока, но далеко не все. Во-первых, БТШ синтезируются в некотором количестве постоянно в любых ядерных клетках, во множестве внутриклеточных структур (в цитоплазме, ядре, эндоплазматическом ретикулуме, митохондриях и хлоропластах) у всех многоклеточных организмов, начиная с самых примитивных, как у растений, так и у животных, вне зависимости от воздействия стрессовых факторов. Даже в покоящихся клетках до 2% всех белков могут составлять представители этого семейства.
Во-вторых, повышение внутриклеточного синтеза БТШ происходит отнюдь не только на тепловой шок, но и на любое стрессовое воздействие: внешнее (УФ, тепловой шок, тяжелые металлы, аминокислоты), патологическое (вирусные, бактериальные и паразитарные инфекции, лихорадка, воспаление, злокачественная трансформация, аутоиммунные реакции) или даже физиологическое (ростовые факторы, клеточная дифференциация, гормональная стимуляция, тканевый рост). Синтез БТШ является универсальным неспецифическим ответом клетки на стресс, и, по современным данным, нет такого вида клеточного стресса, при котором не происходило бы синтеза БТШ. В некоторых случаях содержание БТШ в клетках, подвергнутых шоку, может достигать 20% всех растворимых цитоплазматических белков.
Выделяют четыре основных семейства БТШ:
Несмотря на общую задачу всех этих белков (обеспечение выживания клетки в условиях стресса), функции и тканеспецифичность БТШ варьируют от группы к группе как в нормальных условиях, так и при стрессе.
Белки теплового шока
Белки теплового шока (англ. HSP, Heat shock proteins ) — это класс функционально сходных белков, экспрессия которых усиливается при повышении температуры или при других стрессирующих клетку условиях. [1] Повышение экспрессии генов, кодирующих белки теплового шока, регулируется на этапе транскрипции. Чрезвычайное усиление экспрессии генов, кодирующих белки теплового шока является частью клеточного ответа на тепловой шок и вызывается в основном фактором теплового шока (HSF англ. heat shock factor ). [2] Белки теплового шока обнаружены в клетках практически всех живых организмов, от бактерий до человека.
Белки теплового шока называют согласно их молекулярным массам. Например, наиболее изученные белки теплового шока Hsp60, Hsp70 и Hsp90 относятся к семействам белков с молекулярными массами 60, 70 и 90 кДа, соответственно. [3] Убиквитин является относительно небольшим белком (8 кДа), выполняющим функции белков теплового шока. Убиквитином в клетке помечаются белки, предназначенные для деградации. [4]
Содержание
История открытия
Было показано, что быстрое нагревание до сублетальных температур делает организмы нечувствительными к нагреванию до более высоких температур. В 1962 году Ритосса показал, что нагревание и ингибитор метаболизма динитрофенол вызывают сходные изменения в структуре пуффов политенных хромосом Дрозофилы. Это открытие далее привело к выделению белков теплового шока англ. heat-shock proteins (HSP) или белков стресса. Повышение экспрессии генов, кодирующих указанные белки у Дрозофилы было показано в 1974 году. Экспрессия повышалась после действия на мух стрессирующих факторов, например, теплового шока. [5]
Начиная с середины 1980-х годов было показано, что многие белки теплового шока действуют как шапероны и играют важную роль в сворачивании белков, внутриклеточном транспорте белков и ренатурации белков, изменивших конформацию после теплового шока.
Функции
Механизм активации
Точный механизм, по которому тепловой шок активирует экспрессию генов белков теплового шока, не выяснен. Однако, некоторые исследования свидетельствуют о том, что активация белков теплового шока происходит неправильно сложенными или поврежденными белками.
Повышение синтеза при стрессе
Высокие уровни белков теплового шока в клетке наблюдают после воздействия различных стрессирующих факторов — при инфекциях, воспалительных процессах, внешних воздействиях токсинов (этанол, мышьяк, тяжелые металлы), при ультрафиолетовом облучении, голодании, гипоксии, недостатке азота (у растений) или нехватке воды. Белки теплового шока называют белками стресса, так как повышение экспрессии соответствующих генов часто наблюдается при ответе на стресс. [6]
Шапероны
Белки теплового шока действуют как внутриклеточные шапероны в отношении других белков. Белки теплового шока играют важную роль в белок-белковых взаимодействиях, например, при фолдинге и сборке сложных белков, препятствуют нежелательной агрегации белков. Белки теплового шока стабилизируют частично свернутые белки и облегчают их транспорт через мембраны внутри клетки. [7] [8]
Некоторые белки теплового шока экспрессируются в малых или умеренных количествах во всех типах клеток всех живых организмов, так как играют ключевую роль в существовании белков.
Внутриклеточные функции
Белки теплового шока присутствуют в клетках и при нестрессовых условиях, как бы следят за белками в клетке. Белки теплового шока утилизируют старые белки в составе протеасомы и помогают корректно свернуться заново синтезированным белкам.
Сердечно-сосудистая система
По-видимому, белки теплового шока играют важную роль в сердечно-сосудистой системе. Для белков теплового шока hsp90, hsp84, hsp70, hsp27, hsp20, и альфа-B-кристаллин показана роль деятельности сердечно-сосудистой системы. [9]
Hsp90 связывает эндотелиальную синтетазу оксида азота и гуанилатциклазу, которые в свою очередь участвуют в расслаблении сосудов. [10]
В системе передачи сигнала при помощи оксида азота далее протеинкиназа G фосфорилирует малый белок теплового шока, hsp20, который принимает участие в расслаблении гладких мышц. [11] Hsp20 по-видимому, играет важную роль в развитии гладких мышц и предотвращает агрегацию тромбоцитов, предотвращает апоптоз после ишемического инсульта, а также имеет значение в функционировании скелетных мышц и ответе мышц на инсулин. [12]
Hsp27 является главным фосфопротеином при мышечном сокращении. [13]
Иммунитет
Внеклеточные и связанные с плазматической мембраной, белки теплового шока, и особенно Hsp70, участвуют в связывании и презентации антигенов. [14]
Клиническое значение
Фактор теплового шока 1 (англ. HSF1 ) является транскрипционным фактором, регулирующим экспрессию гена Hsp70. [15] Было показано, что HSF1 является многосторонним фактором канцерогенеза. Мыши, нокаутные по гену HSF1 имели сниженные уровни возникновения раковых опухолей после нанесения мутагена 7,12-диметилбенантрацена. [16]
Применение
Так как некоторые белки теплового шока играют роль в презентации антигенов, [14] их используют в качестве адъювантов для вакцин. [17] Более того, некоторые исследователи считают, что белки теплового шока могут принимать участие в связывании белковых фрагментов разрушенных опухолевых клеток, осуществляя презентацию антигена иммунной системе. [18] Некоторые белки теплового шока могут повышать эффективность вакцин против рака. [14] [19]
Противораковые препараты
Внутриклеточные белки теплового шока экспрессируются в раковых клетках и необходимы для выживания этих клеток. Показана роль малых молекул, ингибирующих белки теплового шока в качестве противораковых средств. [20] Эффективный ингибитор Hsp90 17-N-аллиламино-17-деметоксигельданамицин проходит клинические испытания как средство против некоторых видов рака. [21]
Применение в сельском хозяйстве
Исследована роль белков теплового шока в устойчивости к стрессу у гибридов растений, что может далее привести к выведению засухоустойчивых сортов, растущих на бедной почве. [22]
Классификация
Белки теплового шока, которые имеют функции шаперонов, классифицируют в пять классов: HSP33,HSP60, HSP70, HSP90, HSP100, и малые белки теплового шока (sHSPs). [5]
| Ориентировочная молекулярная масса, кДа | Прокариотические белки | Эукариотические белки | Функция |
|---|---|---|---|
| 10 кДа | GroES | Hsp10 | |
| 20-30 кДа | GrpE | Группа белков теплового шока HspB включает десять представителей у млекопитающих, в их числе Hsp27 | |
| 40 кДа | DnaJ | Hsp40 | Кофактор Hsp70 |
| 60 кДа | GroEL, антиген массок 60 кДа | Hsp60 | Участвует в фолдинге белков после их посттрансляционного транспорта в митохондрию или хлоропласт |
| 70 кДа | DnaK | Группа белков теплового шока HspA. Включает в себя Hsp71, Hsp70, Hsp72, Grp78 (BiP). Причем Hsx70 обнаружен только у приматов | Принимает участие в сворачивании и разворачивании белков, обеспечивает клетке нечувствительность к нагреванию. Предотвращает сворачивание белков в ходе посттрансляционного транспорта в митохондрии и хлоропласты. |
| 90 кДа | HtpG, C62.5 | Группа белков теплового шока HspC, включает в состав Hsp90, Grp94 | Поддержание структуры стероидных рецепторов и факторов транскрипции |
| 100 кДа | ClpB, ClpA, ClpX | Hsp104, Hsp110 | Обеспечивает невосприимчивость к повышению температуры |
Многие белки, представленные в таблице имеют разновидности, получающиеся в результате альтернативного сплайсинга, например, Hsp90α и Hsp90β.
Белок теплового шока что это такое
Белки теплового шока (heat shok proteins HSPs) широко распространены в живой природе и являются одними из наиболее консервативных молекул биосферы. Основная функция HSPs — защита биологических систем от повреждающих стрессорных воздействий. В процессе эволюции эукариот некоторые HSPs приобрели функции, позволившие им интегрироваться в систему иммунитета.
Роль HSPs во взаимодействии механизмов врожденного и приобретенного иммунитета определяется способностью HSPs перехватывать антигенные пептиды и репрезентировать их с помощью ДК Т-лимфоцитам в контексте молекул МНС.
Белки теплового шока обеспечивают важные жизненные функции и представлены у всех живых организмов. Продукты генов, наименованные белками теплового шока или белками клеточного стресса, вырабатываемые в условиях гипертермии, изначально были идентифицированы как молекулы, вырабатываемые в ответ на присутствие в клетках белков с нарушенной конформацией. Затем было установлено, что HSPs играют роль шаперонов в нековалентной сборке и демонтаже других макромолекулярных структур, хотя сами не являются перманентными компонентами этих структур при выполнении своих биологических функций.
Реакция белков теплового шока зафиксирована не только в условиях гипертермии, но также при оксидативном стрессе, ацидозе, ишемии, гипоксии-гипероксии, энергетическом истощении клеток и т п. В этих условиях HSPs высвобождаются из некротизированных клеток при разрушении ткани или лизисе инфицированных клеток.
Благодаря особенности распознавания гидрофобных аминокислотных последовательностей на поверхности белков, как предупредительного сигнала о конформационной их нестабильности, HSPs способны осуществлять такие жизненно важные функции, как участие в обеспечении пространственной организации белковых молекул (фолдинге), их стабилизации, коррекции конформационных изменений (рефолдинге), транслокации белков через мембраны внутриклеточных органелл, предотвращении белковой агрегации и деградации нестабильных белков. Наряду с этим, HSPs проявляют антиапоптотическую активность. В совокупности, HSPs выполняют роль буферной системы, противодействующей стохастическим и потенциально дестабилизирующим факторам клеточного окружения.
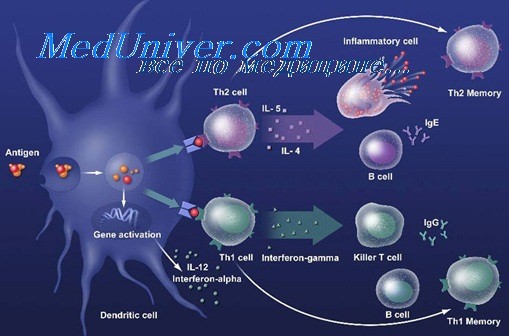
HSPs играют важную роль в индукции иммуного ответа, в особенности врожденного иммунитета: усиливают активность NK-клеток, созревание АПК и продукцию цитокинов. Пептидные фрагменты расщепляющихся белковых молекул перехватываются HSPs и, в конечном итоге, претерпевая процессинг в АПК, индуцируют реакции адаптивного иммунитета. Таким образом, через активацию АПК и участие в процессинге антигена белки теплового шока интегрируют реакции врожденного и приобретенного (адаптивного) иммунитета.
Иммуностимулирующие свойства проявляют HSP про- и эукаритического происхождения. Способностью к индукции иммунного ответа обладают представители нескольких семейств HSP (кальретикулин, HSP10, HSP60, HSP70, HSP90, HSP100 и HSP170).
Шаперонная функция белков теплового шока осуществляется не только в процессе биогенеза других белков, но и при иммунном ответе на антигены. Изменение окружающей среды при инфицировании создает стрессорную ситуацию как для вторгшегося патогена, так и для клеток хозяина, что проявляется в обоюдной интенсификации синтеза и функциональной активности белков теплового шока. Молекулярные шапероны бактерий выступают в роли лигандов для рецепторов на поверхности клеток хозяина.
HSPs могут быть распознаны TLR2, TLR4. Другие др96, HSP90 и HSP70, взаимодействуют с антигенпрезентирующими клетками через общий рецептор, CD91. HSP-шаперонные пептиды проникают в макрофаг/дендритные клетки через CD91, процессируются и презентируются вместе с молекулами МНС I и МНС II. Это вызывает активацию CD4 и CD8 Т-клеток. HSP-ДК взаимодействие через CD91 ведет к созреванию дендритных клеток и секреции ряда цитокинов.
В результате взаимодействия рекомбинантного HSP 70 М tuberculosis с TLR-2 и TLR-4 in vitro запускается сигнальный каскад с вовлечением адапторных белков MyD88, TIRAP, TRIF и TRAM в эндотелиоцитах человека и в макрофагах мышей происходит активация фактора транскрипции NF-кВ.
Представленный в эндоплазматическом ретикулуме эукариот, шаперон GRP94/gp96 через взаимодействие с TLR-2 и TLR-4 активирует дендритные клетки к инициации CD8′ Т-лимфоцитарного ответа. При этом усиливается экспрессия MICA/B молекул, взаимодействующих с NKG2D рецептором, представленным на поверхности CD8, но не СD4*Т-клеток. При взаимодействии TLR7 с HSP70, активно секретируемым, так и освобождаемым при некротической гибели клеток млекопитающих, усиливается фагоцитарная функция макрофагов. Данный эффект проявляется за несколько минут и выражается не только в стимуляции фагоцитоза, но также и функции представления антигена Т-клеткам через сигнальные пути, опосредуемые фосфоинозитид 3-киназой и р38 МАР-киназой.
В осуществлении презентации антигена хелперным Т-клеткам принимают участие также зрелые В-лимфоциты, экспрессирующие TLR-2 и TLR-4. Они отвечают на LPS, пептидогликан, HSP60 повышением экспрессии МНС II и костимуляторных молекул. HSP 60 человека, но не GroEL E. coli или HSP65 М. tuberculosis индуцируют пролиферацию наивных В-клеток мышей и секрецию ими IL-6 и IL-10.
На сегодняшний день многие рецепторы, распознающие паттерны известных PAMPs прокариотов, грибков, вирусов, простейших патогенов остаются еще не охарактеризованными. Существует взаимосвязь между фагоцитозом и экспрессией TLRs, поскольку активация сигналов через TLR усиливает фагоцитарные процессы, а фагоцитоз модулирует последовательность активации TLR.
Является очевидным, что еще неопределенные молекулярные паттерны могут искажать или направлять адаптивный имунный ответ по Тh-2 типу Возможно, что отсутствие сигналов (например — PAMPs), подобно дефициту своих МНС I для NK-клеточной активации является стимулом для запуска иммунитета второго типа.
Индукция сигналов через Toll-подобные рецепторы может обеспечивать не только защиту организма от различных инфекций. Нарушение функции проводимости данных сигналов приводит к развитию целого ряда патологических процессов в организме. Например, чрезмерная продукция провоспалительных цитокинов эндогенными лигандами может стать причиной развития хронического воспаления, аутоиммунных заболеваний, таких как болезнь Крона, диабет типа 1, атеросклероз. Изменение баланса в сторону провоспалительных цитокинов, вероятно, обусловлено развитием локальных отеков и воспалительных реакций в ЦНС инициированных провоспалительными цитокинами (TNF-a или IL-1p). В формировании длительно сохраняющихся неврологических нарушений принимают участие несколько цитокинов, которые потенцируя продукцию и действие друг друга, дольше сохраняются в циркуляции.
Постоянное присутствие цитокинов поддерживает хронический воспалительный процесс в ЦНС, сопровождающийся демиелинизацией, а в ряде случаев и гибелью нейронов.
Эффективность белков теплового шока в комплексе с иммунотерапией
Белок теплового шока – лекарство против рака, открывающее большие перспективы в лечении этого смертельного заболевания. Они позволяют одновременно блокировать тормозные рецепторы PD-1 и Tim-3, Т-лимфоцитов. Благодаря этому снимается блокировка иммунной системы, активируется естественная противораковая защита организма.
Что такое белки теплового шока (БТШ70)
Это белки, которые вырабатываются при воздействии на клетки высоких температур и других экстремальных факторов. Их синтез активируется при различных интоксикациях, стрессе, воздействии ультрафиолета на кожу. Эти соединения выполняют защитную функцию.
В периоды отсутствия воздействия стрессовых факторов БТШ70 также присутствуют в организме. Они защищают белковые молекулы, из которых построены ткани, позволяют вновь образовавшимся белкам приобрести правильную структуру. Также БТШ70 участвуют в иммунном ответе и связывании антигенов и остатков разрушенных белковых молекул. Именно последнее свойство заинтересовало онкологов.
Механизм действия белков теплового шока при раке
БТШ70 и их коньюгаты с полиэтиленгликолем и фрагментом Ig G1 оказывают блокирующее действие на рецепторы PD-1 и Tim-3, расположенные на поверхности Т-лимфоцитов. Благодаря этому активируется иммунный противоопухолевый ответ организма. Исследования проф. С.Б. Оникиенко и его соавторов показали, что количество PD-1 позитивных клеток снижается в 1,6-2,7 раза, а количество Tim-3 позитивных – в 10,5 раз.
Комбинированная терапия Ниволумабом и БТШ70: результаты клинических исследований
Учитывая механизм действия белков токсического шока, российские ученые решили попробовать использовать их в рамах комбинированной терапии рака вместе с препаратом Ниволумаб.
Результаты клинического исследования показали такие данные: при изолированном применении Ниволумаба регресса опухоли удалось добиться у 16% пациентов, при использовании комбинированной терапии – в 52% случаев.
Онколизис при комбинированном применении блокаторов «тормозных» рецепторов Ниволумаба и БТШ70. Канцероматоз плевры у пациента с метастатическим раком почки
Следует отметить, что комбинация с БТШ70 позволила снизить дозу Ниволумаба, благодаря чему значительно уменьшилось количество аутоиммунных реакций, которые при изолированном применении препарата мешали дальнейшему лечению у половины пациентов. Белок теплового шока против рака – это важное открытие в сфере онкологии, которое позволяет сделать иммунотерапию более безопасной и эффективной.
Для прогнозирования эффективности лечения БТШ70 используют инкубационные биопробы. Они позволяют in vitro оценить, как влияет терапия на количество комплексов раковых клеток, неассоциированных с лимфоцитами.
Результаты и перспективы
На сегодняшний день доказана эффективность лекарств от рака на основе белков теплового шока у пациентов с меланомой, астроцитомой, опухолями почек, желудка, легких, предстательной железы. Также проводились эксперименты на животных, в ходе которых получен положительный результат.
Учеными разработаны пролонгированные формы БТШ70, позволяющие значительно повысить эффективность лечения. С этой целью используются конъюгаты с Fc-фрагментом Ig G и ПЭГ. Именно эти формы стали основой препаратов, которые используются в комплексе с иммунотерапией.
Комбинированная схема лечения имеет следующие преимущества по сравнению с изолированным использованием Ниволумаба:
БТШ70 также используются и в других схемах терапии онкозаболеваний. Их успешно применяют в сочетании с онколитическими вирусами, радиотерапией. Благодаря масштабным научным исследованиям сегодня можно подобрать эффективный метод лечения для ранее безнадежных пациентов.
Перспективным направлением в лечении рака является персонализированная терапия. Комбинация препаратов подбирается в зависимости от иммунного статуса пациента, который определяется не только в начале, но и в процессе лечения. При гиперэкспрессии PD-1 рецепторов актуальна схема: Ниволумаб+БТШ70.
Использование белков теплового шока – это возможность воспользоваться всеми преимуществами иммунотерапии, при этом значительно сократив процент нежелательных последствий, которые вызывают серьезные изменения в организме и препятствуют дальнейшему лечению. Благодаря новым методикам лечения рака многие люди получили шанс избавиться от смертельного заболевания или прожить намного дольше, чем это было возможно ранее.
Белок теплового шока что это такое
В 1974 году Тиссиерес и соавт. [2] впервые обнаружили, что в ответ на повышение температуры среды происходит активация синтеза специфической группы белков. Эта группа белков получила название белки теплового шока – шапероны (heat shock proteins, Hsp). Позже было установлено, что синтез этих белков индуцируется не только при повышении температуры, но и при многих других неблагоприятных стрессорных на организм воздействиях, а также под влиянием некоторых гормонов и ростовых факторов. В связи с этим белки теплового шока стали называть стресс-белками [6]. Было установлено, что в ответ на тепловой шок в клетках эукариот включается активация транскрипции всех генов, индуцируемых стрессом, осуществляемая специальным транскрипционным фактором (фактор теплового шока HSF). В клетках, не подвергшихся стрессу, HSF присутствует и в цитоплазме и в ядре в виде мономерной формы, связанной с шапероном Hsp70, и не имеет ДНК-связывающей активности.
В ответ на тепловой шок или другой стресс, Hsp70 отсоединяется от HSF и начинает укладывать денатурированные белки. HSF собирается в тримеры, у него появляется ДНК связывающая активность, он аккумулируется в ядре и связывается с промотором. При этом транскрипция шаперонов в клетке возрастает во много раз. После того, как стресс прошел, освободившийся Hsp70 опять присоединяется к HSF, который при этом теряет ДНК-связывающую активность и все возвращается в нормальное состояние. Аналогичным образом все происходит и при других стрессах. Согласно современной классификации, в основу которой положены различия в молекулярных массах, выделяют пять основных классов шаперонов (Hsp): Hsp100, 90, 70, 60 и малые Hsp (small Hsp, sHsp). Каждый из этих классов белков теплового шока выполняет характерные функции. Белки семейства Hsp60 могут участвовать в фолдинге сложно устроенных много доменных белков (таких как актин или тубулин), а также в АТР-зависимом исправлении ошибок в структуре частично денатурированных белков [8]. Hsp90 образуют сложный комплекс с шаперонами. Такой комплекс взаимодействует с рецепторами стероидных гормонов, обеспечивает эффективное связывание гормона с рецепторами и последующий перенос гормон-рецепторного комплекса в ядро. Помимо этого, белки класса Hsp90 участвуют в направленном переносе нескольких типов протеинкиназ к участкам их функционирования [5].
К последней группе белков теплового шока относятся Hsp с малыми молекулярными массами (sHsp – small heat shock proteins) – малые белки теплового шока, выполняющие множество разных функций в клетке. По данным ряда авторов окислительный стресс сопровождается усиленным синтезом sHsp [9]. В настоящее время большая часть исследователей склоняется к заключению, что sHsp защищают клетку от окислительного шока, хотя в литературе высказывается и противоположная точка зрения. Установлено, что N-концевой домен sHsp состоит аминокислотных остатков богатый метионином. Для всех sHsp хлоропластов этот участок очень консервативен и, по всей видимости, участвует в распознавании субстратов [10]. Предполагают, что sHsp каким-то образом активируют или стабилизируют глюкозо-6-фосфат дегидрогеназу – фермент, продуктом которого является NADPH [7]. NADPH используется глутатионредуктазой для поддержания нормального уровня восстановленной формы глутатиона, используемого глутатионпероксидазой для разрушения гидроперекисей. Все эти данные указывают на то, что функциональные эффекты шаперонов связаны с тиоловыми системами, через которые обеспечивается их антиоксидантное и другое действие.
Ранее нами была высказана гипотеза посттрансляционной трансформации нормальных клеточных прионов РrРC в аномальные РrРSс прионы [3]. Причиной появления РrРSс является не копирование конформации с ранее поврежденного приона, а связано с нарушением функции шаперонов контролирующих фолдинг полипетидных цепей нормальных прионов и сохранение их нативной структуры. В частности, аномальные РrРSс за счет гидрофобного взаимодействия с гидрофобными радикалами активного центра тиоредоксинредуктазы и глутатионредуктазы, ингибируют эффекты этих ферментов, необходимых для восстановления тиоредоксина и глутатиона. Эти тиоловые соединения необходимы для как для антиоксидантной защиты, так и для правильной укладки полипептидной цепи белковых молекул, а их недостаток блокирует функцию шаперонов, контролирующих формирование вторичной и третичной структуры нормальных клеточных прионов.
С учетом вышеуказанных позиций, о функциональной связи белков теплового шока с активностью тиоловых систем, нами была поставлена задача, в сравнительном плане изучить состояние глутатиновой редокс-системы и глутатионпероксидазы при перегревании и при охлаждении организма животных, как экспериментальной модели стресса, при которой возможна индукция синтеза стрессорных белков – шаперонов.
Материалы и методы исследования