ген е и ген n коронавирус что такое при исследовании
Генетические варианты SARS-CoV-2: что они означают?
В ходе пандемии, вызванной коронавирусом тяжелого острого респираторного синдрома 2 (SARS-CoV-2), клинические и научные сообщества и системы общественного здравоохранения были вынуждены реагировать на новые генетические варианты вируса. Каждый новый вариант вызвал шквал внимания со стороны средств массовой информации, различные реакции научного сообщества и призывы правительств либо «сохранять спокойствие», либо принять немедленные контрмеры. Хотя многие ученые первоначально скептически относились к значимости мутации D614G, появление нового «британского варианта» — линии B.1.1.7 — вызвало широкую озабоченность. Чтобы понять, какие именно варианты вызывают обеспокоенность и почему, необходимо разобраться в эволюции вируса и геномной эпидемиологии SARS-CoV-2.
Дорогие коллеги, компания BestDoctor ищет среди наших подписчиков людей на позиции врача-консультанта, врача-куратора и врача-терапевта для онлайн-консультаций.
Мутации, варианты и распространение
Мутации возникают как естественный побочный продукт репликации вирусов [1]. Частота мутаций у РНК-вирусов обычно выше, чем у ДНК-вирусов. Однако у коронавирусов происходит меньше мутаций, чем у большинства других РНК-вирусов, потому что они кодируют фермент, который исправляет некоторые ошибки, возникающие во время репликации. Как правило, судьба вновь возникшей мутации определяется естественным отбором. Частота тех мутаций, которые дают вирусу конкурентное преимущество в отношении репликации, распространения или ухода от иммунитета, будет увеличиваться, а те, которые снижают приспособленность вируса, склонны отбраковываться из популяции циркулирующих вирусов. Однако частота мутаций также может увеличиваться и уменьшаться в результате случайных событий. Например, «эффект основателя» возникает, когда в ходе распространения ограниченное число отдельных вирусов создает новую популяцию. Мутации, присутствующие в геномах этих вирусов-предков, будут доминировать в популяции независимо от их влияния на приспособленность. Такое же взаимодействие естественного отбора и случайных событий формирует эволюцию вируса внутри хозяев, в различных сообществах и странах.
Хотя термины «мутация», «вариант» и «штамм» при описании эпидемиологии SARS-CoV-2 часто используются как взаимозаменяемые, важно понимать различия между ними. Термин «мутация» относится к фактическому изменению последовательности (ДНК или белка): D614G обозначает замену аспарагиновой кислоты на глицин в положении 614 гликопротеина шиповидных отростков (S-белка). Геномы, последовательности которых различаются, часто называют вариантами. Этот термин несколько менее точен, поскольку два варианта вируса могут отличаться одной или несколькими мутациями. Строго говоря, вариант — это штамм, обладающий явно отличающимся фенотипом (например, различиями в антигенности, трансмиссивности или вирулентности).
Оценка нового варианта SARS-CoV-2 должна включать в себя ответы на следующие вопросы: достиг ли вариант доминирующего положения в результате естественного отбора или случайных событий? Если имеющиеся данные свидетельствуют о естественном отборе, то какие мутации подверглись отбору? Каково адаптивное преимущество этих мутаций? Какое влияние эти мутации оказывают на трансмиссивность и распространение, антигенность или вирулентность?
Мутация D614G S-белка
Мутация D614G гликопротеина шиповидных отростков (S-белка) SARS-CoV-2 была впервые обнаружена на значительном уровне в начале марта 2020 года и в течение следующего месяца достигла глобального доминирования [2]. По-видимому, изначально мутация возникла независимо и одновременно распространилась по нескольким географическим регионам. Эта очевидная конвергентная эволюция наводит на мысль о естественном отборе и адаптивном преимуществе D614G. Однако при последующих секвенированиях мутация D614G была выявлена в вирусах, которые были распространены в нескольких китайских провинциях в конце января. Это свидетельствует в пользу того, что глобальное распространение этой мутации могло быть результатом случайных событий с «эффектом основателя», когда вирусы, несущие 614G, просто инициировали большинство ранних случаев передачи в нескольких местах.
Такая правдоподобная нулевая гипотеза заставила многих в эволюционном сообществе усомниться, что мутация D614G была адаптивной, несмотря на данные, полученные in vitro, которые показывают ее влияние на связывание с рецепторами. Недавний популяционно-генетический и филодинамический анализ более 25 000 последовательностей из Великобритании показал, что вирусы, несущие 614G, по-видимому, действительно распространяются быстрее и дают начало более крупным филогенетическим кластерам, чем вирусы, несущие 614D [3]. Величина эффекта в данном анализе была умеренной, и различные модели не всегда достигали статистической значимости. Совсем недавно дополнительное исследование на животных показало, что вирусы, несущие 614G, передаются более эффективно [4, 5].
Мутация N453Y S-белка и норки
Тревожные вспышки SARS-CoV-2 начали происходить на норковых фермах в Нидерландах и Дании в конце весны и начале лета 2020 года [6]. Геномные и эпидемиологические исследования ранней вспышки в Нидерландах показали передачу вируса от человека к норке, от норки к норке и от норки к человеку [7]. В начале ноября 2020 года датские власти сообщили о 214 случаях заболевания человека коронавирусной инфекцией (COVID-19), связанных с норковыми фермами. Многие последовательности SARS-CoV-2 в Нидерландах и Дании несли мутацию Y453F в рецептор-связывающем домене S-белка, которая может усиливать его способность связываться с АПФ2 (ангиотензинпревращающим ферментом 2) у норок. У одиннадцати человек, заразившихся во время датской вспышки, обнаружен вариант вируса под названием «кластер 5», несущий в гене S-белка три дополнительные мутации (del69_70, I692V и M1229I). Первоначальное исследование девяти образцов сыворотки выздоравливающих людей показало умеренное и статистически значимое снижение нейтрализующей активности антител против вирусов из кластера 5 (в среднем в 3,58 раза; диапазон 0–13,5). Очевидная адаптация SARS-CoV-2 к норке, тем не менее, вызывает беспокойство, поскольку продолжающаяся эволюция вируса в организме животных-носителей потенциально может привести к повторным передачам нового SARS-CoV-2 от норки к человеку и другим млекопитающим. По этой причине многие страны активизировали усилия по эпиднадзору и в некоторых случаях осуществили крупномасштабные выбраковки (то есть выборочный забой) норок на фермах.
Линия B.1.1.7 и мутация N501Y
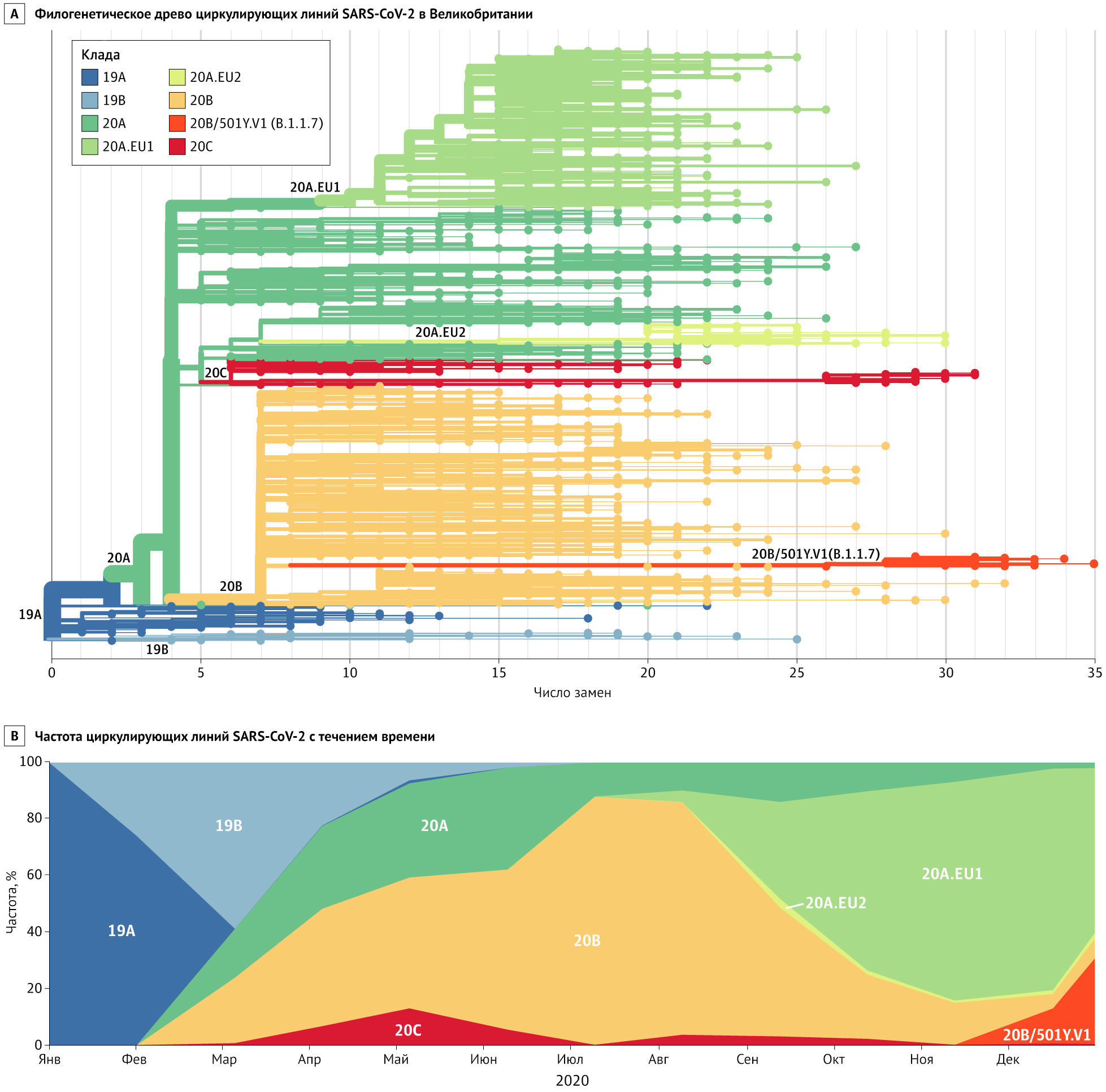
Линия B.1.1.7 (также называемая 501Y.V1) представляет собой филогенетический кластер, который быстро распространяется на юго-востоке Англии [8] (Рисунок). До его обнаружения в начале сентября эта линия накопила 17 специфических мутаций, что свидетельствует о значительной предшествующей эволюции, возможно, в хронически инфицированном хозяине. По состоянию на 28 декабря 2020 года на этот вариант приходилось примерно 28 % случаев заражения SARS-CoV-2 в Англии, и популяционно-генетические модели позволяют предположить, что данная линия распространяется на 56 % быстрее других. В отличие от D614G, для которой, вероятно, могли быть выгодными ранние случайные события, линия B.1.1.7 распространилась, когда SARS-CoV-2 выявлялся уже повсеместно, и, по-видимому, достигла доминирующего положения, превзойдя существующую популяцию циркулирующих вариантов. Это убедительно говорит о естественном отборе вируса с большей трансмиссивностью на популяционном уровне. В то время как меры общественного здравоохранения, такие как маски, соблюдение дистанции и ограничение больших скоплений людей, должны оставаться эффективными, но борьба с более трансмиссивным («более заразным») вариантом, вероятно, потребует более строгого применения и повсеместного принятия этих мер.
Восемь мутаций линии B.1.1.7 затрагивают гликопротеин шиповидных отростков (S-белок), в числе которых N501Y в рецептор-связывающем домене, делеция 69_70 и P681H в сайте расщепления фурином. Все эти мутации могут влиять на связывание АПФ2 и репликацию вируса. Предполагается, что варианты с заменой 501Y в S-белке обладают более высоким сродством к АПФ2 человека. Другой вариант, также с мутацией N501Y, быстро распространяется в Южной Африке. Влияние этих мутаций на антигенность в настоящее время не ясно.
Иммуногенность и эффективность вакцины
Наблюдение за вариантами SARS-CoV-2 в основном сосредоточено на мутациях в гликопротеине шиповидных отростков (S-белке), который опосредует прикрепление к клеткам и является основной мишенью нейтрализующих антител. Существует большой интерес к тому, способствуют ли мутации в S-белке ускользанию от антител хозяина и могут ли они потенциально поставить под угрозу эффективность вакцин, поскольку в современных вакцинах именно S-белок является основным вирусным антигеном. На данном этапе строгий отбор вариантов на уровне популяции, вероятно, не обусловлен антителами хозяина, поскольку на данный момент нет достаточного количества иммунных индивидов для систематического продвижения эволюции вируса в каком-либо определенном направлении. Напротив, если у варианта в S-белке есть одна или несколько мутаций, повышающих трансмиссивность, он может быстро превзойти и вытеснить другие циркулирующие варианты. Поскольку современные вакцины вызывают иммунный ответ на весь S-белок, все еще есть надежда на эффективную защиту, несмотря на некоторые изменения в антигенных участках у различных вариантов SARS-CoV-2.
Разделение причины и следствия важно при оценке данных по нейтрализации антителами вариантов S-белка. Независимо от причины отбора мутации, разумно ожидать, что многие мутации в S-белке могут повлиять на нейтрализацию антителами. Поэтому важно учитывать как уровень изменения нейтрализации, так и количество проанализированных образцов сыворотки. Другая проблема заключается в том, что вирусные гликопротеины подвержены эволюционным компромиссам. Иногда мутация, усиливающая одно свойство вируса, например, связывание с рецептором, может ослабить другое свойство, такое как избегание антител хозяина. Действительно, недавние данные указывают на то, что это может иметь место в случае D614G [10]. Возможно, что мутации в S-белке, которые «полезны» для вируса прямо сейчас, также могут сделать его менее приспособленным к преодолению популяционного иммунитета в будущем. Определение этой динамики и ее потенциального влияния на эффективность вакцин потребует широкомасштабного мониторинга эволюции SARS-CoV-2 и иммунитета хозяина в течение длительного времени.
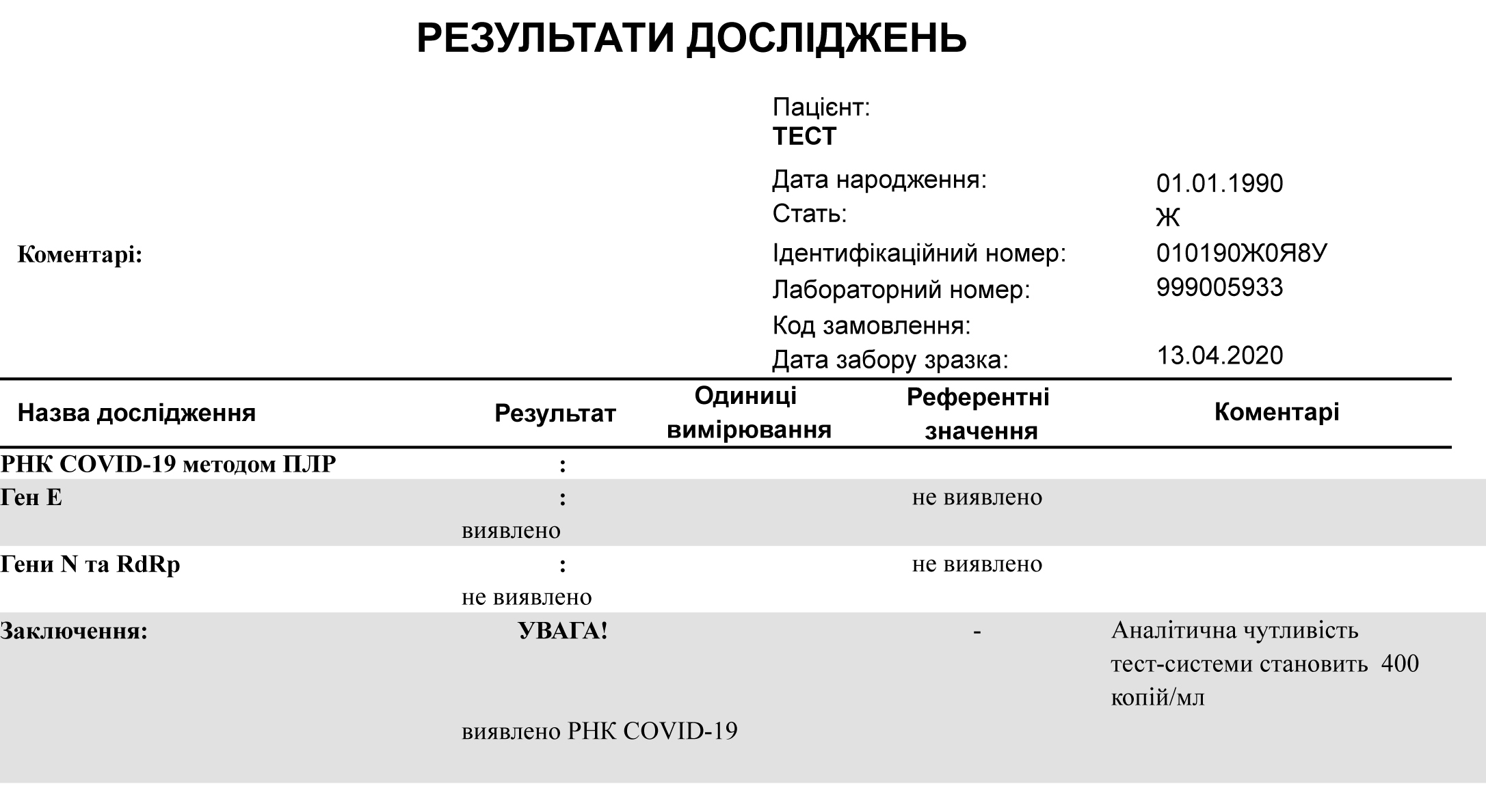
Интерпретация результатов лабораторных исследований на коронавирусную инфекцию
Уважаемые коллеги,
Вашему вниманию второй блок лабораторных алгоритмов COVID-19 – алгоритмы интерпретации.
Хотим отметить, что особенности коронавирусной инфекции и накопленный на сегодня опыт борьбы с ней, не позволяют однозначно использовать традиционные подходы к диагностике вирусных инфекций, как, например, изолированная трактовка результатов иммуноглобулинов. По мере накопления опыта тестирования, мы будем уточнять подходы к интерпретации результатов.
Итак, рассмотрим диагностические варианты:
| 1. | Золотой стандарт диагностики COVID-19 – Коронавирус (SARS-Cov-2), COVID-19, РНК методом RT-ПЦР-качественный (полимеразной цепной реакции) – прямое определение генетического материала возбудителя. |
Это рекомендованный ВОЗ метод идентификации и лабораторного подтверждения случаев COVID-19. Чаще всего проводят исследования биологического материала из ротоглотки или носоглотки.
При наличии клиники, похожей на коронавирусную болезнь и отрицательного результата ПЦР-исследования, рекомендуется повторить ПЦР-исследование из другого образца биологического материала и провести обследование на другие этиологические факторы респираторных заболеваний.
Однократно полученный отрицательный тест на выявление SARS-CoV-2 (особенно, если это образец биологического материала из верхних дыхательных путей) или положительный результат исследования на другой респираторный возбудитель не исключает заражения COVID-19, если существует обоснованное подозрение на инфицирование COVID-19 следует проверить другой образец с помощью других ПЦР-исследований (приказ МЗ Украины №722 от 28.03.2020).
Характеризуется наличием позитивной реакцией на РНК возбудителя COVID-19 при отсутствии заражения вирусом SARS-COV-2.
Причины, которые приводят к такому результату:
| 2. | Серологические методы исследования (выявление IgM, IgG к вирусу SARS-COV-2) определяют напряжение иммунитета у пациентов, инфицированных дольше недели, или уже переболевших коронавирусной болезнью. |
Положительные результаты
Отрицательные результаты серологических тестов не исключают заражения SARS-COV-2, особенно среди тех, кто недавно подвергся контакту с вирусом. Люди с иммунодепрессией могут не выработать иммунный ответ к вирусу SARS-CoV-2.
| 3. | Экспресс-тесты. Предложены для скрининга на коронавирусную болезнь с помощью определения антител к вирусу SARS-COV-2. |
| Таким образом, ранним методом идентификации и лабораторного подтверждения случаев COVID-19 является выявление РНК вируса SARS-COV-2 методом ПЦР |
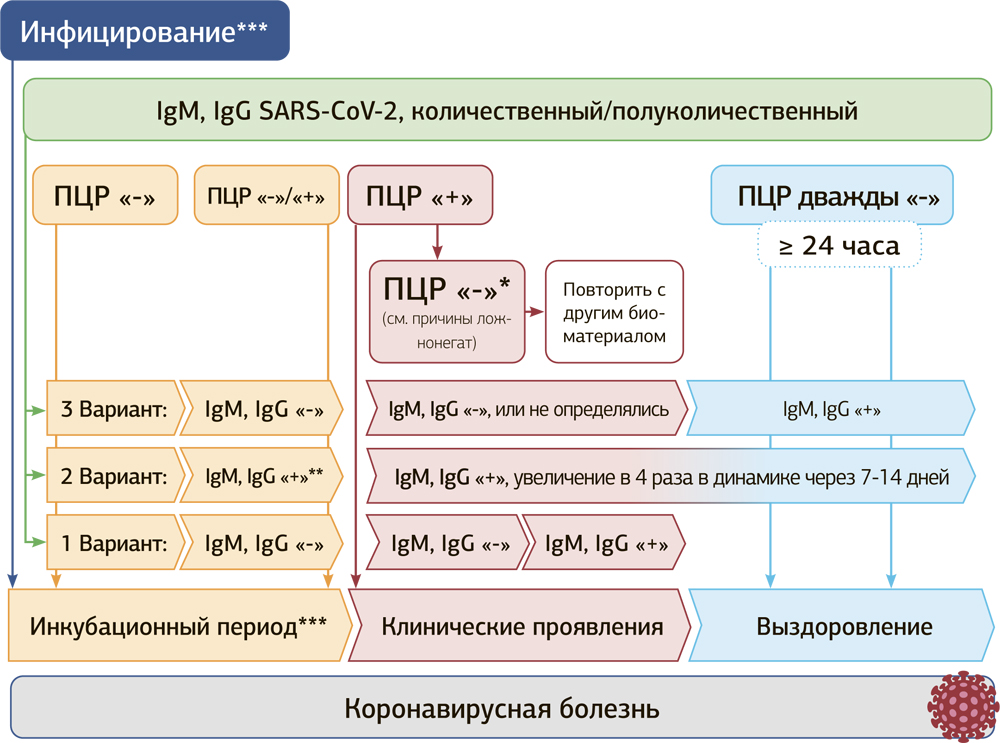
Алгоритм интерпретации результатов лабораторных исследований COVID-19
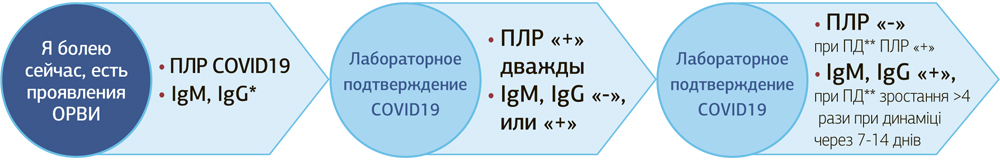
Интерпретация результатов лабораторного обследования в зависимости от анамнеза коронавирусной болезни
 |
 |
 |
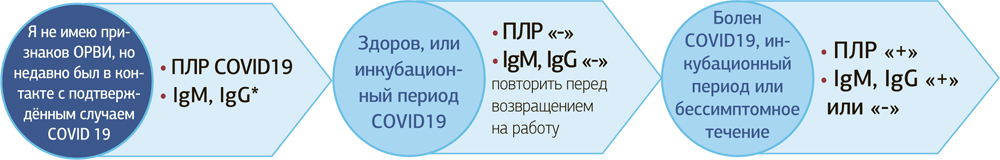 |
* IgM, IgG количественным / полуколичественным аппаратным лабораторным методом (ELISA, ИФА)
** повторном исследовании (ПД) другого биологического материала
*** нельзя исключить бессимптомное течение
Интерпретация диагностических тестов на SARS-CoV-2
Пандемия коронавирусной инфекции 2019 года (COVID-19) продолжает оказывать свое влияние на весь мир. Знания о диагностических тестах на SARS-CoV-2 по-прежнему расширяются, и крайне важным является понимание смысла этих тестов и правильная интерпретация их данных. Этот материал объясняет, как интерпретировать два типа диагностических тестов, обычно используемых для диагностики инфекции, вызванной SARS-CoV-2 — ПЦР с обратной транскрипцией и ИФА для определения IgG и IgM — и как их результаты могут изменяться с течением времени.
.
Определение вирусной РНК методом обратной транскрипции
На сегодняшний день наиболее часто используемый и достоверный тест для диагностики COVID-19 — это ПЦР с обратной транскрипцией. В качестве материала для исследования чаще всего используют мазок из носоглотки или реже другие образцы из верхних дыхательных путей, например, мазок из ротоглотки или слюну. Производители используют разные целевые гены в структуре РНК, но большинство тестов определяет наличие таких генов, как env, spike (S), ORF1, ген нуклеокапсида (N) и ген РНК-зависимой РНК полимеразы (RdRp). По данным сравнительного исследования, тесты сопоставимо чувствительны к различным индивидуальным генам; исключение составляет зонд RdRp-SARSr, который обладает меньшей чувствительностью (вероятно, из-за несоответствия нуклеотидов в обратном праймере).
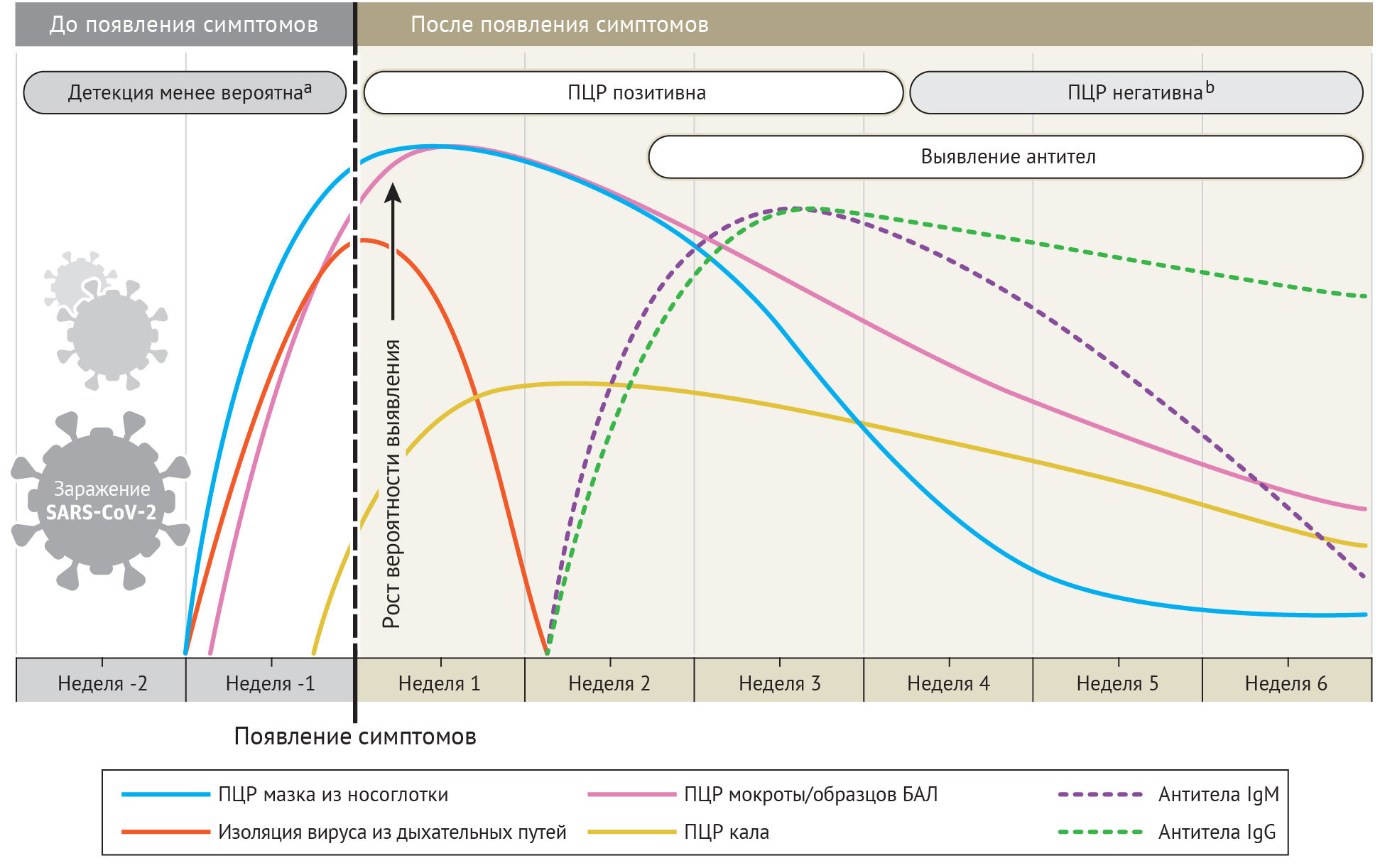
У большинства людей с симптомами коронавирусной инфекции нагрузка вирусной РНК в мазке из носоглотки определяется по порогу числа циклов (cycle treshold, Ct), выявляется со дня появления симптомов и становится максимальной в течение первой недели. Ct — это количество циклов репликации, необходимое для формирования флюоресцентного сигнала. При этом наименьший показатель Ct соответствует наибольшей нагрузке вирусной РНК. Показатель Ct менее, чем 40, клинически соответствует положительной ПЦР. Этот уровень начинает снижаться к третьей неделе заболевания и вскоре становится неопределяемым. Показатель Ct у госпитализированных пациентов с тяжелыми случаями инфекции ниже такового при легко протекающих формах; в тяжелых случаях положительная ПЦР может отмечаться более трех недель с момента начала заболевания, тогда как большинство легких случаев в это время будут показывать негативный результат. Как бы то ни было, положительная ПЦР отражает только присутствие вирусной РНК и не обязательно показывает наличие жизнеспособных вирусов.
В некоторых случаях вирусная РНК определяется методом ПЦР с обратной транскрипцией даже через шесть недель после первого позитивного теста. В нескольких случаях тест был положителен после двух последовательных негативных тестов ПЦР, проведенных с разницей в 24 часа. Неясно, было это обусловлено ошибкой в исследовании, реинфекцией или реактивацией. В исследовании девяти пациентов попытки изолировать вирус в культуре после восьмого дня с момента начала заболевания не увенчались успехом, что объясняется снижением инфекционных свойств вируса после первой недели. Отчасти поэтому «стратегия, основанная на симптомах» Центра по контролю и профилактике заболеваний показывает, что «медицинские работники могут приступить к работе, если как минимум три дня (72 часа) прошло с момента выздоровления: отсутствие лихорадки без применения антипиретиков и снижение респираторных симптомов (кашель, затруднение дыхания); и как минимум 10 дней прошло с того момента, как симптомы впервые появились».
Временная шкала изменения результатов ПЦР изменяется, если в качестве образцов используют не мазок из носоглотки. «Позитивность» ПЦР снижается медленнее в мокроте и может быть выявлена даже после того, как мазки из носоглотки уже отрицательны. В одном исследовании ПЦР была позитивна в образцах кала у 55 из 96 инфицированных пациентов (57 %) и оставалась позитивной после получения отрицательного результата в мазке из носоглотки с медианой 4–11 дней. При этом обнаружение позитивной ПЦР в кале не коррелировало с клинической тяжестью процесса. По оценкам Wolfel с соавт. длительность выявления положительной ПЦР в мокроте и кале одинакова.
В исследовании 205 пациентов с подтвержденной коронавирусной инфекцией вирусная нагрузка, выявленная ПЦР с обратной транскрипцией, была высокой в образцах, полученных методом бронхоальвеолярного лаважа (93 %), в мокроте (72 %), назофарингеальных мазках (63 %) и глоточных мазках (32 %). Ложноотрицательные результаты в основном появлялись при несоблюдении временного интервала забора образцов и нарушении техники забора, особенно в случае мазков из носоглотки. Специфичность большинства тестов ПЦР с обратной транскрипцией составляет 100 %, потому что дизайн праймеров высоко специфичен к геномной последовательности SARS-CoV-2. Случайные ложнопозитивные результаты могут появляться вследствие технических ошибок или контаминации образца.
Выявление антител к SARS-CoV-2
Инфицирование коронавирусом также может быть определено непрямым способом — путем исследования иммунного ответа пациента. Серологический диагноз особенно важен для пациентов с легкими или среднетяжелыми формами, которые могут начать наблюдаться поздно, по прошествии первых двух недель от начала заболевания. Серологический диагноз также становится важным инструментом для понимания степени распространения COVID-19 в популяции и выявления лиц, иммунизированных и «защищенных» от заражения.
Наиболее чувствительным и ранним серологическим маркером является общий уровень антител. Уровни IgM и IgG начинают нарастать со второй недели с момента появления симптомов; ИФА для их определения обычно становится положительным раньше, на четвертый день после появления симптомов, достигая максимального уровня на 2–3 недели заболевания.
Как было показано на 23 пациентах в исследовании To и соавт. и 85 пациентах в исследовании Xiang с соавт., сероконверсия IgM и IgG появляется у всех пациентов между третьей и четвертой неделями заболевания. К этому времени уровень IgM начинает снижаться, достигает наименьшего значения к 5 неделе и полностью исчезает к седьмой неделе, тогда как IgG выявляется позже седьмой недели. В исследовании 140 пациентов, чувствительность комбинации методов ПЦР и ИФА в отношении антигена нуклеокапсида (NC) составила 98,6 % в сравнении с таковой в 51,9 % у одной ПЦР. В течение первых 5,5 дней количественная ПЦР имеет более высокий рейтинг выявления положительных случаев, чем ИФА, затем этот показатель меняется.
ИФА для определения IgM и IgG имеет более чем 95 % специфичность для диагностики COVID-19. Первоначальная ПЦР, исследование парных сывороток и второе исследование через две недели могут повысить точность диагностики. Как правило, большинство антител продуцируются против наиболее интенсивно вырабатываемого протеина вируса — нуклеокапсида. Поэтому тесты, которые выявляют антитела к нуклеокапсиду, должны быть более чувствительными. С другой стороны, белок RBD-S — это белок прикрепления из организма хозяина, и исследование антител к нему должно быть более специфичным. Исследование одного или обоих антигенов для выявления IgG и IgM должно повысить общую чувствительность. Антитела могут, однако, показывать перекрестную реактивность в отношении SARS-CoV-2 и других коронавирусов.
Экспресс-тесты для детекции антител широко разрабатываются и продаются, имея при этом разный уровень качества. Многие производители не раскрывают природу используемых антигенов. Эти тесты редко показывают результат в качественном отношении; как правило, ими можно выявить только присутствие или отсутствие антител против SARS-CoV-2. Наличие нейтрализующих антител может показать только реакция нейтрализации, но высокие титры IgG в ИФА могут позитивно коррелировать с уровнем нейтрализующих антител. Длительность существование и функционирования нейтрализующих антител остается неизвестной.
Выводы
С использованием доступных доказательств была выработана клинически применимая временная шкала диагностических маркеров для детекции COVID-19. Большинство доступных сведений актуальны для взрослых не иммунокомпрометированных лиц. Время обнаружения положительной ПЦР и сероконверсии может изменяться у детей и некоторых групп взрослых, включая большое число бессимптомных пациентов, диагностика коронавирусной инфекции у которых требует активного вмешательства. Остается много вопросов, например, как долго сохраняется иммунитет у перенесших COVID-19 лиц с симптомами и без таковых.
Новые ущербы от инфекции SARS-CoV-2 за пределами дыхательной системы
Автор
Редакторы
Статья на конкурс «Био/Мол/Текст»: Все мы помним, как с начала декабря 2019 года в китайском городе Ухань был выявлен ряд случаев пневмонии, связанных с коронавирусной инфекцией COVID-19 c серьезными симптомами, такими как респираторные проблемы (кашель, одышка, поражение легких) и лихорадка. Но вы когда-нибудь задумывались о том, что же происходит с остальными органами нашего тела? Так давайте разберём, как крошечный вирус может поражать не только дыхательную систему, но и вызвать повреждение других систем человеческого организма.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Школьная» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Партнеры номинации — медико-биологическая школа «Вита» и «Новая школа».
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Введение
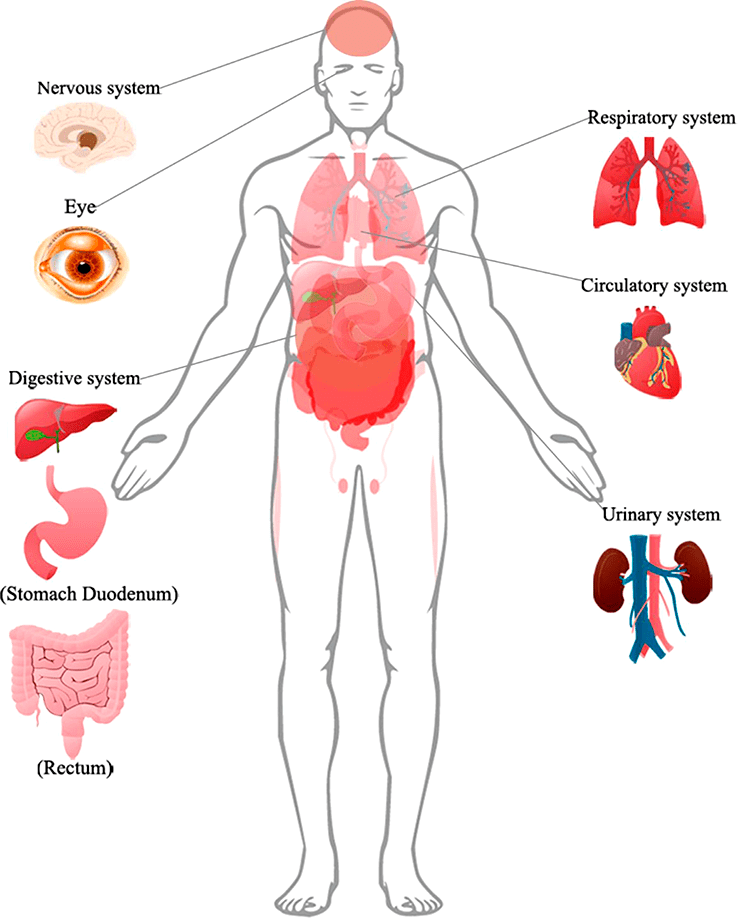
Согласно исследованиям немецких ученых, SARS-CoV-2 проникает внутрь организма с помощью клеточного рецептора — ангиотензинпревращающего фермента 2 (АПФ2; ACE2 — англ.), который специфически синтезируется в определенных органах и тканях. Соответственно, ACE2 играет важную роль в регуляции сердечно-сосудистой, кишечной, почечной и репродуктивной функций [1]. Попав в систему кровообращения, коронавирус, вероятнее всего, распространяется через кровоток [2]. Следуя этим данным, мы можем понять, как SARS-CoV-2 заражает не только дыхательную систему, но и представляет потенциальную угрозу для пищеварительной и мочеполовой систем, ЦНС и системы кровообращения.
Рисунок 1. Поражения органов, подтвержденные клиническими признаками или биопсией, у пациентов с COVID-19
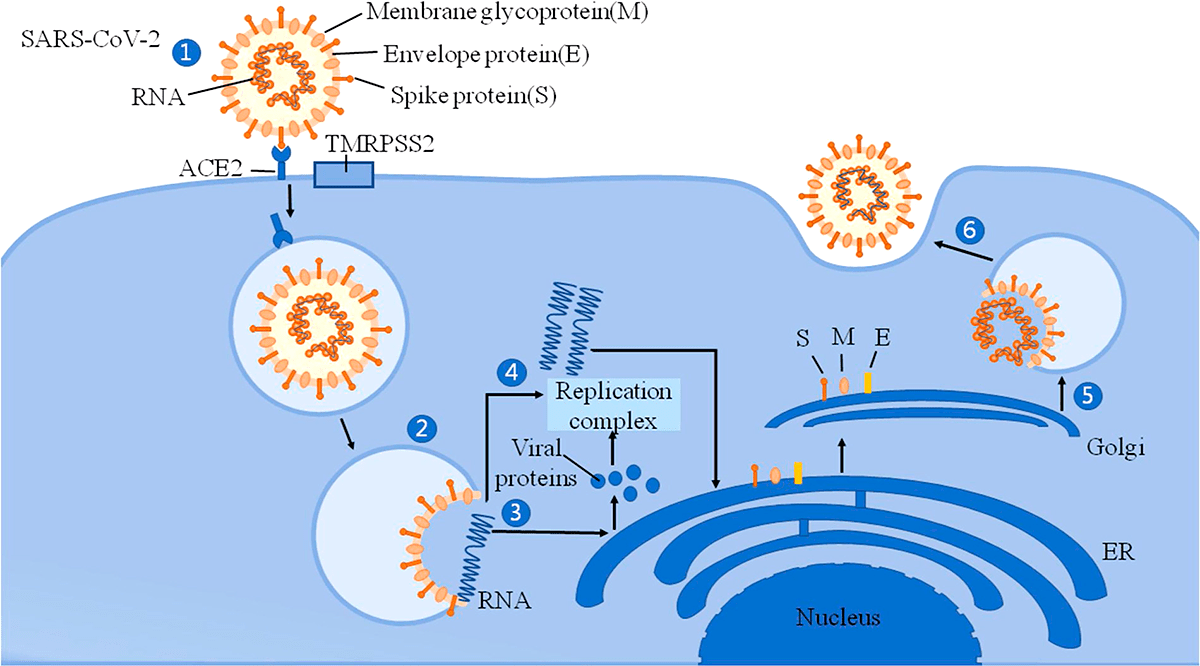
Рисунок 2. Механизм вторжения SARS-CoV-2 в клетку
SARS-CoV-2 и пищеварительная система
Помимо главного рецептора ACE2, SARS-CoV-2 использует трансмембранную сериновую протеазу 2 (TMRPSS2), фермент, который также экспонируется на эпителиальных клетках тонкой кишки. Он способствует проникновению вируса в клетки [3]. Активность SARS-CoV-2 может вызывать модификации ACE2 в кишечнике, которые повышают восприимчивость к воспалению кишечника и диарее. ACE2 оказывает значительное влияние на состав кишечной микробиоты [4]. Первичные воспалительные стимулы вызывают высвобождение в систему кровообращения микробных продуктов и цитокинов, которые могут вызвать микробный дисбиоз и воспалительную реакцию.
Изменения микробиоты кишечника могут быть связаны с изменениями в иммунной системе и предрасположенностью к более серьезным последствиям COVID-19. Наш микробиом меняется с возрастом: в первые несколько лет жизни микробиота малоразнообразна и нестабильна [5], [6]; во взрослом возрасте стабильна и разнообразна, а к пожилому возрасту разнообразие микробиоты уменьшается, а дисбиоз увеличивается, что связывают с когнитивным дефицитом, депрессией и воспалением [7]. Сниженное разнообразие микробиоты — еще один фактор риска заражения COVID-19 для пожилых людей.
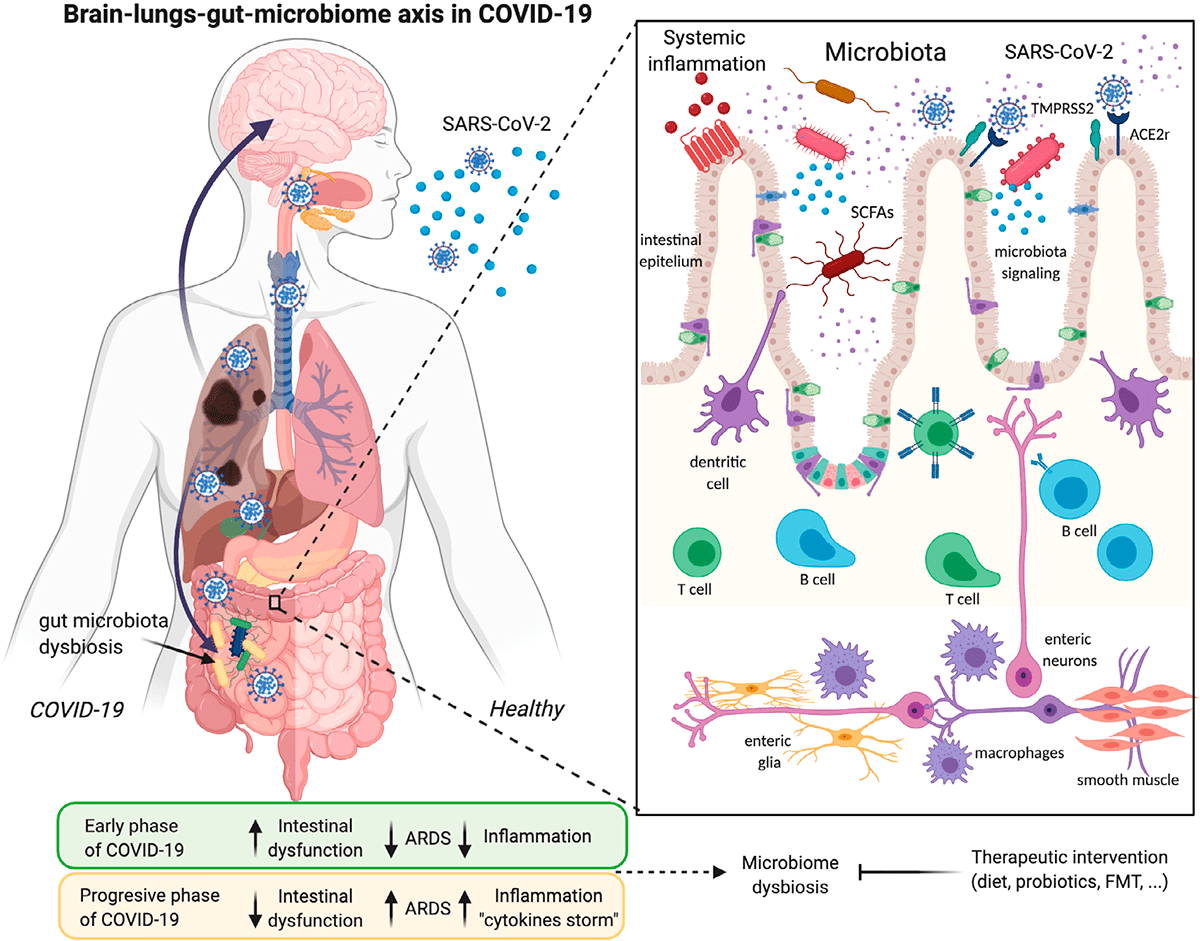
Рисунок 3. Инфекция SARS-CoV-2 и ее связи с осью легких—кишечника—мозга и дисбиозом микробиома
Изменение кишечной флоры также связано с ожирением, еще одним фактором риска для тяжелого течения COVID-19 [8], [9]. Жировая ткань может служить резервуаром для распространения SARS-CoV-2 и активации системного иммунитета [10]. Коронавирусная инфекция вызывает изменения в кишечной бактериальной флоре, которые могут повлиять на ось «кишечник—мозг». Таким образом, кишечная флора играет решающую роль в регуляции неврологических функций, таких как депрессия или тревога [11].
Следовательно, режим питания играет значительную роль во время заражения вирусом SARS-CoV-2. Из-за вирусной инфекции иногда начинается дисбиоз, который может быть скомпенсирован компонентами диеты и пробиотиками [12]. Несколько исследований показывают, что оптимальный иммунный ответ зависит от правильного питания [13], [14]. Недоедание может поставить под угрозу иммунитет, тем самым влияя на уязвимость ответа на COVID-19. Потребление достаточного количества белка имеет решающее значение для выработки антител, поддержания ворсинчатой морфологии кишечника и уровня кишечного иммуноглобулина, что улучшает кишечный барьер [15–17]. Таким образом, высококачественные белки являются важным компонентом противовоспалительной диеты, которая включает омега-3 жирные кислоты, витамины С и Е, фитохимические вещества, которые широко присутствуют в продуктах растительного происхождения (фруктах, овощах, орехах, злаках и т.д.) [18–21]. Правильная диета укрепляет иммунную систему и способствует защите организма от тяжелого течения COVID-19.
SARS-CoV-2 и центральная нервная система (ЦНС)
Кроме пищеварительной системы, коронавирусная инфекция (COVID-19) также затрагивает центральную и периферическую нервную систему. Неврологические проявления могут возникать по разным причинам, включая прямое вирусное поражение центральной нервной системы (ЦНС) и иммунноопосредованные процессы. Примеры заболеваний ЦНС при COVID-19 могут включать энцефалит (воспаление головного мозга), менингит и инсульт. В периферической нервной системе COVID-19 ассоциируется с дисфункцией обоняния и вкуса, повреждением мышц и синдромом Гийена—Барре, при котором иммунная система человека поражает собственные периферические нервы.
Рисунок 4. Коронавирусная инфекция и нервная система
Ученые Университета Гонконга отметили, что механизмы инфекции SARS-CoV-2 могут быть аналогичны механизмам инфекции SARS-CoV из-за 79,5% сходства последовательностей РНК этих двух коронавирусов [22]. Однако SARS-CoV-2 обладает более мощной способностью к распространению, чем SARS-CoV и MERS-CoV. Причина в том, что SARS-CoV-2 и ACE2 обладают более сильной связывающей способностью [23]. S-белок (спайк-белок) на поверхности коронавируса связывается с ACE2 и прикрепляется к поверхности клетки; затем сериновая протеаза (TMPRSS2) активирует S-белок, что помогает вирусу проникать в нейрон [1]. Так как клетки кровеносных сосудов экспонируют ACE2 в большом количестве, SARS-CoV-2 может атаковать эндотелиальные клетки в кровеносных сосудах головного мозга через этот рецептор и нарушить гематоэнцефалический барьер (ГЭБ — барьер между кровеносной системой и центральной нервной системой). Нарушенный ГЭБ может способствовать вторжению вируса в ткани мозга и нейроны и привести к серьезным неврологическим осложнениям [24].
SARS-CoV-2 и система кровообращения
Помимо дыхательных путей, SARS-CoV-2 поражает сердечно-сосудистую систему. Это приводит к высвобождению высокочувствительных сердечных тропонинов (hs-cTnl) — белков, содержащихся в сердце и скелетных мышцах человека. В процессе заражения мембраносвязанный белок ACE2 может расщепляться трансмембранным дезинтегрином ADAM17, высвобождая ACE2 в кровоток. Таким образом, вирус циркулирует в крови зараженного организма. Воспаление сосудистой системы и миокарда может привести к миокардиту, сердечной недостаточности и быстрому ухудшению состояния больного [25].
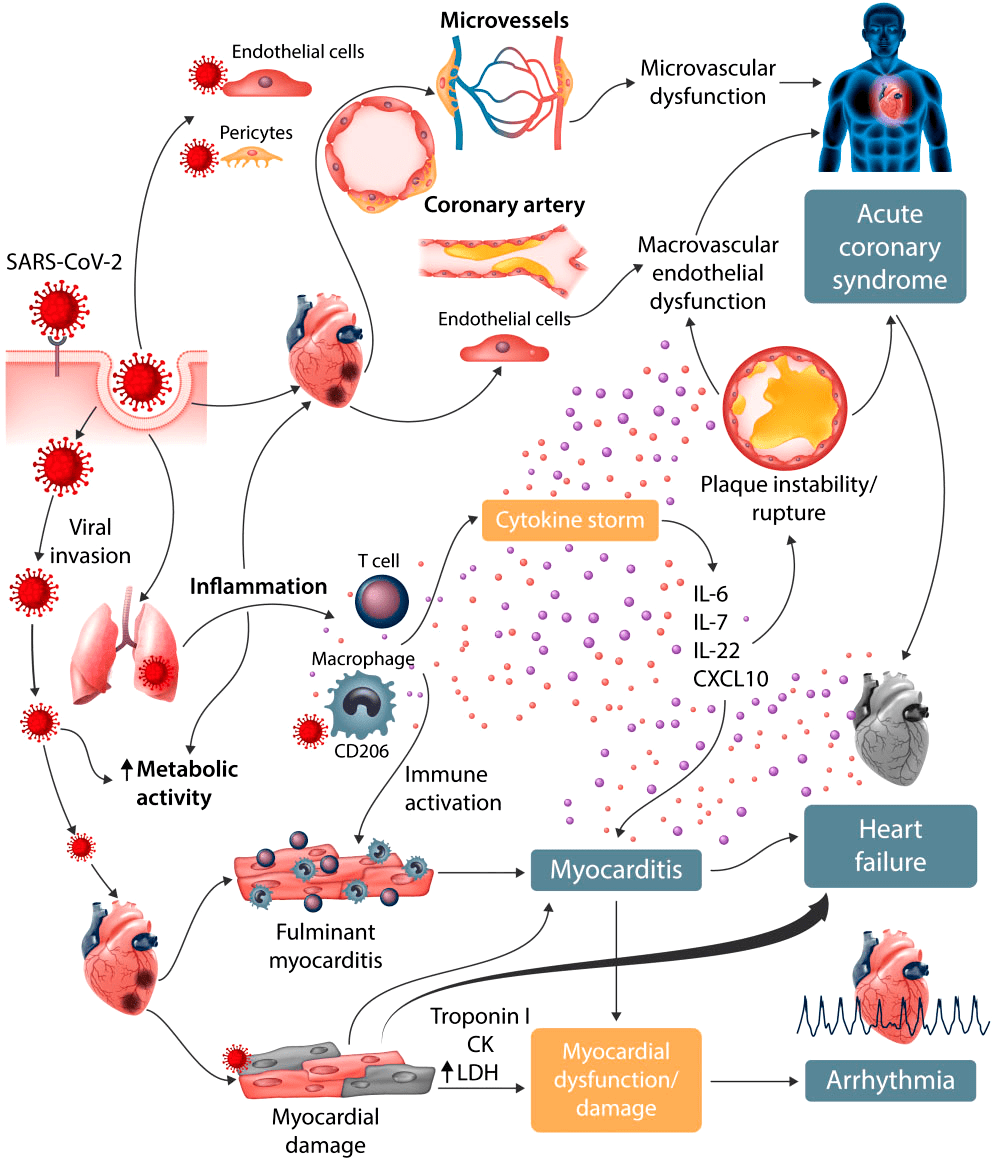
Рисунок 5. Сердечно-сосудистое поражение при COVID-19
SARS-CoV-2 и мочеполовая система
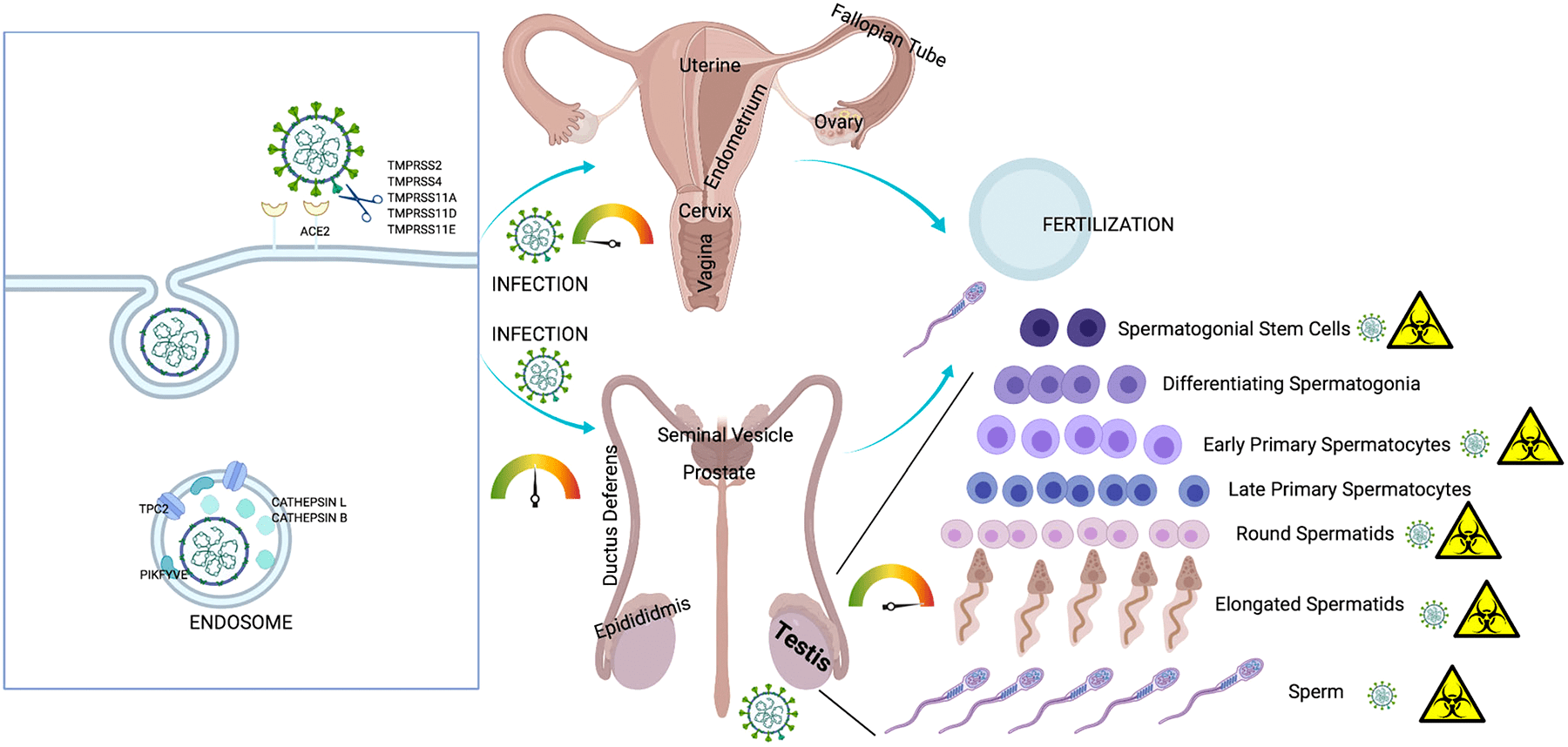
Инфекция репродуктивной системы требует большего внимания, потому что она не только влияет на нынешнее поколение, но также может распространяться на потомство через поврежденные гаметы. На сегодняшний день несколько исследований подтвердили влияние SARS-CoV-2 как на мужскую, так и на женскую репродуктивную систему [26], [27]. В настоящее время хорошо известен факт, что мужчины более восприимчивы к инфекции SARS-CoV-2 и у них выше уровень смертности, чем у женщин. Это объясняется тем, что клетки семенного протока и сперматогонии синтезируют много ACE2 [28–30].
По мнению ученых, SARS-CoV-2 нарушает репродуктивные функции мужчин через несколько механизмов, таких как воспалительные реакции, окислительный стресс и апоптоз [31–33]. Инфекция SARS-CoV-2 приводит к перепроизводству активных форм кислорода, которые могут усиливать внутриклеточные сигнальные пути (NF-κB-TLR). Это приводит к высвобождению цитокинов, что еще больше усиливает воспалительный ответ. К примеру, орхит, вызванный инфекцией SARS-CoV-2, может привести к окислительному стрессу в тканях яичка. Окислительный стресс может вызвать внутриклеточное окислительное повреждение сперматозоидов, что приводит к ухудшению их качества и мужскому бесплодию.
Рисунок 6. Инфекция SARS-CoV-2 и репродуктивная система
Рецепторы ACE2 были также обнаружены в женских яичниках [34], [35]. Можно предположить, что SARS-CoV-2 поражает ткань яичников и клетки гранулезы и таким образом ухудшает функцию яичников и жизнеспособность ооцитов, что может привести к бесплодию или невынашиванию [33]. Недавно ученые (Виванти и др.) сообщили о трансплацентарной передаче вируса от матери, инфицированной COVID-19, новорожденному. Мать была инфицирована в последнем триместре беременности, и гены SARS-CoV-2 были обнаружены в ткани плаценты. Согласно этому отчету, трансплацентарная передача может привести к воспалению плаценты [36]. Однако стоит отметить, что плацента имеет плацентарный барьер, который не смешивает кровь матери и плода, тем самым защищая плод от всех видов материнской инфекции. Невосприимчивые клетки плаценты обладают противовирусными свойствами, которые дополнительно предотвращают проникновение SARS-CoV-2 в клетки ребенка [37].
Вывод
Прочитав эту статью, мы с вами узнали, как вирус поражает не только дыхательную систему, но и другие системы человека. Это осложняет потенциальные клинические проявления и затрудняет лечение случаев COVID-19. Однако биомедицинские исследования могут помочь нам больше узнать о способностях нового коронавируса и о том, как с ним бороться, чтобы определить важные ориентиры для дальнейших исследований, диагностики и лечения. Также стоит всегда помнить, что соблюдая правильную диету и карантинные меры, мы снижаем риски заражения и ухудшения состояния здоровья во время COVID-19. Ведь вирус не всегда может вызвать вышеуказанные осложнения, если мы будем правильно заботиться о своем здоровье.