генетик перед эко зачем
Вопросы о генетике
Зачем нужна консультация у генетика? Своевременно проведенная консультация и диагностика у генетика может помочь человеку или молодой семье заметно снизить риск проявления наследственных заболеваний (например, рака или кистозного фиброза). После консультации вы получите информацию обо всех болезнях и оценку риска унаследования их будущим ребенком.
Что делает врач-генетик? Он предоставляет молодой семье исчерпывающую информацию о врожденных дефектах или генетических нарушениях каждого из членов. Он ответит на все вопросы и проведет диагностику, после которой будет проще планировать зачатие ребенка.
В каких случаях требуется консультация генетика? Она требуется, когда в семье есть некое генетическое заболевание, которое может проявиться или передаться детям. Также очень важно пройти консультацию, когда семья планирует ребенка, когда есть подозрения на наличие заболевания. Если у ребенка есть проблемы, и в них может быть виновата наследственность. Если в семье были случаи рака, и вы хотите оценить риск его возникновения. Если семья уже ожидает ребенка, но получила неудовлетворительные анализы.
Что такое генетика? Это направление в медицине, которое занимается изучением генов и способов их передачи будущим поколениям. Например, когда требуется понять, есть ли в семье наследственное заболевание или мутированный ген, который передается от родителей к детям.
Что собой представляет посещение врача-генетика? Всё зависит от причины посещения врача. Обычно он дает информацию о самых часто встречающихся заболеваниях, общается с вами и, возможно, другими родственниками, чтобы получить примерную картину наследственных заболеваний. Врач определяет риски их проявления, изучает историю вашей семьи и партнера, составляет родословное древо. С врачом вы обсуждаете необходимость тех или иных тестов, далее вы направляетесь на сдачу анализов. Через какое-то время генетик рассказывает вам о результатах, информирует о том, где можно получить поддержку или пройти лечение.
Какая стоимость услуг? Так как генетическая диагностика требует самого современного и очень сложного оборудования, проведения трудоемкого анализа и привлечения узкоспециализированных профессионалов, стоит она дорого. Однако прогресс не стоит на месте, и уже сейчас подобная диагностика стала намного доступнее, чем это было всего 5 лет назад.
Процедура является безболезненной? В зависимости от конкретного случая, генетический анализ может браться из слюны, крови, волос, стула, мочи и пр. Чаще всего делается генетический анализ крови из вены. Сам по себе процесс не причиняет боли, но может доставлять дискомфорт. Болезненность сильно зависит от навыков медработника, а также от индивидуальной чувствительности. При взятии слюны, мочи или спермы дискомфорт не испытывается.
Обязательно ли нужны оба супруга? Конечно, ведь они оба участвуют в планировании беременности и зачатии ребенка. Более того, для составления верной картины могут понадобиться и другие родственники, с которыми также может быть проведена консультация.
Как подготовиться к посещению генетика? Желательно заранее провести небольшое самостоятельно исследование – спросить родственников обоих супругов, какие заболевания они пережили в детстве и в жизни в целом. Также рекомендуется заранее проконсультироваться со своим терапевтом, сделать выписку из амбулаторной справки, уточнить у врача, можно ли вам делать те или иные виды анализов (например, при плохой свертываемости крови не рекомендуется проводить ее анализ). Всё это сэкономит время и сделает первое посещение генетика более плодотворным.
Что такое риск развития заболевания? Это значит, что человек унаследовал мутированный (измененный) ген, и он может проявить заболевание как сразу после рождения, так и в течение жизни.
В медицинской практике данный вид анализа относится к специфическому.
Предымплантационное генетическое тестирование при ЭКО
Количество женщин, пользующихся услугами центров репродуктивных технологий, за последние двадцать лет значительно возросло. Это объясняется тем, что семейные пары начинают планирование беременности в более позднем возрасте. Также расширен список диагнозов, при которых в прошлом беременность была невозможна, а сейчас многие пары могут иметь детей. В этих случаях, как правило, им на помощь приходит экстракорпоральное оплодотворение (ЭКО).
Факторы, влияющие на успех ЭКО
Казалось бы, что с увеличением количества ЭКО должен значительно вырасти уровень успеха этой процедуры. Однако, как показывают результаты многочисленных исследований на эту тему, несмотря на популярность ЭКО, улучшение диагностики бесплодия до этой процедуры, лучшее оснащение, лучший подбор лекарственных препаратов и разнообразие протоколов, процент успешных клинических беременностей изменился незначительно и продолжает оставаться в пределах 27–35 % случаев рождения живых детей уже многие годы. Оказалось, что успех процедуры мало зависит от тщательной подготовки эндометрия, техники переноса эмбрионов и поддерживающей гормональной терапии, а непосредственно связан только с качеством эмбрионов. А качество эмбрионов, в свою очередь, зависит от возрастного фактора.
Но так как далеко не все семейные пары способны иметь детей в более молодом возрасте, все чаще поднимается вопрос о том, как можно определить качество эмбрионов, особенно наличие отклонений в их хромосомном наборе. Также вопрос качества эмбрионов в отношении наличия определенных генов поднимаю те пары, у которых имеется семейная история заболеваний, связанных с наследственностью, то есть для них особенно важна хромосомно-генетическая характеристика — наличие генов или дефектов генов, причастных к возникновению серьезных заболеваний и пороков развития.
До сих пор во многих лечебных учреждениях отдают предпочтение традиционной инвазивной процедуре — забору ворсин хориона для изучения набора хромосом будущего ребенка (кариотипа), который обычно проводится на ранних сроках беременности. Если в кариотипе находят отклонения или измененные гены, женщине могут предложить прервать беременность. Но каково при этом бывает разочарование пар, которые потратили большие суммы на проведение ЭКО, получили желанный результат и столкнулись с дилеммой сохранения заведомо проблемной беременности или ее прерывания из-за дефекта хромосом и генов!
В большинстве публикаций, посвященных теме репродуктивных технологий, фигурируют данные о большей частоте пороков развития у плодов и новорожденных после ЭКО по сравнению с общей популяцией. Однако недавно появились данные, что предымплантационное генетическое тестирование не только понижает количество беременностей с плодами, пораженными пороками развития, хромосомными и генетическими заболеваниями, но и повышает уровень успешного проведения ЭКО и рождения здоровых детей. Объясняются эти утешительные сведения тем, что такое тестирование может отсеять дефектные эмбрионы еще до проведения ЭКО. Фактически проводится селекция здоровых эмбрионов, использование которых повысит шансы на получение здорового потомства.
Вокруг предымплантационного генетического тестирования в недавнем прошлом разгоралось много дискуссий, особенно в плане безопасности этой процедуры для самого эмбриона. Поскольку этот вид тестирования недешевый и требует как сложного технического оснащения, так и специалистов для его проведения и интерпретации, стоимость ЭКО в целом повышается. А значит, повышается и частота злоупотребления этим тестированием.
Виды предымплантационного тестирования
В современной репродуктивной медицине имеются две разновидности предымплантационного тестирования: предымплантационный генетический скрининг (ПГС) и предымплантационная генетическая диагностика (ПГД). В реальности четких отличий между двумя видами тестирования не существуют, так как они проводятся практически одними и теми же методами, но цели их проведения все же отличаются.
При ПГС проводят выявление (случайное) аномального хромосомного набора у эмбрионов, готовых к подсадке, и чаще всего этим видом тестирования пользуются в тех случаях, когда важную роль играет возрастной фактор. От 40 до 60 % всех эмбрионов вообще — некачественные, а с возрастом количество бракованных эмбрионов возрастает, к 40 годам достигая 80 %, что понижает уровень успешной имплантации после ЭКО до 6 %. Поэтому все чаще предимплантационный генетический скрининг используют у пар старше 35–37 лет, хотя четких рекомендаций, с какого возраста проводить ПГС, пока не существует.
В отличие от диагностики, скрининг может быть поверхностным, то есть с его помощью выясняют общее количество хромосом и отсутствие грубых «поломок» в них.
ПГД позволяет определить наличие пораженных генов или изменения в хромосомах при наличии в роду или семье генетических и хромосомных заболеваний. Существует около 200 заболеваний, связанных с поломкой всего лишь одного гена (кистозный фиброз, бета-талассемия, миотоническая дистрофия, синдром Марфана, мышечная дистрофия Дюшенна, гемофилия А и др.), включая возникновение наследственных видов рака (ретинобластома, рак молочной железы и др.).
Также подобная диагностика важна для определения пола будущего ребенка, поскольку ряд наследственных заболеваний может передаваться исключительно через половые хромосомы.
Технология проведения тестирования
Существует несколько технологий определения кариотипа и ДНК, в том числе полученной всего из одной клетки. Все технологии имеют свои преимущества и недостатки, поэтому результаты могут быть и ложно-положительными, и ложно-отрицательными, что требует от врача учета многих других важных фактов из истории семейной пары для принятия правильного решения.
Материал для исследования путем биопсии может быть получен из оплодотворенной яйцеклетки (через 8–14 часов после ее оплодотворения), и обычно такое тестирование проводится в странах, где получение клеток эмбриона запрещено. Этот сложный метод тестирования также имеет много погрешностей.
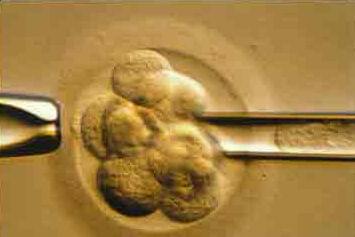
После оплодотворения яйцеклетка начинает делиться без увеличения ее размеров, что приводит к возникновению бластомера: сначала 2 клетки, дальше — 4, 8 и 16 клеток. При проведении биопсии используют обычно 1 клетку на стадии 8-клеточного (3-дневного) эмбриона. В прошлом для тестирования брали две клетки, но оказалось, что забор ¼ (25 %) клеточного состава будущего ребенка часто негативно отражался на развитии эмбриона. Также наблюдалась потеря других клеток (до 33 % клеточного состава эмбриона). На получение результатов уходит от 1 до 2 дней, поэтому подсадку проводят чаще всего на 5–6 день развития эмбриона. Такой вид биопсии сопровождается худшим уровнем имплантации эмбрионов — она снижается до 39 %.
Деление бластомера продолжается и начинают формироваться определенные части плодного яйца — так возникает морула, а за ней бластоцист, который содержит внутри уже небольшое количество жидкости, что позволяет провести забор от 5 до 10 клеток эмбриона. Большее количество клеток для исследования повышает качество диагностики, поэтому таким видом предымплантационного генетического тестирования сейчас стали пользоваться чаще.
Как показывают клинические исследования, ПГС и ПГД с использованием бластоциста не отражаются негативно на развитии эмбриона, одновременно улучшая качество и успех ЭКО, хотя при этом виде тестирования увеличивается количество женщин, которым ЭКО не проводят. Если не удается получить качественные и генетически здоровые эмбрионы, семейной паре могут предложить донорские яйцеклетки, или сперматозоиды, или готовые эмбрионы.
К сожалению, далеко не все репродуктивные клиники проводят предымплантационное генетическое тестирование. Качество эмбрионов в них определяется визуально — с учетом внешнего вида (морфологии) эмбрионов. Использование же предымплантационного генетического тестирования повышает успешность имплантации почти полтора раза по сравнению с визуальной оценкой.
Перед проведением любого вида предымплантационного генетического тестирования семейная пара должна быть ознакомлена с плюсами и минусами и этой процедуры, и самого ЭКО.
Конечно же, идеальным было бы тестирование, которое позволяло определить не только количество и вид хромосом, изменения в единичных генах, но и весь генетический профиль будущего ребенка (у человека имеется 20 000–25 000 генов, отвечающих за выработку белков, значение других участков ДНК пока не известно). Современные технологии, в том числе компьютерные, позволяют создавать карту генома человека (karyomapping), но этот процесс очень дорогостоящий, поэтому находится пока что на уровне эксперимента. Объемное тестирование требует и больше времени для получения результатов. Поэтому даже в репродуктивных клиниках ПГС и ПГД из-за дороговизны и нехватки времени проводят в сокращенном варианте (кариотип и/или генотирование для 10–12 распространенных заболеваний).
Тем не менее репродуктивную медицину уже невозможно представить без предымплантационного генетического тестирования, а быстрое совершенствование технологий позволяет заметно повышать качество и безопасность этой процедуры, давая возможность многим семейным парам иметь желаемое здоровое потомство.
Преимплантационный генетический анализ эмбрионов
Каждая из 100 триллионов клеток в организме человека (за исключением красных кровяных клеток) содержит весь человеческий геном. Хромосомы – это струноподобные элементы внутри ядра (в центре) каждой клетки вашего тела. Они содержат генетическую информацию, ДНК. Ген занимает определенное место на хромосоме. В норме, есть 23 идентичных пары хромосом (2 метра ДНК) в каждой клетке, в общей сложности 46 хромосом. Каждый партнер во время оплодотворения обычно предоставляет 23 хромосомы. Если яйцеклетка или сперматозоид имеют аномальную упаковку хромосом, эмбрион, который они создают, также будет иметь хромосомные аномалии. Иногда это связано с перестройкой хромосом, или недостатком части хромосомы. В некоторых случаях есть отсутствующие хромосомы, или дополнительная хромосома (анеуплоидии), ведущие к наследственным заболеваниям. Любой эмбрион, в котором отсутствует хромосома (моносомия) перестанет расти до имплантации (фатальная аномалия). Если анеуплоидии включают хромосомы 13, 18, 21, Х или Y, беременность может дойти до родов. Наиболее распространенной из этих несмертельных аномалий является трисомия 21, или синдром Дауна, при которой присутствует дополнительная 21-я хромосома. Другие включают синдром Тернера у женщин и синдром Клайнфельтера у мужчин.
История преимплантационной генетической диагностики (ПГД)
Первые живорождения после ПГД были зарегистрированы в Лондоне в 1989 году. Две двойни девочек-близнецов родились от пяти пар с риском передачи связанного с Х-хромосомой заболевания. В настоящее время с помощью методов генетического анализа или ПГД могут быть обнаружены около 90% аномальных эмбрионов. Не все хромосомные или генетические заболевания могут быть определены этими процедурами, так как в ходе одной процедуры может быть диагностировано только ограниченное число хромосом. Многочисленные исследования на животных и некоторые исследования на человеке показывают, что микрохирургия эмбриона (биопсия), необходимая для удаления клеток, не влияет на нормальное развитие ребенка. Эта процедура, однако, была выполнена относительно небольшому числу пациентов во всем мире, поэтому точные негативные последствия, если таковые имеются, неизвестны. Несмотря на то, что после генетического анализа для выявления анеуплоидии всем мире на сегодняшний день было рождено уже много детей, эта процедура все еще относительно нова. В исследованиях на животных не было обнаружено никаких очевидных проблем и предварительные данные с эмбрионами человека позволяют предположить справедливость этого вывода. В исследовании, проведенном в Университетском колледже Лондона, исследователи недавно рассмотрели 12 преимплантационных эмбрионов с новой техникой, которая сочетает в себе амплификацию всего генома (WGA) и сравнительную гибридизацию генома (CGH). В результате в 8 из 12 изученных эмбрионов были обнаружены значительные хромосомные аномалии. Это может объяснить, почему люди имеют в лучшем случае 25% шансов на достижение жизнеспособной беременности в месяц при естественном зачатии.
Как передаются по наследству генетические заболевания
В диаграммах ниже, D или d представляет дефектный ген, а N или n представляет нормальный ген. Мутации не всегда приводят к болезни.
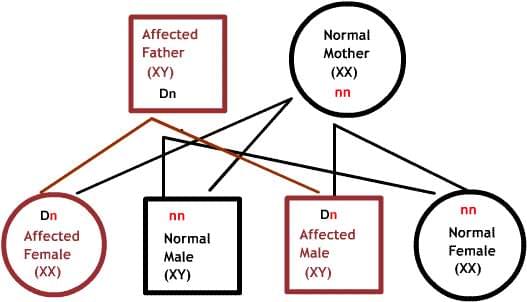
Доминантные заболевания:
Один из родителей имеет один дефектный ген, который доминирует над своей нормальной парой. Так как потомки наследуют половину своего генетического материала от каждого из родителей, есть 50% риск наследования дефектного гена, и, следовательно, заболевания.
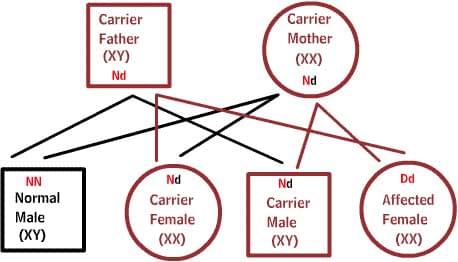
Рецессивные заболевания:
Оба родителя являются носителями одного дефектного гена, но при этом имеют нормальную пару гена. Для наследования заболевания необходимы две дефектных копии гена. Каждый потомок имеет 50% шанс быть носителем, и 25% шанс унаследовать заболевание.
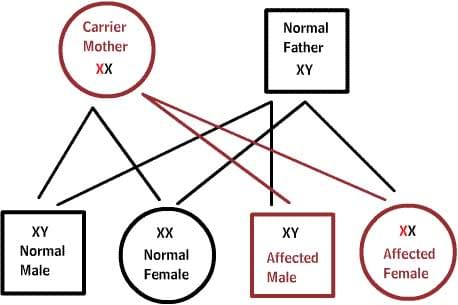
X-сцепленные заболевания:
Нормальные женщины имеют XX хромосомы, а нормальные мужчины XY. Женщины, которые имеют нормальный ген на одной из Х-хромосом, защищены от дефектного гена на их другой Х-хромосоме. Однако, у мужчины отсутствует такая защита в связи с наличием только одной Х-хромосомы. Каждый мужской потомок от матери, которая несет в себе дефект, имеет 50% шанс унаследовать дефектный ген и заболевание. Каждый женский потомок имеет 50% шанс быть носителем, как и ее мать. (на рисунке ниже X представляет нормальный ген а X представляет дефектный ген)
Возможные преимущества генетического анализа
Преимплантационная генетическая диагностика позволяет отобрать и перенести не измененные (хромосомно нормальные) эмбрионы, которые могут привести к большей частоте имплантации на эмбрион, сокращению потерь беременности и рождению большего числа здоровых детей. Генетическая диагностика предлагает парам альтернативу мучительному выбору по поводу того, чтобы прервать пострадавшую беременность после пренатальной диагностики, производимой путем амниоцентеза или биопсии ворсин хориона (CVS) на более поздних стадиях беременности. Почти все генетически связанные заболевания, которые могут быть диагностированы в перинатальном периоде либо амниоцентезом или CVS, могут быть обнаружены и ПГД. Процедура должна уменьшить психологическую травму для пар, которые несут повышенный риск генетических заболеваний для потомства.
Преимущества преимплантационной генетической диагностики (ПГД) могут включать в себя:
Возможные риски генетического анализа
Кандидаты для биопсии эмбриона и ПГД
Кандидаты для биопсии эмбриона и ПГД включают в себя:
Пары с повторными неудачами ЭКО.
Используемые методы
Для анализа на наличие генетических дефектов эмбриона, из него необходимо удалить либо первое полярное тельце из неоплодотворенной яйцеклетки и/или 1 или 2 клетки от каждого эмбриона. Это называется биопсией яйцеклетки или эмбриона и обычно делается перед тем, как происходит оплодотворение, или через 3 дня после оплодотворения. Биопсия на 6-10 клеточной стадии не оказывает отрицательного влияния на преимплантационное развитие. На этом этапе каждая клетка имеет полный набор хромосом. Обычно из эмбриона удаляется только одна клетка, так как ожидается, что будут одинаковыми со всеми другими клетками в эмбрионе. Иногда необходимо удалить вторую клетку из эмбриона, например, если сигнал в первой не обнаружен. Для диагноза предрасположенности с помощью первого и второго полярных телец, как показателей генетического статуса яйцеклетки, используется анализ методом FISH. Недостатком анализа полярных телец заключается в том, что он не принимает во внимание отцовские анеуплоидии.
Анализ биопсированной клетки использует один из двух методов:
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.
Медико-генетическое консультирование
Это возможность заранее подготовиться к возможным сложностям и своевременно принять меры, которые позволят родить здорового ребенка
Современной медицине известно свыше 6000 генетических патологий, частота их возникновения достигает 1.5-2%, и эта цифра продолжает расти. Подобные заболевания становятся причиной рождения детей с различными пороками и нарушениями в развитии, могут стать причиной внутриутробной смерти. К числу таких болезней относятся Синдром Эдвардса и Патау, синдром Дауна, ферментопатии, различные формы умственной отсталости, дефекты органов слуха, зрения, врожденные пороки развития и многое другое.
Чтобы снизить риски возникновения генетически-обусловленных нарушений у ребенка, существует программа медико-генетического консультирования.
Что такое медико-генетическое консультирование
Генетическое консультирование это обсуждение с врачом-генетиком риска наследственных заболеваний в семье. Одним из его видов является преконцепционный скрининг — специально разработанная программа медицинской помощи, ориентированная на предотвращение врожденных пороков развития и других генетических патологий у детей. Цель скрининга — уточнение риска в конкретной семье, в том числе выявление носительства мутаций, которые не проявляют себя у родителей, но опасны для потомства — повышают риск рождения ребенка с наследственной болезнью.
В рамках генетического консультирования специалисты выполняют действия, цель которых — количественная оценка рисков возникновения генетических патологий. На основе полученной информации удается разработать предупредительные меры для конкретной семьи, направленные на предотвращение наследственных заболеваний.
В этот комплекс входят:
Показания для консультации генетика
Наиболее актуальным временем для консультации генетика является этап планирования семьи. Но данные консультации также проводятся в рамках пренатальной диагностики, позволяя определять риски генетических аномалий у ребенка и предотвращать их.
Основными показаниями к консультированию являются:
Показания для получения консультирования
Генетическая консультация помогает уменьшить риски в процессе вынашивания плода. Также она дает возможность заранее подготовиться к возможным сложностям и своевременно принять меры, которые позволят родить здорового ребенка.
Как проводится консультация
На базе клиники GMS ЭКО проведение генетической консультации включает:
Консультацию членов семьи у врача-генетика с анализом родословной и оценкой необходимости генетических исследований. После этого выполняются дополнительные исследования, включающие анализы генов и хромосом.
Если выявлена генетическая патология, генная или хромосомная мутации, врач составляет прогноз. Определяется риск рождения детей с наследственным заболеванием или развития патологии у членов семьи.
Специалист описывает возможные способы снижения риска рождения больного ребенка и помогает семье совершить выбор.
5 вопросов по теме
Нужна ли консультация, если у меня нет генетических болезней?
Это разумная мера, ведь вы можете не подозревать, что являетесь носителем мутации.
Долго ли проводится консультирование?
Процесс занимает около 40 минут, после чего пациент получает подробные рекомендации врача-генетика.
Насколько достоверный этот метод?
Мы используем новейшее диагностическое оборудование и методики генетической диагностики, привлекаем лучших врачей, поэтому точность прогноза высока.
Актуальна ли консультация вне подготовки к беременности?
Да, ведь эта программа позволяет оценить риски развития наследственных заболеваний и у взрослого человека, особенно если в анамнезе семьи присутствуют такие патологии.
Можно ли проходить консультирование, если я уже беременна?
Можно и в этом есть смысл, ведь вы сможете получить информацию о здоровье ребенка, а также прогноз о его развитии, жизни, уровне генетического риска.
ПГТ (преимплантационное генетическое тестирование): преимущества, как проходит процедура
Онлайн-консультация
Когда я говорю об этом с пациентами, одна из первых реакций, которую я получаю, заключается в том, что они думают, что это связано со 100-процентной беременностью и идеально здоровым ребенком. Другой миф, который я слышу, заключается в том, что большинство думает, что им это не нужно, потому что у них в семье нет никого с хромосомными проблемами. Оба эти утверждения – мифы. ПГТ – это самое лучшее, что может предложить наука, чтобы дать нам максимальный шанс на здоровую беременность, но у него есть ограничения: он проверяет только хромосомы, а не генетические заболевания, врожденные дефекты или гены аутизма. Большинство моих пациентов, узнав больше об этом, считают целесообразным проведение генетического тестирования перед имплантацией.
Прежде всего. Вы должны знать, что, если у вас есть бластоциста (5-6-дневный эмбрион с сотнями клеток), красивая внешне, это не значит, что она обладает генетической целостностью для здоровой беременности. Было бы хорошо, если бы эмбрионы были точно такими же, как бриллианты, но это не так. Бластоцисты могут быть оценены как бриллианты, но один только внешний вид не говорит о том, что хромосомы в норме. Вы не можете определить это без проведения ПГТ. Если кто-то говорит вам, что ваш эмбрион в порядке внешне, это не обязательно означает, что он имплантируется и разовьется в нормальную беременность. Внешние характеристики не свидетельствуют о нормальных хромосомах. Если человеку тридцать пять лет, то в среднем он получит около пяти бластоцист, и вероятность того, что каждая из них будет иметь нормальные хромосомы (она же эуплоидная бластоциста), составляет 80%. Если вам сорок два года, то среднее количество бластоцист в каждом цикле – одна, а вероятность того, что она будет эуплоидной, составляет 10%.
Я хочу, чтобы вы знали эту информацию сейчас, чтобы у вас был правильный набор ожиданий относительно того, что может произойти в вашем цикле, и вы могли идти в него с широко открытыми глазами. Это не значит, что мы все должны забеременеть в двадцать пять лет, когда у нас самые здоровые яйцеклетки. Нет. Этого не произойдет. Но мы должны знать, как снижается наша фертильность с возрастом. Если вы пытаетесь забеременеть, выясните, какой у вас диагноз по бесплодию. Узнайте, каковы ваши шансы в вашем нынешнем возрасте, и определите, поможет ли вам ПГТ.
Содержание
Что такое ПГТ?
Раньше это называлось ПГС (исследование количества хромосом у эмбрионов, проводящееся при ЭКО перед переносом эмбрионов в матку).
Как проводится преимплантационное генетическое тестирование?
Через три дня после извлечения яйцеклетки мы проводим так называемый вспомогательный хетчинг, чтобы подготовить эмбрионы к биопсии. У меня есть пациенты, которые сомневаются в том, что эмбрионы вылупляются с помощью вспомогательного хетчинга. Я сравниваю это с удалением аппендикса. Это может произойти только через операцию. Точно так же мы можем провести генетический анализ эмбриона, только если сначала вылупим его, а затем с помощью лазера проведем биопсию. При этом вы удаляете несколько клеток из оболочки эмбриона и отправляете их в лабораторию, занимающуюся генетическим тестированием. После биопсии эмбрионы замораживаются, и составляется отчет (так называемый отчет о заморозке), в котором описывается качество каждого эмбриона. Результаты вы получаете от лаборатории, проводящей генетическое тестирование, обычно через неделю.
Кто и когда должен рассматривать возможность получения ПГТ?
Каждый должен рассмотреть этот вопрос. Я хочу, чтобы пациенты были полностью информированы о своих возможностях. Я сажусь со своими пациентами и рассказываю им обо всех способах проведения ЭКО. Я хочу, чтобы они знали о своих возможностях. Есть причины, по которым проведение ПГТ может дать вам больше шансов на беременность. Тем не менее, не все должны это делать. Если ваш эмбрион низкого качества, но достаточно сильный, чтобы наступила здоровая беременность, я прошу своих пациентов пересмотреть вопрос о потенциальном стрессе эмбриона. Не все должны это делать. Если вы не хотите этого делать, тоже ничего страшного.
Но есть моменты, когда стоит подумать об этом точно:
Существуют ли какие-либо риски при проведении ПГТ?
Да! Я только что упомянула об этом выше. Мы хотим быть уверены, что тестирование эмбрионов не повредит им.
Каковы преимущества ПГТ?
Почему я должен рассмотреть возможность проведения ПГТ?
Вот возможные причины, которые я советую вам обсудить с вашим врачом:
Мои советы профессионала:
В заключение
Это все, что я хотела бы знать, если бы была пациентом, рассматривающим возможность проведения ПГТ. Спасибо, что прочитали это. Я надеюсь, что все, что вы делаете, работая над достижением своей цели, будет успешным. Я посылаю вам всю свою положительную энергию.