гипохромия выраженная что это значит у женщин
Гипохромия выраженная что это значит у женщин
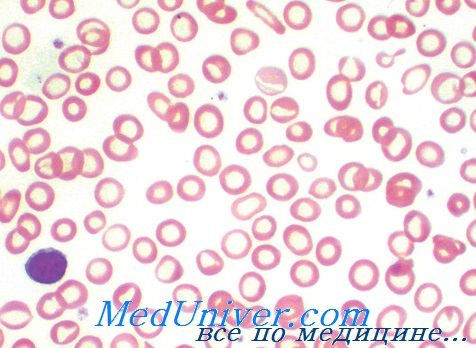
К этой большой группе относятся те анемии, общей чертой которых является понимание концентрации гемоглобина в эритроцитах (до менее 34%). В принципе это нарушение сочетается с одновременным сокращением объема эритроцитов, что, морфологически, выражается микроцитозом. Следовательно, состояние эритроцитной гипохромии представляется в виде морфологической почвы развития количественно неполноценного синтезирования (сокращения) гемоглобина, составляющего основное нарушение в патогенезе гипохромной анемии.
Вместе с тем известно, что синтез гемоглобина в зритробластах предполагает одновременное образование гема (в митохондриях) и глобина (в цитоплазме). При этом синтез гема требует синтезирование протопорфирина и связывание последнего с железом. Представляется ясным, что нарушение синтезирования гемоглобина может развиться в результате расстройства синтеза протопорфирина, глобина или метаболизма железа.
Наиболее часто встречаются те гипохромные анемии, в которых происходит нарушение метаболизма железа за счет его недостатка, например при железодефицитной анемии. Реже наблюдаются гипохромные анемии, при которых железо не используется в процессе кроветворения по причине его блокирования макрофагами (анемии, развивающиеся при хронических воспалениях) или отсутствия трансферина, в связи с каким либо генетическим дефектом — например при атрансферинемии.
Нарушение синтеза протопорфирина в связи с блокированием ферментов на различных ступенях (врожденном или приобретенном) также способствует развитию гипохромной анемии, причем нередко смешанного морфологического характера (гипохромные эритроциты, сосуществующие с нормальной популяцией). Однако при этом всегда наблюдается ненормальное отложение железа в митохондриях, в виде мицелиев, способствующее образованию патологических сидеробластов, называемых кольчатыми. Вот почему эта группа анемий получила название «сидеробластических анемий».
И наконец, наиболее частое нарушение синтезирования глобина наблюдается при талассемических заболеваниях, когда замедляются темпы синтеза одной из полипептидных цепей глобина (альфа или бета).
При иных гемоглобинопатиях, таких как гемоглобин К или гемоглобин Е отмечается эритроцитная гипохромия (см. главу гемоглобинопатии).
Ниже приведена патогенетическая классификация гипохромных анемий.
Классификация гипохромных анемий
II. Нарушение в процессе синтезирования протопорфирина:
1) Врожденная сидеробластическая анемия (недостаточность S-аминолевулинсинтетазы и копропорфириногеноксидазы)
2) Приобретенная генуинная сидеробластическая анемия (недостаток геминсинтетазы)
3) Вторичная сидеробластическая анемия (отравление свинцом, обусловленное ГИНК, ревматоидным артритом, новообразованием и пр.).
Б. Нарушение синтеза глобина:
1) Талассемические болезни
2) Гемоглобин К, гемоглобин Е, гемоглобин «Lepore», гемоглобин «Constant Spring».
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Лечение анемии
Железодефицитная анемия ЖДА — это гипохромная микроцитарная анемия, развивающаяся в результате абсолютного дефицита железа в организме.
Помимо анемического синдрома, для нее характерно нарушение функции кожи, ее придатков и слизистых оболочек — сидеропенический синдром.
ЖДА — это последняя стадия дефицита железа; до появления анемии часто при подробном расспросе и осмотре пациента можно обнаружить проявления сидеропении, что позволит своевременно выявить причину дефицита железа и предотвратить развитие ЖДА.
Эпидемиология
Впервые ЖДА описал немецкий врач Й. Ланге в 1554 г., а препараты для ее лечения впервые применил Т. Сиденгам в XVII в. Анемии, развивающиеся в результате дефицита железа в организме, наиболее широко распространены в клинической практике. По данным ВОЗ, около 2,5 млрд человек на Земле имеют скрытый дефицит железа и 1 млрд человек страдает ЖДА.
Достоверно доказано влияние ЖДА на увеличение частоты материнской и детской смертности. ЖДА встречаются у 12–13 % детей в возрасте от 6 мес. до 2 лет. В развивающихся странах этот показатель значительно выше: в Индии и странах Африки он достигает 72–76 %. В развитых странах Европы и Северной Америки ЖДА выявляется у 7,5–11 % всех женщин детородного возраста, а у 20–25 % наблюдается скрытый тканевой дефицит железа. Значительно большая частота ЖДА в странах Азии, Африки и Латинской Америки, где она достигает эпидемических величин и составляет 45–60 %. Из всех анемий, встречающихся в клинической практике, около 80 % являются железодефицитными. В Российской Федерации сведений по частоте ЖДА нет, однако, по нашим данным, в Москве ее частота составляет 30–35 % среди женщин детородного возраста, а скрытого дефицита железа — до 60 %.
Развитие анемии
Со временем дефицит железа прогрессирует, течет долгие годы латентно, а затем, после полного истощения запасов железа в депо, развивается ЖДА. Основной механизм развития анемии — нарушение гемоглобинообразования в эритрокариоцитах костного мозга. В основе патологии эритропоэза при дефиците железа лежит нарушение синтеза гема, в результате которого гемоглобинизация эритронормобластов запаздывает по сравнению с процессом обратного развития ядерных структур. Поскольку синтез гемоглобина из-за дефицита железа страдает в большей степени, чем образование эритроцитов, для ЖДА при сравнительно умеренном снижении числа эритроцитов свойственно более выраженное падение содержания в них гемоглобина, что проявляется гипохромией эритроцитов и развитием гипохромной микроцитарной анемии.
Второй патологический механизм, который имеет место в условиях дефицита железа, — это снижение образования других важнейших белков, участвующих в накоплении и транспорте кислорода. Уменьшается содержание миоглобина в поперечнополосатой мускулатуре. Нарушение образования цитохромов и каталаз приводит к угнетению энергетического обмена всех клеток организма, при этом в основном страдают быстро делящиеся ткани (кожа и слизистые оболочки).
В зависимости от причин, вызывающих дефицит железа, выделяется пять групп ЖДА:
1) хронические постгеморрагические ЖДА;
2) ЖДА, связанные с нарушением всасывания и поступления железа с пищей;
3) ЖДА, связанные с недостаточным исходным уровнем железа в организме (чаще у детей);
4) ЖДА, обусловленные повышением потребности организма в железе (без кровопотери);
5) ЖДА, связанные с нарушением транспорта железа.
Стадии дефицита железа
В настоящее время выделяют несколько стадий дефицита железа:
1. Предрасположенность к развитию железодефицита (вегетарианство, подростковый возраст в сочетании с нарушением менструального цикла у девочек, частые роды, наличие хронических заболеваний ЖКТ или женской репродуктивной системы, связанных с кровопотерей).
2. Предлатентный дефицит железа. На этой стадии нет никаких лабораторных критериев дефицита железа, однако можно определить повышение абсорбции 59Fe3+ в ЖКТ, которое может превышать 50 % (в норме 10–15 %).
3. Латентный дефицит железа. Характеризуется развитием сидеропенического синдрома, снижением запасов железа в организме по данным лабораторных исследований.
Лечение анемии
Лечение ЖДА строится на следующих принципах. До начала лечения обязательно следует выявить и по возможности устранить причину развития ЖДА
Для лечения надо использовать только лекарственные железосодержащие препараты. Вне зависимости от тяжести анемии лечение начинается с пероральных препаратов, исключая противопоказания (острая язва желудка и двенадцатиперстной кишки, эрозивный гастрит), невозможность использования пероральных препаратов (нарушение глотания, отсутствие сознания, интубация и др.).
Лечебная доза пероральных препаратов железа составляет 100– 200 мг элементарного железа в сутки (максимально 300 мг), разделенная на 2 приема. Использование парентеральных средств возможно только при доказанном абсолютном дефиците железа, лечение должно проводиться только в стационаре, вводится только расчетная доза препарата. Внутримышечное введение препаратов железа в настоящее время не применяется. Трансфузии эритроцитарной массы обычно не используются. Они показаны только пожилым людям при наличии тяжелой анемии.
Сроки лечения при использовании пероральных препаратов железа зависят от тяжести анемии, составляют 3–4 мес. при использовании препаратов Fe2+ или 4–6 мес. при использовании препаратов Fe3+.
Анемия (малокровие)
Содержание статьи:
Анемия (малокровие) – патология, для которой свойственно снижение уровня гемоглобина в крови, количества эритроцитов (красных кровяных телец), изменение их формы. Пониженный гемоглобин – обязательный признак анемии, изменение числа эритроцитов и их деформация присутствуют не всегда.
Анемия – распространенное заболевание. Ему подвержены более четверти всего населения мира – 27,9 % или 1,9 млрд человек. Ежегодный темп прироста анемий составляет 6,6 %. Чаще всего патология встречается у детей дошкольного возраста (47,4 % от всех случаев), женщин, особенно во время беременности, реже – у мужчин (12,7 %). В России анемия ежегодно диагностируется у более чем 1,5 млн пациентов.
Причины возникновения патологии
Железодефицитная анемия (ЖДА), самая частая форма малокровия, обусловлена тремя факторами: недостаток поступления железа, его усиленная потеря, высокая потребность в этом микроэлементе, не восполняемая в достаточной мере.
Одна из причин недостатка поступления железа – неполноценное питание (недоедание, однообразное меню с малым количеством белка и красного мяса, вегетарианство, искусственное вскармливание). Кроме того, поступлению необходимого объема микроэлемента препятствует нарушение его усвояемости. Это происходит из-за различных патологий, мешающих ионизации железа в желудке (гастрит с атрофией слизистой, резекция желудка, гипо- и авитаминоз витамина C), и затрудняющих его всасывание в кишечнике (дуоденит, энтерит, колит).
Потерю железа сверх нормы провоцируют кровотечения – из носа, десен, желудочно-кишечные, геморроидальные, маточные, почечные, геморрагические диатезы, частое донорство.
Гиперпотребность в железе вызывают физиологические и патологические состояния. К физиологическим относятся интенсивный рост и половое созревание, беременность и кормление грудью, профессиональные тренировки, тяжелые физические нагрузки. К патологическим – глистные инвазии.
Дефицит железа бывает связан с некоторыми инфекционными болезнями, также нехватка этого элемента фиксируется у детей, рожденных матерями с анемией.
Группы риска
Исходя из причин, можно выделить категории людей, подверженных развитию малокровия:
Патогенез болезни
Ведущее звено патогенеза ЖДА – нарушение синтеза гемоглобина вследствие снижения запасов железа, которое крайне необходимо для нормальной жизнедеятельности организма. Железо присутствует в составе гемоглобина и миоглобина, отвечает за транспортировку кислорода, различные биохимические процессы.
Железо всасывается в кровь из желудочно-кишечного тракта (ЖКТ), соединяется с трансферрином и либо накапливается в печени в составе белка ферритина, либо направляется в красный костный мозг, где с его участием идет синтез гемоглобина. Некоторая часть микроэлемента в составе трансферрина принимает участие в окислительно-восстановительных реакциях в тканях.
Симптомы анемии
Общие признаки:
Зачастую начальные симптомы заболевания при легкой стадии анемии пациенты списывают на усталость, недосып, тяжелый рабочий график. Человека должны насторожить такие признаки как слабость при незначительной нагрузке, чувство разбитости, сонливость даже после полноценного ночного сна. В этом случае следует сдать общий анализ крови, чтобы не пропустить начало заболевания.
При острых и тяжелых анемиях возможно резкое ухудшение самочувствия – тошнота, рвота, обмороки, вплоть до гипоксической комы.
Классификация
Разновидности анемии в зависимости от причины:
По качественным и количественным показателям:
В этой классификации применяется величина цветового показателя крови (ЦП), норма которого равна 0,86-1,1. При нормохромной анемии ЦП остается в допустимых пределах, при гипохромной – опускается ниже 0,86, при гиперхромной – поднимается выше 1,1.
По течению (для геморрагических анемий):
Стадии анемии
ЖДА развивается, последовательно проходя три этапа:
Для ЖДА выделяют три степени тяжести, каждой из которых соответствует определенный уровень гемоглобина. В норме показатель составляет от 110 до 130 г/л, нижняя граница допустима для детей и беременных женщин, верхняя – для мужчин.
| Степень тяжести | Уровень гемоглобина (г/л) |
|---|---|
| Легкая | 100-129 |
| Средняя | 70-109 |
| Тяжелая | менее 70-80 |
Диагностические мероприятия
Основа диагностики анемии – общий (ОАК) и биохимический анализ крови.
По биохимическому анализу оцениваются уровень сывороточного железа и ферритина, увеличение общей железосвязывающей способности сыворотки, коэффициент насыщения трансферрина железом.
Лечение анемии
Важный этап в лечении – устранение факторов, вызывающих недостаток железа. Одновременно больному назначается терапия для нормализации уровня этого микроэлемента. Диета – важная составляющая процесса лечения, но она является вспомогательным элементом, вылечить анемию без применения лекарств невозможно.
В основе лечения – препараты железа. Предпочтение отдается пероральному приему лекарств, инъекционно они вводятся только при тяжелом течении анемии, необходимости быстрого восстановления уровня железа, непереносимости или неэффективности пероральных препаратов, заболеваниях органов пищеварения, препятствующих всасыванию лекарственных средств.
Помимо препаратов железа рекомендованы витамины (B12, C), фолиевая кислота.
Для лечения отдельных видов анемий применяются специальные методы. При постгеморрагической анемии требуется восполнение объема циркулирующей крови, в том числе с помощью гемотрансфузий. При апластической анемии показаны гемотрансфузии, гормональная терапия и другие мероприятия, вплоть до трансплантации костного мозга.
Лечение железодефицитной анемии продолжается от 3 до 6 месяцев. Его нельзя прекращать сразу после восстановления уровня гемоглобина, в организме должен сформироваться запас железа.
Осложнения болезни
Последствия анемии возникают при ее долгом течении и отсутствии терапии. Дефицит железа в организме вызывает ослабление иммунитета, уменьшается сопротивляемость простудным, вирусным, бактериальным заболеваниям. Возможны осложнения со стороны нервной системы, нарушения функций печени, сбои менструального цикла. Из-за постоянной гипоксии возникают нарушения функций сердечно-сосудистой системы – дистрофия миокарда, застойные явления, развивается сердечно-сосудистая недостаточность. Наиболее тяжелым осложнением анемии является гипоксическая кома.
Прогноз и профилактика анемии
При своевременной диагностике и адекватной терапии прогноз благоприятный. Как правило заболевание лечится амбулаторно, госпитализация пациента не требуется.
Для профилактики ЖДА необходимо полноценное питание с достаточным поступлением белка, ежегодная сдача общего анализа крови, контроль за состоянием здоровья в целом и устранение заболеваний, которые могут стать источником пусть даже небольшой хронической кровопотери. Люди из групп риска по назначению врача могут ежегодно принимать курс препаратов железа, однако делать это самостоятельно недопустимо, так как бесконтрольный прием этих лекарств может вызвать тяжелые побочные эффекты.
Источники:
| Прием (осмотр, консультация) врача-гематолога первичный, лечебно-диагностический, амбулаторный |
* Ознакомиться подробнее с условиями можно здесь — Лечение в кредит или рассрочку.
Гипохромная анемия как фоновая патология у инфекционных больных
Полное название:
Гипохромная анемия как фоновая патология у инфекционных больных: частота выявления при госпитализации в различных возрастных группах, сопряженность с нозологией, анализ обследования и объем терапии, клинические наблюдения
Вопросы оценки состояния догоспитальной и ранней госпитальной диагностики инфекционных болезней важны для характеристики качества лечебной помощи при различной патологии. Качество выявления фоновой патологии, начиная с приемного отделения, зависит не только от квалификации врача, но и от полноты получения информации из документации участковой сети (карта амбулаторного больного, переводной эпикриз, направление на госпитализацию). Фоновая патология накладывает отпечаток на особенности течения тех или иных инфекционных заболеваний, затрудняя диагностику, замедляя процесс выздоровления и, тем самым, приводит к увеличению экономических затрат, связанных со стационарным лечением и последующими реабилитационными мероприятиями.
Известно, что в Европе гипохромной анемией (ГА) страдают 7,3-11% женщин и не менее 3-6% мужчин. При этом скрытый дефицит железа у женщин на территории Европы доходит до 25%, а в странах СНГ — до 13,5%. По некоторым данным, дефицит железа среди населения в мире встречается в 10-20%. В то же время, среди женщин детородного возраста и детей дефицит железа в некоторых регионах достигает даже 40-50%.
Цель исследования: оценка распространенности гипохромной анемии среди больных, госпитализированных в инфекционный стационар, с учетом возраста, нозологии, пола, характера и объема корригирующей терапии. При постановке диагноза гипохромной анемии использованы критерии Всемирной организации здравоохранения: анемия регистрируется у мужчин при уровне гемоглобина (Hb) менее 130 г/л, гематокрита — 39%; у женщин, соответственно, 120 г/л и 36%, при этом у беременных менее 110 г/л. Анализу подвергнуты материалы больных, госпитализированных в 2007 году. Фоновой считали гипохромную анемию, выявленную при поступлении. Данные сравнительного анализа были сгруппированы соответственно поставленным задачам, обработаны статистически в относительных показателях. За анализируемый период было госпитализировано 5153 больных, среди которых гипохромная анемия была выявлена у 1562 (30,31%) больных, из которых женщины составили 50,5 ± 1,26%, мужчины 49,5 ± 1,26%.
В табл. 1 представлен сопоставительный анализ возрастной структуры населения региона, всех госпитализированных инфекционных больных, больных с выявленной гипохромной анемией и показатель относительной частоты гипохромной анемии в отдельных возрастных группах.
Как видно из табл. 1, наиболее часто госпитализировались больные от 0 до 9 лет (более чем в 4 раза в сравнении с показателями в популяции населения области). Аналогичные данные по частоте отмечены среди всех лиц с гипохромной анемией. В сравнении с госпитализированными больными в возрасте старше 30 лет произошло постепенное возрастание частоты лиц с гипохромной анемией по мере увеличения возраста, что подтверждено показателями относительной частоты гипохромной анемии среди всех поступивших в каждой возрастной группе. Если в группе детей до 9 лет практически каждый 4 ребенок был с гипохромной анемией, то в группе от 10 до 14 и от 15 до 18 лет частота гипохромной анемии уменьшилась, а с 19-25 лет начиналось постепенное возрастание частоты гипохромной анемии, достигая настораживающего уровня после 31 года. Практически каждый 2-й больной пенсионного возраста имел гипохромную анемию, а у лиц старше 70 лет гипохромная анемия сопутствовала основному диагнозу в 100% случаев. При углубленном анализе выявлено, что если у госпитализированных взрослых больных старше 18 лет гипохромная анемия выявлена в 35,48 ± 0,95% (889 из 2505), то у детей (от 0 до 18 лет включительно) — в 25,41 ± 0,84% (673 из 2648), что статистически высоко достоверно (р
Предполагаемыми причинами гипохромной анемии в детском возрасте были распространенность искусственного вскармливания и роды кесаревым сечением, что подтверждено анализом историй болезни. Снижение частоты гипохромной анемии в возрасте от 10 до 18 лет объясняется сбалансированным питанием, активизацией анаболических процессов в организме в период полового созревания. Нарастание частоты гипохромной анемии в последующем можно объяснить нерациональностью питания, его несбалансированностью по составу, интоксикациями различного генеза, включая алкоголь, на фоне увеличения сопутствующей патологии желудочно-кишечного тракта. На закономерное увеличение частоты хронической патологии, начиная с 25-летнего возраста, указывают многие исследователи.
Резкое нарастание гипохромной анемии у лиц преклонного возраста, особенно старше 70 лет, следует объяснить свойственными этому возрасту пищевыми ограничениями (болезни, социальная обеспеченность) и возрастными особенностями в целом (истощение функции костного мозга). В целом в генезе гипохромной анемии не исключается и реализация возможных последствий инкорпорации радиоактивного стронция, особенно у лиц старше 25 лет, подвергнутых этому воздействию в ранний период после аварии на ЧАЭС.
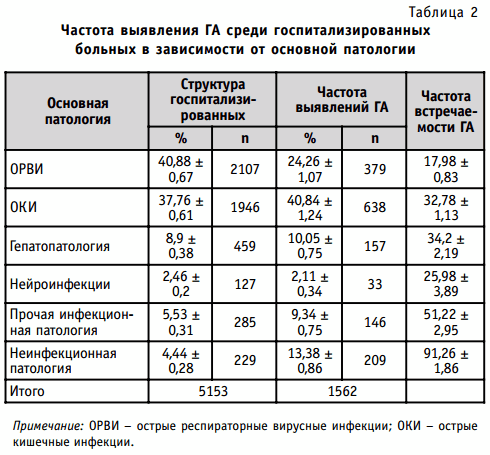
Нами проанализирована частота выявления анемии среди госпитализированных с учетом имевшейся основной патологии (табл. 2).
Как видно из табл. 2, наиболее распространенными среди госпитализированных были ОРВИ, затем группа ОКИ, которая составляла в целом более 3/4 всех больных. Тем не менее, на этот контингент выпало только 2/3 всех случаев выявленной гипохромной анемии. Если изначальная (фоновая) гипохромная анемия у больных с ОРВИ выявлена только у каждого 6-го пациента, то у больных с ОКИ она обнаруживается у каждого третьего.
Аналогичная ситуация отмечена у больных с гепатопатологией. Довольно часто фоновая гипохромная анемия выявлялась у больных с нейроинфекциями (каждый 4-й). Важно подчеркнуть, что среди всех больных сводной группы прочих инфекций гипохромная анемия выявлена у половины пациентов, а при неинфекционной патологии — у 90%. Последнюю группу составили в основном больные старше 65 лет (более 80%). Естественно, что все отмеченное подтверждало крайнюю необходимость уточнения всего комплекса причин, приводящих к гипохромной анемии. Высокие показатели фоновой гипохромной анемии среди группы прочих инфекций (сепсис, генерализованная герпетическая инфекция, ВИЧ-инфекция и т. п.) отражали воздействие патологического процесса на организм больного в догоспитальном периоде и по сути были следствием общеинтоксикационных явлений. Хотелось бы подчеркнуть, что если в популяции жителей региона достоверно преобладали женщины (женщины 53,09 ± 0,015% и мужчины 46,91 ± 0,015; p 12 /л; Hb — 83 г/л; Ht — 0,25; Тр. — 158,4 × 10 9 /л; L — 27,4 × 10 9 /л с формулой: эозинофилы — 3%, миелоциты — 1%, юные — 5%, палочкоядерные нейтрофилы — 30%, сегментоядерные нейтрофилы — 11%, лимфоциты — 48, моноциты — 2%. СОЭ — 50 мм/час. Анизоцитоз (++), нормобласты — 1:100. Перелита эритромасса 10.10.2007 г. в объеме 40 мл А(II)-Rh+. Лечение, адекватное основному заболеванию и тяжести состояния (цефтриаксон, альбумин, коррекция водно-солевого обмена). Анализ крови при выписке от 16.10.2007 г.: Эр. — 4,01 × 10 12 /л; Hb — 133 г/л; L — 4,8 × 10 9 /л с формулой: эозинофилы — 2%, сегментоядерные — 15%, лимфоциты — 82%, моноциты 1%. СОЭ — 8 мм/час. Состояние удовлетворительное. Выписана под наблюдение участкового педиатра.
Случай 2. Ребенок Л., 11 месяцев (И. б. 1013/2007), поступила из ЦРБ с диагнозом: ротавирусная инфекция, среднетяжелая форма: острый бронхит; анемия смешанной этиологии, тяжелая форма. Родоразрешение кесаревым сечением. Анализ крови при поступлении от 8.03.2007 г.: Эр. — 2,1 × 10 12 /л; Hb — 71 г/л; Ht — 0,21; Тр. — 260,2 × 10 9 /л; L — 11,9 × 10 9 /л с формулой: эозинофилы — 1%, палочкоядерные нейтрофилы — 9%, сегментоядерные нейтрофилы — 35%, лимфоциты — 51%, моноциты — 3%, плазматические клетки — 1%. СОЭ — 19 мм/час, анизоцитоз и пойкилоцитоз (++). Перелита эритромасса 8.03.07 г. в объеме 90 мл А(II)-Rh+. Лечение: цефтриаксон, альбумин, витаминотерапия, коррекция водно-солевого обмена. Анализ крови при выписке 16.03.2007 г.: Эр. 3,68 × 10 12 /л; Hb — 122 г/л; L — 7,15 × 10 9 /л с формулой: эозинофилы — 1%, палочкоядерные нейтрофилы — 1%, сегментоядерные нейтрофилы — 28%, лимфоциты — 68%, моноциты — 5%. СОЭ — 5 мм/час. Переведена по месту жительства.
Случай 3. Ребенок К., 6 месяцев (И. б. 2102/2007), поступил из района с диагнозом: врожденные пороки развития; острая внебольничная двухсторонняя очаговая пневмония с обструктивным синдромом; ДП II-III ст.; синдром дезадаптации сердечно-сосудистой системы; двухсторонний гнойный отит, гнойный конъюнктивит; тубулоинтерстициальный нефрит; анемия средней степени тяжести. Анализ крови при поступлении от 21.05.2007 г.: Эр. — 2,45 × 10 12 /л; Hb — 83 г/л; Тр. — 162 × 10 9 /л; L — 6,6 × 10 9 /л с формулой: базофилы — 1%, эозинофилы — 1%, палочкоядерные нейтрофилы — 9%, сегментоядерные нейтрофилы — 26%, лимфоциты — 60%, моноциты — 3%. СОЭ — 19 мм/час. Анизоцитоз и пойкилоцитоз (+). Перелита эритромасса 22.05.07 г. в объеме 60 мл 0(I)-Rh+. Лечение проводилось меропенемом, преднизолоном (2 дня), сальбутамолом и др. Анализ крови при выписке 28.05.2007 г.: Эр. 3,78 × 10 12 /л; Hb — 118 г/л; Тр. 279,4 × 10 9 /л, L — 12,2 × 10 9 /л; с формулой: палочкоядерные нейтрофилы — 2%, сегментоядерные нейтрофилы — 28%, лимфоциты — 69%, моноциты — 1%. СОЭ — 13 мм/час. Переведен для подготовки к коррекции врожденных пороков в детскую больницу в среднетяжелом состоянии из-за основной патологии.
Случай 4. Ребенок Р., 6 месяцев (И. б. 5034/2007), поступил из ЦРБ с диагнозом: аденовирусная инфекция (ринофаринго-конъюнктивальная лихорадка); двухсторонняя очаговая пневмония; ДН I ст.; нейротоксикоз; гипокалиемия; анемия средней степени тяжести смешанной этиологии. Анализ крови при поступлении от 18.12.2007 г.: Эр. — 2,84 × 10 12 /л; Hb — 70,8 г/л; Ht — 0,21; Тр. — 144,8 × 10 9 /л; L — 16,7 × 10 9 /л с формулой: эозинофилы — 1%, палочкоядерные нейтрофилы — 9%, сегментоядерные нейтрофилы — 37%, лимфоциты — 50%, моноциты — 3%. СОЭ — 25 мм/час. Анизоцитоз и пойкилоцитоз (++). Перелита эритромасса 20.12.07 г. в объеме 50 мл А(II)-Rh−. В лечении использовали нетрамицин, цефтриаксон, коррекция водно-солевого обмена. При выписке анализ крови 28.12.2007 г.: Эр. 3,7 × 10 12 /л; Hb — 120,4 г/л; L — 10,8 × 10 9 /л с формулой: эозинофилы — 5%, палочкоядерные нейтрофилы — 2%, сегментоядерные нейтрофилы — 34%, лимфоциты — 58%, моноциты — 1%. СОЭ — 15 мм/час. Выписан по месту жительства.
Случай 5. Больная К., 46 лет (И. б. 3758/2007), поступила в клинику 20.09.07 г. Клинический диагноз: острый гастроэнтероколит неинфекционный (алиментарно-токсический); хронический гепатит алкогольного генеза; хронический панкреатит; анемия смешанной этиологии средней тяжести; педикулез. Больная не работает, страдает хроническим алкоголизмом. Анализ крови при поступлении от 20.09.2007 г.: Эр. 2,36 × 10 12 /л; Hb — 83 г/л; Ht — 0,27; Тр. — 174,6 × 10 9 /л; L — 8,9 × 10 9 /л с формулой: палочкоядерные нейтрофилы — 3%, сегментоядерные нейтрофилы — 86%, лимфоциты — 11%. СОЭ — 12 мм/час. Перелита эритромасса 21.09.2007 в объеме 350 мл О(I)-Rh+. При выписке анализ крови: Эр. — 2,94 × 10 12 /л; Hb — 104 г/л; Тр. — 211,9 × 10 9 /л; L — 3,25 × 10 9 /л с формулой: сегментоядерные нейтрофилы — 22%, лимфоциты — 73%, моноциты — 5%. СОЭ — 15 мм/час. Выписана по месту жительства.
Случай 6. Больной П., 54 лет (И. б. 3634/2007), поступил в клинику 11.09.2007 г. Клинический диагноз: цирроз печени смешанной этиологии (алкоголь + обменный) в стадии декомпенсации; печеночно-клеточная недостаточность, спленомегалия; состояние после кровотечения из варикозных вен пищевода; сахарный диабет. Инвалид II группы. Анализ крови при поступлении от 11.09.2007 г.: Эр. — 2,52 × 10 12 /л; Hb — 89 г/л; Тр. — 120 × 10 9 /л; L — 3,6 × 10 9 /л с формулой: палочкоядерные нейтрофилы — 1%, сегментоядерные нейтрофилы — 50%, лимфоциты — 45%, моноциты — 4%. СОЭ — 60 мм/час. Анизоцитоз (++). Перелита эритромасса 12.09.2007 г. в объеме 300 мл В(III)-Rh+. В связи с основным заболеванием переведен для хирургического лечения в специализированный стационар. При переводе анализ крови от 27.09.2007 г.: Эр. — 3,71 × 10 12 /л; Hb — 118 г/л; Тр. — 129,5 × 10 9 /л; L — 3,35 × 10 9 /л с формулой: сегментоядерные нейтрофилы — 38%, лимфоциты — 60%, моноциты — 2%. СОЭ — 56 мм/час.
Случай 7. Больная М., 37 лет (И. б. 2716/2007), поступила в клинику 7.08.2007 г. Клинический диагноз: сепсис, тяжелая форма; гнойный менингоэнцефалит, двухсторонняя пневмония, левосторонний экссудативный плеврит, гидроторокс, миокардиодистрофия, пиелонефрит, пролежни, плегия правой руки, нижняя параплегия, варикоз нижних конечностей, фибромиоматоз матки. Сельская жительница, доярка. Анализ крови при поступлении от 7.08.2007 г.: Эр. — 2,94 × 10 12 /л; Hb — 100 г/л; Тр. — 170,5 × 10 9 /л; L — 6,7 × 10 9 /л с формулой: миелоциты — 1%, палочкоядерные нейтрофилы — 27%, сегментоядерные нейтрофилы — 53%, лимфоциты — 17%, моноциты — 2%; гипохромия, анизоцитоз (+++). СОЭ — 65 мм/час. Перелита эритромасса в объеме 200 мл О(I)-Rh+. На момент перевода в областную клиническую больницу в связи с наличием нервной патологии. Анализ крови от 2.09.2007 г.: Эр. — 3,89 × 10 12 /л; Hb — 96 г/л; L — 14,2 × 10 9 /л с формулой: палочкоядерные нейтрофилы — 2%, сегментоядерные нейтрофилы — 92%, лимфоциты — 5%, моноциты — 1%. СОЭ — 57 мм/час. Анизоцитоз и пойкилоцитоз (+).
Случай 8. Больной В., 47 лет (И. б. 3176/2007), поступил в клинику 22.08.2007 г. Клинический диагноз: очаговый туберкулез легких; алкоголизм; цирроз печени в стадии декомпенсации; портальная гипертензия; энцефалопатия смешанного генеза; полинейропатия смешанной этиологии; внегоспитальная правосторонняя нижнедолевая пневмония; обструктивный бронхит в стадии обострения; ДН II ст.; хронический панкреатит; хронический колит; кахексия; анемия средней степени тяжести смешанного генеза. Больной не работает, асоциален. Анализ крови при поступлении: Эр. — 2,21 × 10 12 /л; Hb — 73 г/л; L — 5,5 × 10 9 /л с формулой: палочкоядерные нейтрофилы — 9%, сегментоядерные нейтрофилы — 62%, эозинофилы — 3%, лимфоциты — 22%, моноциты — 4%. СОЭ — 37 мм/час. Анизоцитоз и пойкилоцитоз (+++). Перелита эритромасса дважды (530 и 560 мл) В(III)-Rh+. Наблюдался гематологом. Переведен в противотуберкулезный диспансер в связи с необходимостью проведения специфической терапии. При переводе 6.09.2007 г.: Эр. — 3,05 × 10 12 /л; Hb — 97 г/л; Нt — 0,25; Тр. — 167,8 × 10 9 /л; L — 5,1 × 10 9 /л с формулой: палочкоядерные нейтрофилы — 11%, сегментоядерные нейтрофилы — 72%, эозинофилы — 2%, базофилы — 1%, лимфоциты — 10%, моноциты — 4%. СОЭ — 34 мм/час. Токсическая зернистость нейтрофилов ++. Анизоцитоз и пойкилоцитоз (+).
Кроме переливания эритроцитарной массы больные (23 чел.) получали кратковременно препараты железа и заметно чаще — фолиевую кислоту (114 чел.). Эти назначения санкционировались лечащим врачом-инфекционистом, но не подвергались коррекции гематологом.
Анемия фонового характера зачастую развивается у больных задолго до поступления в стационар. Это делает обоснованным упрек в недостаточности внимания, уделяемого больным (особенно лицам пожилого и старческого возраста) со стороны участковой (поликлинической) сети. Несколько лучше картина в педиатрической службе, что можно объяснить преемственностью наблюдения от педиатра-неонатолога до участкового педиатра. Многое можно отнести и на счет внимания родителей к здоровью ребенка. Уточнению самих факторов, приводящих к анемизации детей и взрослых, уделяли внимание не столько интернисты, сколько экологи, гигиенисты, радиологи и т. п. Суммируя характеристику неблагоприятных факторов, приводящих к анемизации, можно согласиться, что этому способствует прежде всего вредное воздействие нарушений в экосреде, нерациональное питание, воздействие алкоголизации (у взрослых), накопление радионуклидов, что в целом приводит к снижению общей резистентности организма. Если учесть, что лица 65-70 лет в прошлом (1986 год) были в активном работоспособном возрасте, то влияние возможной инкорпорации радионуклидов после аварии на Чернобыльской АЭС было усугублено плохим питанием и в целом тяжелой экологической ситуацией в бывшем СССР, а также связано с употреблением продуктов питания с завышенным уровнем радиоактивности.
Полученные нами данные являются основой для дальнейшего углубленного анализа причин фоновой анемизации населения в целом и инфекционных больных в частности. Указанные факты должны стать объектом внимания гематологической службы, так как последняя в поликлиниках находится только в стадии формирования. Именно на уровне поликлиники эти специалисты должны заниматься «малой» гематологией. Если учесть, что нами проанализированы только случаи изначально зафиксированной гипохромной анемии с момента поступления в стационар и что это состояние имело место до болезни, то определить его длительность не представляется возможным. Установленный факт поэтапного нарастания анемизации с увеличением возраста отражает сохраняющуюся несбалансированность питания, обусловленную сложностями экономического положения населения и в настоящем. Определенный вклад вносит и нарастающая алкоголизация населения. Учитывая, что задачей здравоохранения является улучшение здоровья населения и преодоление проблем демографической ситуации, разработка мер по профилактике и лечению анемий должна стать наиболее важной для участковой сети настолько, насколько она сможет обеспечить нахождение больных с анемией под пристальным вниманием специалистов-гематологов.
Васильев В. С., Богуцкий М. И., Васильев А. В., Шейко М. И. Гродненский государственный медицинский университет.
Журнал «Медицинская панорама» № 1, январь 2009.