офс стандартные образцы гф 14
Офс стандартные образцы гф 14
Взамен ст. ГФ XI, вып.2
Настоящая общая фармакопейная статья определяет основные
требования и положения, предъявляемые к стандартным образцам (СО),
которые могут применяться для оценки качества лекарственных средств
(ЛС), включая биологические лекарственные средства (БЛС), и тем самым
являться неотъемлемой частью фармакопейной статьи (ФС) или
нормативной документации (НД).
Настоящая общая фармакопейная статья не распространяется на
стандартные образцы генотерапевтических лекарственных средств и
радиофармацевтических препаратов.
Цель использования СО в фармакопейном анализе – достижение
надлежащего уровня контроля качества субстанций для фармацевтического
применения и лекарственных препаратов. В рамках фармакопейной статьи
могут использоваться только фармакопейные стандартные образцы (ФСО).
СО не предназначены для использования в качестве лекарственных
ОСНОВНЫЕ ТЕРМИНЫ И ОПРЕДЕЛЕНИЯ
Стандартные образцы (СО)
— вещества, посредством сравнения с
которыми осуществляется контроль качества исследуемых лекарственных
средств с помощью физико-химических и биологических методов в целях
подтверждения соответствия лекарственных средств требованиям
нормативной
государственной регистрации, и которые применяются для калибровки
стандартных образцов производителя лекарственных средств, используемых
Аттестация фармацевтических стандартных образцов предприятия (СОП)
Содержание
Когда применяются СО предприятия?
Стандартные образцы используются при анализе большинства лекарственных средств
В качестве СО при анализе фарм. субстанций следует использовать фармакопейные стандартные образцы, аттестованные уполномоченным фармакопейным органом
ОФС.1.1.0006.15 “Фармацевтические субстанции”, ГФ XIV
На практике, т.к. отечественных фармакопейных СО пока нет, используются стандартные образцы европейской (EP) и американской (USP) фармакопей.
Для некоторых субстанций стандартных образцов, аттестованных уполномоченным фармакопейным органом, просто не существует. Например, если предприятие выпускает новую или редкую субстанцию.
В этом случае предприятия-производители разрабатывают и аттестуют собственные первичные СО, в форме стандартного образца предприятия (СОП):
При их [CО, аттестованных уполномоченным фармакопейным органом] отсутствии для идентификации и оценки содержания действующего вещества должны использоваться первичные стандартные образцы
ОФС.1.1.0006.15 “Фармацевтические субстанции”
В ГФ XIV вошла новая фармакопейная статья, посвященная разработке и аттестации стандартных образцов: ОФС.1.1.0007.18 «Стандартные образцы».
Подробно о стандартных образцах
первичные и вторичные СО, RM, CRM, ГСО, международные СО, СО предприятия, фармацевтические СО
Предприятия так же могут использовать вторичные СО предприятия в рутинном анализе, для снижения расхода дорогостоящих фармакопейных СО.
СО для качественного анализа
Назначение CО для качественного анализа
СО основного вещества применяются:
СО примесей применяются (ВЭЖХ):
Установление аттестованного значения для первичных СО
Для аттестации подлинности (структуры) первичного (primary) стандартного образца должны применяться первичные аналитические методы: спектроскопия ЯМР и масс-спектрометрия.
Масс-спектрометрия
Для анализа органических соединений применяют масс-спектрометры, работающие совместно с газовым или жидкостным хроматографом. Выбор между газовой и жидкостной хромато-масс-спектрометрией определяется свойствами соединения.
Нелетучие и термически-нестабильные соединения анализируют методом жидкостной хромато-масс-спеткрометрии:

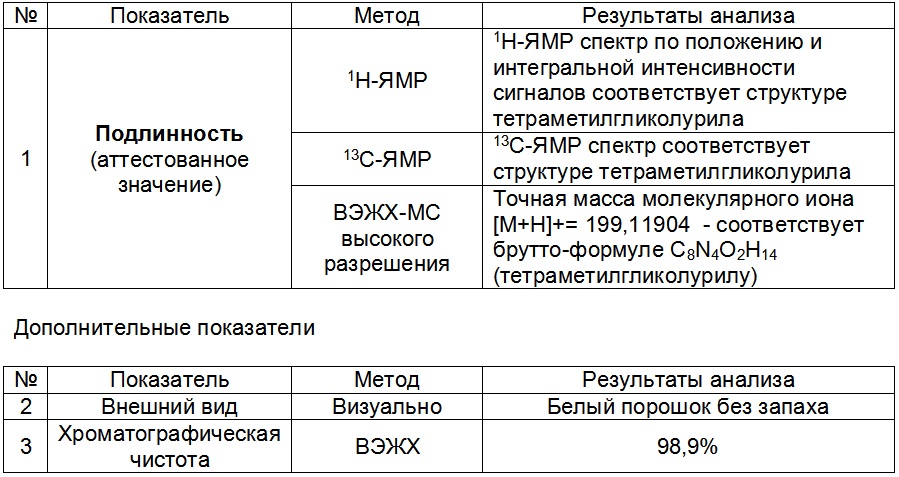
Записывают хроматограмму и снимают масс-спектр пика основного вещества:
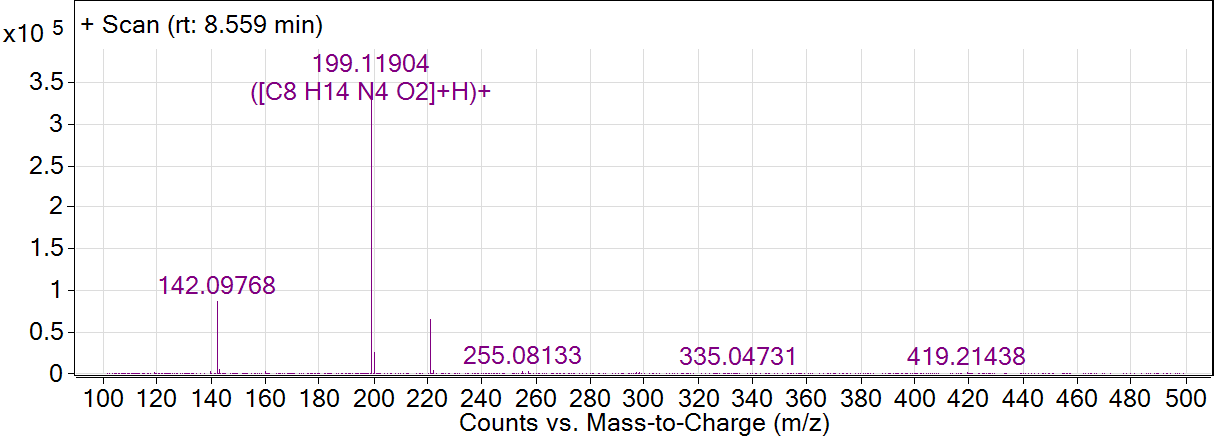
Ионизация в современных жидкостных масс-спектрометрах чаще всего проводится методом электроспрея (ESI). Это «щадящая» ионизация и обычно самый интенсивный пик на масс-спектре соответствен молекулярному иону. Т.е. по масс-спектру в первую очередь устанавливают молекулярную массу соединения, что позволяет подтвердить брутто-формулу.
Из масс-спектра видно, что молекулярный ион имеет отношение массы к заряду m/z = 199.11904 (M+H)+, что соответствует брутто-формуле соединения С8N4O2H14
Летучие и термически-стабильные соединения анализируют методом газовой хромато-масс-спектрометрии:

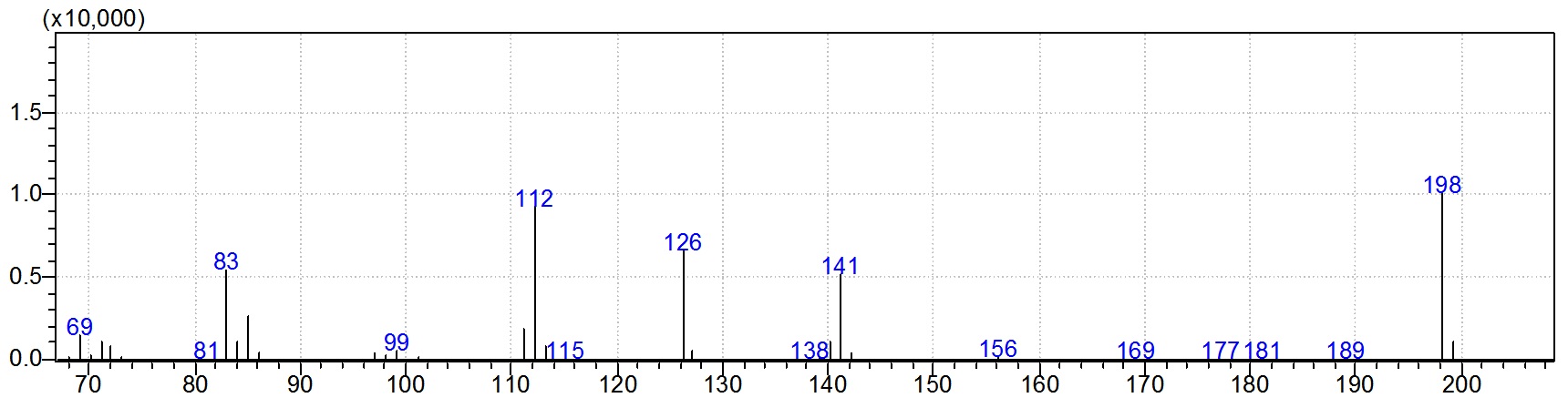
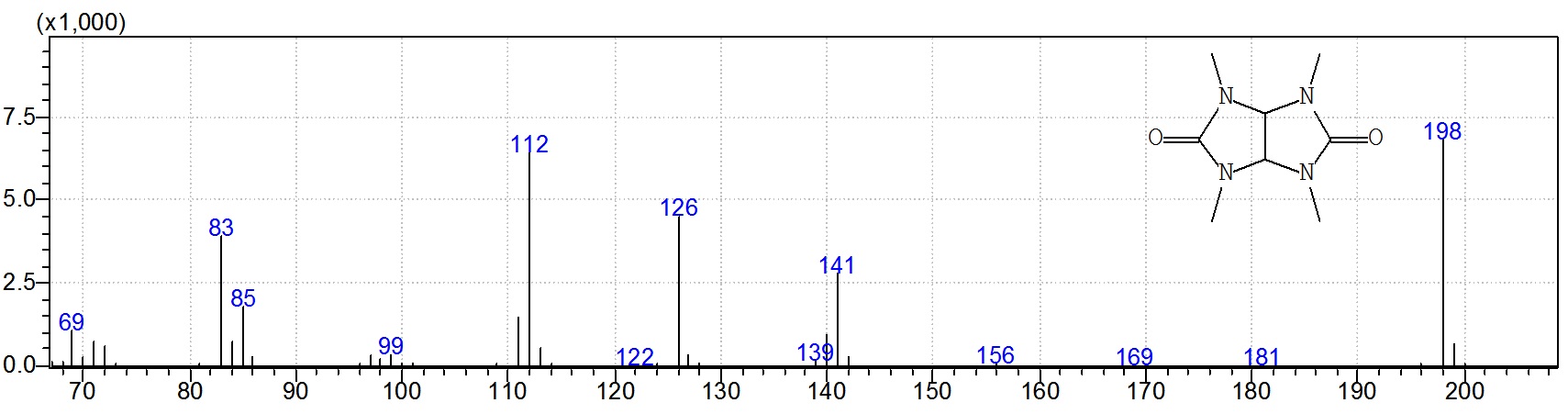
ЯМР-спектроскопия
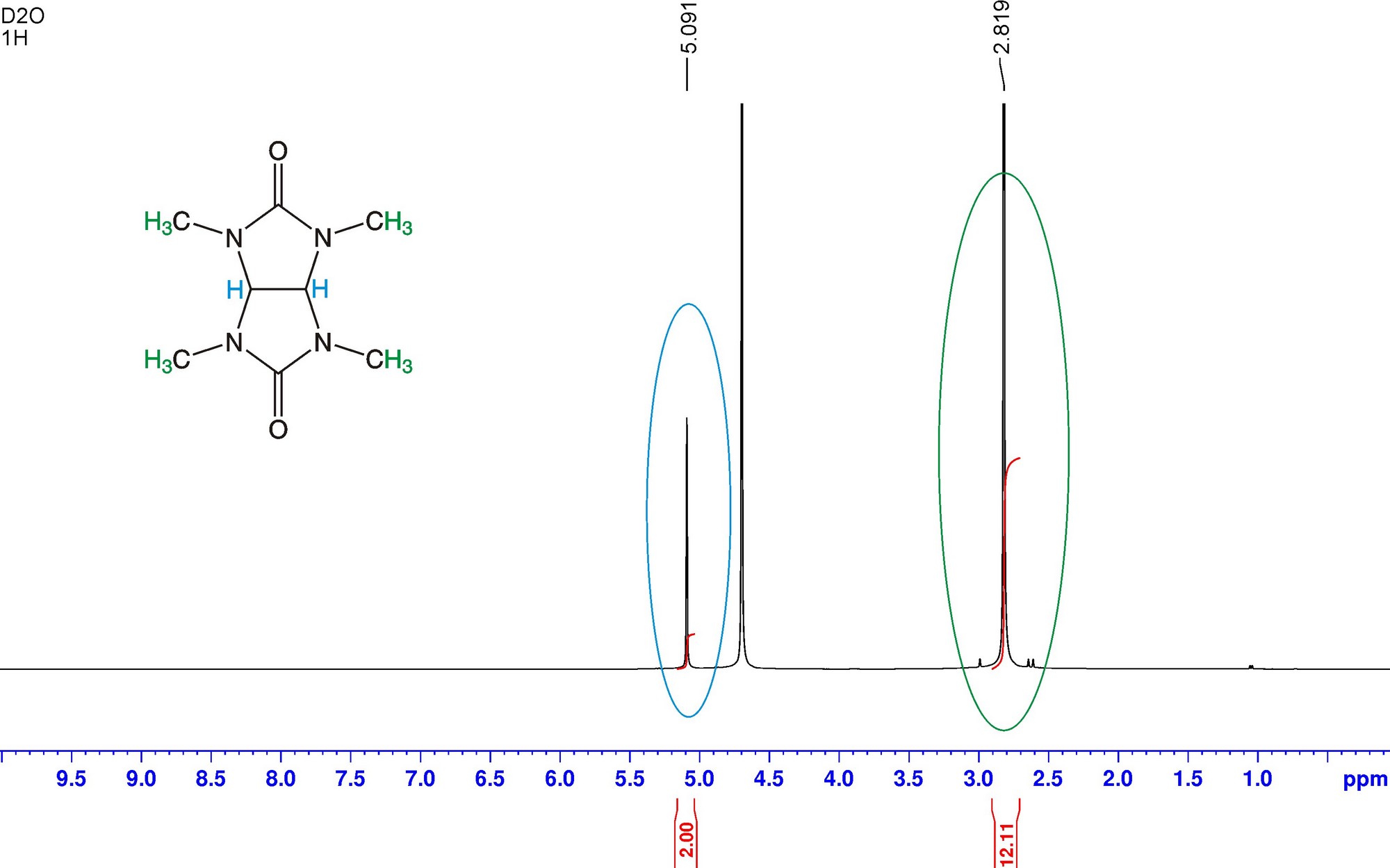

Для сложных соединений не всегда удается полностью «расшифровать» ЯМР-спектр. Однако, связка «ЯМР + масс-спектрометрия» считается золотым стандартом для установления структуры органических соединений.
Дополнительные показатели
Аттестовать образцы для качественного анализа (идентификации) по показателю «массовая доля основного вещества» не требуется. Однако, в качестве дополнительных показателей часто приводят:
Дополнительным подтверждением брутто-формулы может служить элементный анализ (массовая доля C,H,N,S), однако на практике (при наличии ЯМР и масс-спектрометрии), по нашему мнению большого смысла делать CHNS-анализ не имеет.
Пример спецификации
Установление аттестованного значения для вторичных СО
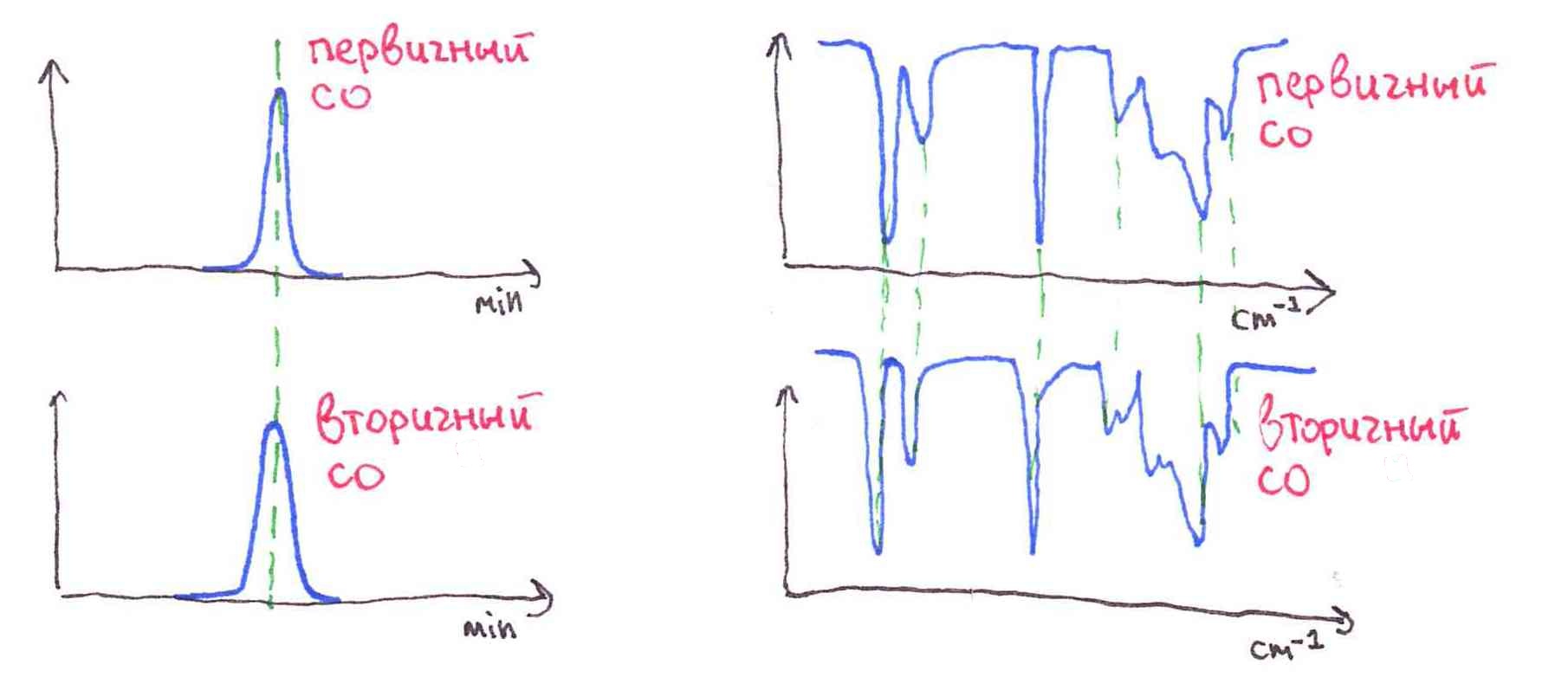
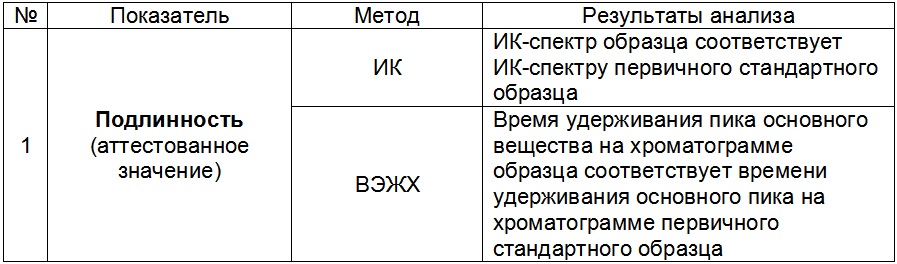
Подтверждение структуры вторичного (secondary) СО для качественного анализа проводят:
Пример спецификации
СО основного вещества для количественного анализа
СО основного вещества для количественного анализа применяется:
Установление аттестованного значения для первичных СО
Для первичных СО оба показателя должны устанавливаться первичными методам. Установление подлинности обсуждали в разделе про СО для качественно анализа.
К определению МДОВ в «СО для количественного определения» предъявляются особые требования. Считается необходимым подтвердить значение МДОВ как минимум двумя независимыми методами:
Для определения МДОВ методом «баланса масс»:
Значение МДОВ, полученное прямым титриметрическим методом должно быть близко к значению, полученному методом «баланса масс».
Пример спецификации
Дополнительное подтверждение чистоты
В качестве дополнительного подтверждения чистоты используют элементный (CHNS)-анализ, дифференциальную сканирующую калориметрию (ДСК) и косвенно ЯМР.
CHNS-анализ
Существуют подход к расчету чистоту органических соединения по данным элементного анализа [Ревельский И.А. и др. Определение основного компонента в высокочистых химических веществах состояние вопроса и перспективы, Журн. аналит. хим., 2009, т. 64, № 9]. Однако, этот подход применим для высокочистых веществ, не содержащих примесей с теми же элементами, что и основное вещество. Для органических соединений и фарм. субстанций элементный анализ является скорее косвенным подтверждением структуры.
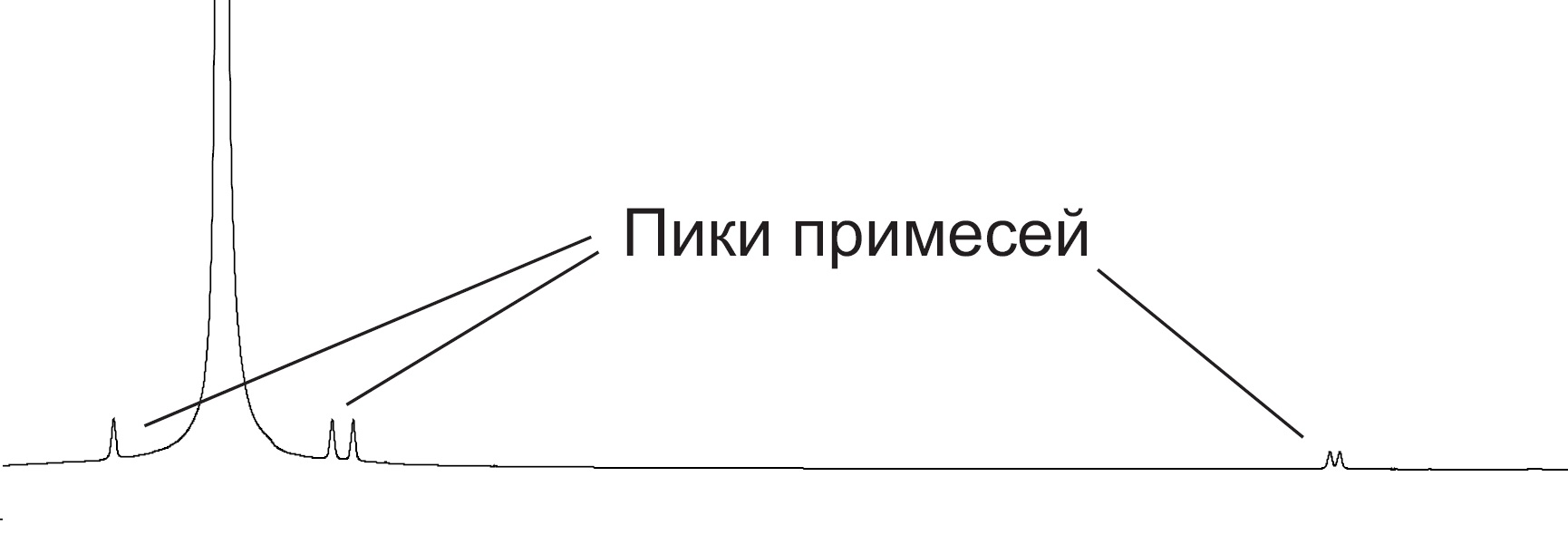
Оценка наличия примесей по 1H-ЯМР спектру
При достаточно высоком содержании примесей (
от 1 до 10%) они могут проявляться на 1H-ЯМР спектре в виде дополнительных пиков, не свойственных основному веществу.
Результаты оценки чистоты методом CHNS-анализа, ДСК и ЯМР являются дополнительным косвенным подтверждением, и не используются в расчетах.
СО примесей
Для проверки разрешающей способности хроматографической системы достаточно использовать СО примеси для качественного анализа (без установления массовой доли основного вещества).
Если примесь не может быть получена в достаточном количестве, возможны следующие варианты:
— подготовка стандартного образца, содержащего смесь основного соединения(ий) и примеси или примесей;
— подготовка стандартного образца, содержащего смесь указанных примесей.
ОФС.1.1.0007.18 “Стандартные образцы”, ГФ XIV
Для СО примесей для количественного анализа определяют структуру (подлинность) и массовую долю основного вещества (МДОВ). Требования к чистоте СО примесей ниже, чем для основного вещества:
При количественном содержании основного вещества от 95 % и выше его принимают за 100 %. При содержании основного вещества менее 95 % в расчетах необходимо учитывать значение фактического содержания.
ОФС.1.1.0007.18 “Стандартные образцы”, ГФ XIV
Оценивание неопределенности аттестованного значения
Результаты определения аттестованного значения массовой доли основного вещества желательно представлять в виде:

Существует два подхода к оценке неопределенности:
Фармокопейный центр Украины и статья 5.12 ГФУ «Стандартные образцы» предьявляет особые требования к значению неопределенности СО:
Аттестация СО предприятия коренным образом отличается от обычного анализа субстанции на соответствие НД. Требования к неопределенности результатов для аттестации СО в 3 раза более жесткие (!), чем для анализа субстанции. В связи с этим при аттестации используются специальные приемы работы (поскольку фактически требования к результатам анализа близки к предельным возможностям метода анализа).
Аттестация, оценка однородности и стабильности, упаковка, маркировка и хранение
Аттестация СО предполагает проведение испытаний по исследованию однородности, стабильности, определению аттестованного значения и границ его погрешности или неопределенности, определению оптимальных условий хранения и транспортировки.
ОФС.1.1.0007.18 “Стандартные образцы”, ГФ XIV
По итогам аттестации составляется отчет, содержащий следующие разделы:
Примеры оценки однородности и стабильности СО можно посмотреть в публикациях:
Где взять материал для изготовления СО предприятия?
СО основного вещества
Где организовать аттестацию СО?
Для определения массовой доли основного вещества требуется валидированная титриметрическая методика, и валидированная методика количественного определения примесей (для «баланса масс»).
Поэтому самым логичным решением является аттестация СО по показателю «массовая доля основного вещества» в заводской лаборатории предприятия, т.к. в ней уже внедрены валидированные методики анализа субстанции, из которой планируется делать СО.
Подтвердить структуру стандартного образца на поверенном оборудовании можно в нашей лаборатории.
Бесплатная консультация по аттестации СО предприятия
Есть вопросы по аттестации фармацевтических СО предприятия? Сможем бесплатно проконсультировать по скайпу.
Литература
ОФС.1.1.0001.15 Правила пользования фармакопейными статьями
Содержимое (Table of Contents)
ОФС.1.1.0001.15 Правила пользования фармакопейными статьями
Взамен ст. ГФ XI, вып.1 Взамен ГФ XII, ч.1, ОФС42-0031-07
Настоящая общая фармакопейная статья определяет правила применения терминов, понятий и методов, используемых в фармакопейных статьях.
Описание.
Указывают характеристики физического состояния и цвет лекарственного средства; если необходимо, приводят информацию о запахе и гигроскопичности.
Твердые субстанции могут быть крупнокристаллическими, кристаллическими, мелкокристаллическими или аморфными.
Крупнокристаллический порошок. Не более 40 % частиц порошка должно быть размером менее 0,4 мм.
Кристаллический порошок. Не менее 95 % частиц порошка должно быть размером менее 0,4 мм и не более 40 % — размером менее 0,2 мм.
Мелкокристаллический порошок. Не менее 95 % частиц порошка должно быть размером менее 0,2 мм.
Аморфный порошок — это порошок, не имеющий признаков кристаллическою строения.
Характеристики кристалличности и гигроскопичности в описании приводятся для информации и испытанию не подлежат. При необходимости нормирования величины частиц в нормативной документации приводят специальный раздел.
Субстанции жидкой консистенции могут быть охарактеризованы такими терминами, как вязкие, подвижные, легколетучие и т.д.
Газообразные субстанции характеризуют по цвету и запаху.
Цвет лекарственного средства следует характеризовать названиями: белый, синий, зеленый, желтый, оранжевый, красный и т.п. При оттеночных цветах на первом месте указывают тот цвет, который содержится в меньшей доле, а затем через дефис — преобладающий цвет (например, красно- коричневый).
Слабоокрашенные образцы имеют оттенок цвета, название которого характеризуют суффиксом «-оват» (например, «желтоватый») или добавляют приставку «светло-» (например, «светло-желтый»).
Цвет твердых веществ следует определять на матово-белом фоне (белая плотная или фильтровальная бумага) при рассеянном дневном свете в условиях минимального проявления тени. Небольшое количество вещества (0,5 — 2,0 г) помещают на белую бумагу и без нажима равномерно распределяют по поверхности бумаги (осторожно разравнивают шпателем или другим приспособлением) так, чтобы поверхность оставалась плоской.
Запах.
Запах следует характеризовать терминами: «без запаха», «с характерным запахом», «со слабым характерным запахом». Если запах не охарактеризован, то подразумевается его отсутствие у анализируемого лекарственного средства.
Испытание проводят сразу после вскрытия упаковки. 0,5 — 2,0 г лекарственного средства равномерно распределяют на часовом стекле диаметром 6-8 см; через 15 мин определяют запах на расстоянии 4-6 см или делают вывод о его отсутствии. В случае легко летучих жидких лекарственных средств наносят 0,5 мл испытуемого образца на фильтровальную бумагу и запах определяют сразу же после нанесения, если нет других указаний.
Масса.
«Взвешивание по разности» (например, до и после высушивания/прокаливания при определении потери в массе при
высушивании; золы общей; золы, нерастворимой в хлористоводородной кислоте и др.) проводят при одинаковых условиях (температура, давление, влажность), используя одни и те же средства измерения и лабораторную посуду. Интервал времени между двумя взвешиваниями определяется свойствами и количеством высушиваемого/прокаливаемого остатка.
После прокаливания/высушивания тигель или бюкс следует охлаждать в эксикаторе до температуры окружающей среды. Промежутки времени с момента извлечения тигля или стаканчика для взвешивания из эксикатора до момента взвешивания должны быть одинаковыми.
Массу следует считать постоянной, если разность результатов двух последующих взвешиваний не превышает 0,0005 г для 1,0 г взятого вещества.
Термин «невесомый» означает, что масса не превышает 0,0005 г.
Объем.
Для обеспечения требуемой точности измерений стеклянная мерная посуда должна соответствовать требованиям класса А Международного стандарта (ISO). Допускается использование стеклянной мерной посуды по ГОСТам (не ниже 1 класса точности).
Понятие «капля» означает объем от 0,02 до 0.05 мл в зависимости от растворителя; для водных растворов объем капли, отмериваемый стандартным каплемером, равен 0,05 мл (в 1 мл содержится 20 капель).
Температура.
Помимо конкретного указания температуры используют также следующие термины:
* Данные термины не применяются при указании условий хранения лекарственных средств, т.к. в этих случаях необходимо указывать конкретные температурные интервалы.
Под «водяной баней» понимают кипящую водяную баню, если в фармакопейной статье не указана температура нагревания.
Испытания следует проводить при комнатной температуре, если нет других указаний.
Если при проведении испытания, когда имеет значение температура, она не указана, то подразумеваю! температуру 20 °С.
Если в тесте «Потеря в массе при высушивании» температурный интервал не указан, то подразумевается, что он равен ± 2 °С от указанного значения.
Влажность.
Основные режимы хранения лекарственных средств в нормальных условиях подразумевают обеспечение относительной влажности воздуха в помещениях хранения лекарственных средств 50 — 60 %. Под термином «сухое место» понимают влажность не более 50 %.
Вакуум.
Точность измерения.
При описании количественного определения или испытания с численно заданными пределами количества вещества, необходимое для проведения испытания количество указывают приблизительно; в действительности оно может отклоняться в пределах ±10% от указанного. Необходимо взять точную навеску анализируемого вещества (или отмерить его каким-либо друг им способом) и все вычисления производить для этого точного количества. Если пределы испытания заданы не численно, а определяются путем сравнения со стандартом при тех же условиях, для испытания берут строго указанное количество вещества. Реактивы всегда берут в строго указанных количествах.
Если значения массы навесок или объемов не используют для дальнейших расчетов, то точность их взятия (отмеривания, отвешивания) должна согласовываться с указанной точностью.
Точность измерений следует обозначать числом десятичных знаков после запятой данного числового значения. Точность взвешивания должна быть ± 5 единиц после последней указанной цифры; например, навеску 0,25 г следует понимать как лежащую в интервале от 0,245 до 0,255 г. Объемы отмеряют следующим образом. Если после запятой стоит «0» или число, заканчивающееся нулем (например, 10,0 мл или 0,50 мл), требуемый объем отмеряют с помощью пинетки, мерной колбы или бюретки. В остальных случаях можно использовать градуированный мерный цилиндр или градуированную пипетку. Микролитры отмеряют с помощью микронипетки или микрошприца.
Точная навеска.
«Точная навеска» означает взвешивание на аналитических весах с погрешностью ± 0,0002 г. Если не указано «точная навеска» и точность взвешивания не задана числом десятичных знаков, то навеску следует брать с погрешностью ± 0,01 г.
При определении массы в граммах с точностью более 4 десятичных знаков следует пользоваться весами с метрологическими или техническими характеристиками, обеспечивающими требуемую точность взвешивания.
Время.
Понятие «сразу» означает отрезок времени не более 30 с.
Понятие «свежеприготовленный раствор» означает раствор, приготовленный не более чем за 8 ч до его применения, если нет других указаний.
Растворители.
Если для растворов не указан растворитель, то подразумевают водные растворы.
Под названием «вода», как растворитель, если нет особых указаний, следует понимать воду, соответствующую требованиям фармакопейной статьи «Вода очищенная». Термин «вода дистиллированная» использованием метода Фишера (полумикрометода и микрометода) или метода дистилляции в соответствии с ОФС «Определение воды».
Под названием «спирт», если нет особых указаний, следует понимать спирт этиловый, «этанол» — спирт этиловый абсолютированный; под названием «эфир» — эфир диэтиловый.
При определении спирта в лекарственных препаратах под процентом подразумевают объемный процент.
Если для проведения испытания требуется использовать растворитель с растворенным в нем индикатором и контрольный опыт не предусмотрен, то растворитель предварительно нейтрализуют по этому индикатору.
Если указано, что при приготовлении смеси растворителей их берут в соотношении (а:в), то имеется в виду соотношение объемов. Например, соотношение гексан — бензол (1:3) означает, что смешивают 1 объем гексана с 3 объемами бензола.
Реактивы.
Для испытаний применяют реактивы квалификации «чистый для анализа». В этом случае квалификация реактива не указывается. При применении реактивов другой квалификации следует приводить соответствующее указание.
Индикаторы.
При титриметрических определениях раствор индикатора, если нет других указаний, добавляют в количестве 0,2 мл или 1 — 5 капель.
Растворы.
Под принятым способом обозначения концентрации растворов твердых веществ в различных растворителях 1:10, 1:2 и т.д. следует подразумевать содержание массовой доли вещества в указанном объеме раствора, т.е. при приготовлении раствора 1:10 следует брать 1 г вещества и растворителя до получения 10 мл раствора; при приготовлении раствора 1:2 следует брать 1 г вещества и растворителя до получения 2 мл раствора и т.д.
Под обозначением «ч» подразумевают массовые части.
Обозначение «ррт» (частей на миллион) подразумевает массовое соотношение.
Процентная концентрация раствора может иметь одно из трех значений:
Если «%» используется без обозначения (м/м, м/о или о/о), то подразумевается массовый процент для смесей твердых веществ, массо-объемный процент для растворов или суспензий твердых веществ в жидкостях, объемный процент для растворов жидкостей в жидкостях и массо-объемный процент для растворов газов в жидкостях. Например, 1 % раствор приготавливают растворением 1 г твердого вещества или 1 мл жидкости в растворителе с получением в последующем 100 мл раствора.
Молекулярная масса.
Под молекулярной массой описанных в фармакопее соединений понимают относительную молекулярную массу, которая рассчитывается по таблице относительных атомных масс 1997 г., принятой Международным союзом но теоретической и прикладной химии (IUPAC) и основанной на шкале углерода-12.
Если молекулярная масса вещества меньше 400, приводят два десятичных знака, если больше 400 — один десятичный знак.
Пределы содержания.
Указываемые пределы основываю гея на результатах, полученных в рамках аналитической практики; в них уже учтены обычные аналитические погрешности, допустимый разброс при производстве и приготовлении, а также ухудшение качества в процессе хранения в пределах, которые считаются приемлемыми.
Если в разделе «Количественное определение» для индивидуальных веществ не указан верхний предел содержания, следует считать, что
последний составляет 100,5 % определяемого вещества.
В тех случаях, когда содержание вещества в препарате выражается в пересчете на сухое или безводное вещество, следует понимать, что потеря в массе при высушивании или содержание воды определены тем методом, который описан в соответствующей фармакопейной статье или нормативной документации.
Контрольный опыт.
Под контрольным опытом подразумеваю] определение, проводимое с теми же количествами реактивов и в тех же условиях, но без испытуемого лекарственного средства, если нет других указаний в фармакопейной статье.
Методы испытаний.
Как правило, в общей фармакопейной статье (ОФС) на методы контроля описано несколько методов анализа. Если в фармакопейной статье или нормативной документации не указано, какой из методов используется, то применяют первый метод, описанный в ОФС.
Защищенное от света место.
Если указано, что испытание проводят «в защищенном от света месте», то это означает, что следует принять меры во избежание попадания прямого солнечного света, любого другого яркого света, а также ультрафиолетовых лучей, например, путем использования посуды из специального стекла, работы в затемненной комнате и т.д.
Фильтрование.
Если для определения содержания примеси используют фильтрат, то перед фильтрованием фильтр промывают соответствующим растворителем. При этом жидкость следует пропускать через подходящий фильтр до тех пор, пока фильтрат не будет прозрачным. При промывании подкисленной водой следует для подкисления применять ту кислоту, которая используется для определения. Если для дальнейших испытаний используют определенную часть фильтрата, то для фильтрования применяют сухой фильтр и первую порцию фильтрата отбрасывают. Объем этой порции не должен превышать 20 % от общего объема фильтрата.
Если не указана марка фильтра, то подразумевают любой бумажный фильтр.
Вычисление результатов испытания.
При всех количественных определениях результат вычисляют с точностью, на два десятичных знака большей, чем число десятичных знаков, указанное в фармакопейной статье или нормативной документации, если это допустимо с точки зрения точности метода. Затем цифры округляют до указанного в пределе количества значащих цифр (если нет других указаний). При этом последнюю цифру увеличиваю! на единицу, если цифра, отбрасываемая при округлении, больше или равна 5. Если цифра, отбрасываемая при округлении, меньше пяти, последнюю цифру оставляют неизменной.
Хранение.
При отсутствии особых указаний лекарственные средства необходимо предохранять от воздействия влаги, замораживания и повышенной температуры.
Стандартные образцы.
Современные методы анализа
предусматривают использование стандартных образцов. В качестве стандартных образцов в фармакопейной статье или нормативной документации должны быть предусмотрены стандартные образцы, введенные в действие уполномоченным фармакопейным органом.
Для проведения текущих анализов при производстве лекарственных средств могут использоваться стандартные образцы серийных субстанций при условии, что они удовлетворяют требованиям нормативной документации и аттестованы по стандартным образцам, введенным в действие в установленном порядке.