перелом нижней стенки правой орбиты
Перелом нижней стенки правой орбиты
Перелом нижней стенки орбиты — самая частая локализация. Он возникает в результате удара по глазному яблоку или по краю орбиты. При многих повреждениях развиваются лишь отёк и экхимоз тканей орбиты. При переломах с ущемлением мягких тканей и сохранением диплопии или при обширных переломах с развитием энофтальма требуется проведение оперативной коррекции.
Эпидемиология и этиология:
• Возраст: обычно наблюдают у пациентов в возрасте 20-40 лет.
• Пол: чаще обнаруживают у мужчин.
• Этиология: прогиб и перелом нижней стенки орбиты происходит при прямом ударе по её нижнему краю. При другом механизме травмы происходит подъём интраорбитального давления и «взрыв» тонкой нижней стенки орбиты.
Внешний вид перелома нижней стенки орбиты. Отёк и экхимоз орбиты различной степени выраженности. Наиболее частые симптомы — инфраорбитальная гипестезия и ограничение подвижности глазного яблока с развитием двоения. При обширных переломах после исчезновения отёка тканей орбиты развивается энофтальм. Кроме того, признаком перелома считают крепитацию.
Визуализация перелома нижней стенки орбиты. При КТ обнаруживают перелом нижней стенки орбиты, часто с наличием крови в синусе. При небольших переломах часто происходит ущемление мягких тканей (например, тканей, окружающих нижнюю прямую мышцу; сама мышца ущемляется очень редко). МРТ недостаточно информативна.
Особые случаи. У детей при переломе нижней стенки орбиты экхимоз иногда отсутствует, но возможно тяжёлое ущемление нижней прямой мышцы, возникновение тошноты и рвоты. Таких пациентов очень сложно обследовать. Следует провести освобождение ущемлённой мышцы в течение 24-48 ч, поскольку позже развивается её ишемия.
Лечение перелома нижней стенки орбиты. При развитии функциональной диплопии, не разрешающейся после исчезновения отёка, требуется проведение реконструкции открытым доступом. При переломах, охватывающих более половины нижней стенки орбиты, развивается выраженный энофтальм, в связи с чем также рекомендуют выполнение реконструктивной операции в течение 2 нед после травмы. При восстановлении стенок орбиты в большинстве случаев устанавливают различные имплантаты.
Прогноз. Хороший, если восстановление проведено в течение 2 нед. У некоторых пациентов обнаруживают прямое повреждение нерва или мышцы, при этом улучшение наступает в течение нескольких месяцев или отсутствует.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Реконструкция орбиты глаза
Восстановление травмированной глазницы с сохранением зрения и подвижности глаза.
Реконструкция орбиты глаза чаще всего выполняется в связи с травмой после ДТП. В результате сильного удара в область глазного яблока возникает перелом стенок орбиты. Восстановление орбиты выполняется собственными тканями пациента или титановой сеткой.
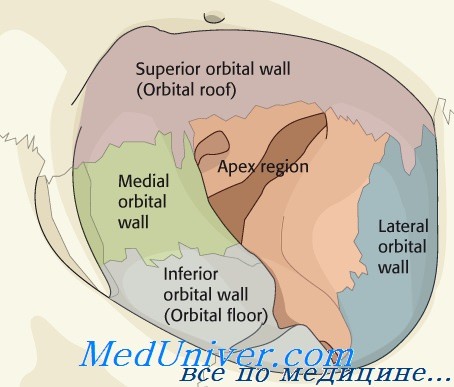
Анатомия периорбитальной зоны
Перелом нижней стенки орбиты
Травма нижней стенки глазницы приводит к тому, что содержимое орбиты проваливается в гайморову пазуху и положение глаз становится асимметричным:
Если при травме повреждается инфраорбитальный нерв, который проходит сквозь нижнюю стенку орбиты, то теряется чувствительность скуловой зоны, верхних зубов, крыла носа с соответствующей стороны.
Пластика нижней стенки орбиты
Осложнения после реконструкции дна орбиты
Сразу после операции глаз находится в положении выше, чем необходимо. Это называется гиперкоррекция. В течение месяца гиперкоррекция проходит, и положение глаз становится симметричным. При неправильном планировании гиперкоррекция не учитывается, и асимметрия частично возвращается.
Реабилитация после реконструкции нижней стенки орбиты
После операции пациент должен находится в клинике в течение одного-двух дней для профилактики образования гематом внутри орбиты.
На 4-5 сутки снимаются швы с конъюнктивы.
В течение одной-двух недель проходят отёки под глазами.
Через месяц проходит гиперкоррекция, положение глаз нормализуется.
Через 2 месяца можно оценивать конечный результат операции.
Перелом нижней стенки правой орбиты
ВЧП — верхнечелюстная пазуха
ВСТ — волокнистая соединительная ткань
РФКТ — ретикулофиброзная костная ткань
ПКТ — пластинчатая костная ткань
МСКТ — мультиспиральная компьютерная томография
Перелом стенки глазницы — распространенная патология, частота которой составляет от 18 до 80% среди всех черепно-мозговых травм [1, 2]. Перелом нижней стенки глазницы (типа blow-out) встречается в 15—20% всех орбитальных переломов [3, 4]. Восстановление нижней стенки глазницы является сложной и актуальной клинической проблемой, находящейся на стыке нескольких специальностей: оториноларингологии, офтальмохирургии и челюстно-лицевой хирургии. Выбор тактики ведения больных с указанной патологией определяется многими факторами: размерами дефекта, наличием пролапса содержимого орбиты в верхнечелюстную пазуху (ВЧП) или защемления глазодвигательных мышц (нарушения со стороны органа зрения, длительность периода, прошедшего с момента травмы), наличием энофтальма (нарушения подвижности глазного яблока) и др. [5, 6]. Повреждение нижней стенки глазницы обычно подтверждается компьютерной томографией, которая дает возможность оценить состояние костных структур орбиты, размер и местоположение дефекта, а также позволяет измерить любое смещение костных стенок и мягких тканей глазницы для выбора оптимального способа хирургического лечения [3, 7—9].
Известно, что раннее выполнение оперативного вмешательства улучшает прогноз для больного. Несмотря на то, что хирургическую реконструкцию дефекта нижней стенки орбиты можно отложить, при повреждении типа blow-out существует риск защемления мышц, при котором необходимо выполнить экстренное оперативное вмешательство [5, 6]. Для восстановления нижней стенки глазницы применяются различные материалы, в том числе титановые конструкции и разные варианты костных трансплантатов, однако экспериментальное обоснование по их применению отсутствует [2, 10—13].
Цель исследования — представить экспериментальное и клиническое обоснование применения нетканной титановой конструкции и аллогенного деминерализованного костного трансплантата для восполнения дефекта нижней стенки глазницы.
Материал и методы
На базе отдела морфологии ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава России (Уфа) были выполнены экспериментальные исследования на 24 полуторагодовалых кроликах породы шиншилла обоего пола. У лабораторных животных стоматологическим бором моделировали дефект стенки ВЧП диаметром 4 мм. Ранее экспериментальным путем было установлено, что данный размер дефекта не замещается костной тканью самопроизвольно. Затем производили закрытие костного дефекта с помощью конструкции на основе пористого титана (n=12), аллогенного деминерализованного костного трансплантата (n=12) по технике press-fit («заглушка»), после чего выполняли послойное ушивание мягких тканей над областью пластики.
Разработанные технологии закрытия дефектов нижней стенки глазницы применяли в соответствии с регистрационным удостоверением №ФСР 2011/12012 от 30.09.11. С использованием данных технологий нами были прооперированы 15 пациентов с дефектами нижней стенки глазницы.
В тканевом банке ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава России (Уфа) производятся аллогенные трансплантаты костного происхождения «Аллоплант» (ТУ 9398−001−04537642−2011), адаптируемые под размер дефекта нижней стенки глазницы. При обширных (более 3 см) дефектах верхней стенки ВЧП (n=7, или 47%) использовали нетканую титановую конструкцию производства ООО «Прототип» (Самара; ТУ 9437−002−01963143−2010).
Результаты
Применение нетканной титановой конструкции. Через 2 мес после имплантации титановой конструкции на гистологических препаратах выявлялся регенерат, представленный комплексом костных тканей, замещающих дефект.
Перифокальная зона, непосредственно прилежащая к титановой конструкции, была образована из незрелой грубоволокнистой костной ткани, состоящей из крупнопетлистых тонких трабекул. В межтрабекулярных пространствах выявлялась рыхлая волокнистая соединительная ткань (ВСТ), инфильтрированная фибробластами. В ней были обнаружены развитая сеть кровеносных сосудов, жировая ткань и клетки костного мозга. В полостях центральной зоны регенерата наблюдались мелкоячеистые (наноструктурированные) полые структуры, которые состояли из множества округлых ячеек, сгруппированных между собой в кластеры. Гематоксилином и эозином прокрашивались в розовый цвет только стенки ячеек, просветы были свободные. Данные образования не вызывали выраженной воспалительной реакции, однако в костных полостях они покрывались тонкой соединительнотканной капсулой.
В дальнейшем объем коллагеновых волокон увеличивался, петли титана обрастали рыхлой соединительной тканью с небольшим количеством фибробластов, макрофагов и полностью погружались в волокнистый матрикс. Рыхлая ВСТ постепенно трансформировалась в плотную неоформленную соединительную ткань с толстыми пучками коллагеновых волокон, редуцированными кровеносными сосудами. Происходила остеоинтеграция: миграция остеогенных клеток со стороны материнской кости и минерализация коллагеновых волокон, образовавшихся вокруг петель титана (рис. 1). 
При этом петли титана оказывались в толще костного матрикса. Вокруг кластеров титана в кости определялись зоны активного аппозиционного костеобразования. Каналы выстилали активные остеобласты II типа, расположенные плотно друг к другу в один ряд и синтезирующие остеоид и костный матрикс. Сами ячейки титана приобретали более плотную структуру, между ними определялась ВСТ с утолщенными коллагеновыми пучками. При окраске гематоксилином и эозином просветы ячеек окрашивались ацидофильно в розовый цвет и базофильно — в голубой. Некоторые ячейки теряли свою первоначальную структуру и были деформированы. Их стенки лизировались, гомогенизировались и представляли собой плотную бесформенную массу (рис. 2). 
В глубокой зоне костного регенерата, непосредственно прилегающей к материнской кости, выявлялись признаки последовательной трансформации грубоволокнистой незрелой кости в зрелую пластинчатую кость. По всей окружности дефекта определялась тонкая неравномерная полоса зрелой губчатой костной ткани с многочисленными костными лакунами, заполненными остеоцитами. Утолщенные костные трабекулы постепенно созревали в пластинчатую кость с характерной структурой. В костном матриксе пластинчатой кости обнаруживалась развитая сеть гаверсовых каналов, заполненных рыхлой соединительной тканью с кровеносными сосудами.
Таким образом, репаративное костеобразоование происходило центростремительно — от периферии к центру (аппозиционный остеопоэз). Причем скорость процессов остеогенеза и биодеградации титана была различной — темп деструкции имплантата оказался ниже. Механизм остеогенеза представлен интрамембранозным окостенением, т. е. костеобразование происходило через стадию формирования ВСТ с постепенной трансформацией в грубоволокнистую костную ткань и дальнейшим преобразованием в пластинчатую кость. Титановая конструкция не вызывает бурной воспалительной реакции и не обладает иммуногенной активностью, но окружающие ткани реагируют на имплантат как на инородное тело — происходит его инкапсулирование и развитие фиброза.
Применение деминерализованного костного трансплантата. Несколько иные механизмы заместительной регенерации были обнаружены в области имплантации деминерализованного костного трансплантата в трепанационный дефект переднелатеральной стенки ВЧП. В ранние сроки (на 14-е сутки) в области трансплантации определяется полиморфноклеточная инфильтрация. При этом в инфильтрате верифицируются клетки фибробластического, остеобластического и макрофагального дифферонов. Важно подчеркнуть отсутствие в составе клеточного инфильтрата представителей лимфоцитарного дифферона и сегментоядерных лейкоцитов, что свидетельствует об отсутствии гнойной инфекции в зоне подсадки аллогенного трансплантата.
На 45-е сутки деминерализованный костный трансплантат подвергается интенсивной деградации и лизису, о чем свидетельствует изменение его тинкториальных свойств. Однако на данном сроке деминерализованный костный трансплантат все же сохраняет значительную часть объема (рис. 3). 
Процессы резорбции превалировали над синтетической активностью фибробластов и остеобластов, поэтому на 45-е сутки формирующийся регенерат имел незначительные включения костной ткани и на 36,48±4,81% был представлен рыхлой ВСТ.
Далее (90-е сутки) происходит дальнейшая деградация аллогенного костного трансплантата. Большая часть костного биоматериала замещена новообразованной ретикулофиброзной костной тканью (РФКТ). Выраженной инфильтрации макрофагами в области подсадки трансплантата не наблюдается. Скорость резорбции костного трансплантата преобладала над скоростью заместительного остеогенеза. Сам трансплантат частично сохранил структурную организацию пластинчатой костной ткани (ПКТ). Формирующийся регенерат представляет собой плотную оформленную ВСТ с относительно бόльшим, чем в окружающих тканях, количеством клеточных элементов и сосудов. При этом в регенерате менее выражены извилистость коллагеновых волокон и плотность их упаковки. В составе регенерата определялись включения РФКТ. Как показывает морфометрический анализ, костная ткань при этом составляет значительный объем от общей площади исследуемой области.
В результате слияния двух встречных фронтов замещения аллогенного биоматериала на 180-е сутки формируется непрерывный массив РФКТ с включениями ПКТ (см. таблицу). 
Приводим описание клинических наблюдений пластики нижней стенки глазницы деминерализованным костным трансплантатом и нетканной титановой конструкцией.
Клинический пример 1
Пациент С., 17 лет, обратился в нейрохирургическое отделение стационара медико-санитарной части «Нефтяник» с жалобами на диплопию, сохраняющуюся в течение 1 мес после тупой травмы глазницы справа. На мультиспиральной компьютерной томографии (МСКТ) околоносовых пазух и орбиты определяется дефект верхней стенки правой ВЧП с пролабированием параорбитальной жировой клетчатки в пазуху (рис. 4). 
Под общим обезболиванием совместно с нейрохирургом выполнена нижняя орбитотомия. Область дефекта верхней стенки ВЧП освобождена от рубцов, параорбитальная клетчатка смещена кверху. Проведена ревизия ВЧП через верхнюю стенку с использованием эндоскопа «Элмед» 70° диаметром 4 мм. В область дефекта установлен предварительно смоделированный фрагмент деминерализованного костного аллогенного трансплантата (рис. 5). 
На 7-е сутки была выполнена контрольная МСКТ, которая подтвердила стабильное положение аллогенного трансплантата, при этом наблюдался незначительный реактивный отек слизистой оболочки ВЧП со стороны вмешательства (рис. 6). 
Клинический пример 2
Пациент Ш., 18 лет, обратился в нейрохирургическое отделение стационара медико-санитарной части «Нефтяник» с жалобами на диплопию, сохраняющуюся в течение 2 нед после тупой травмы глазницы справа. На МСКТ околоносовых пазух и орбиты справа определяется дефект верхней стенки ВЧП с пролабированием параорбитальной жировой клетчатки в пазуху (рис. 7). 
Под общим обезболиванием совместно с нейрохирургом выполнена нижняя орбитотомия. Область дефекта верхней стенки ВЧП освобождена от рубцов, параорбитальная клетчатка смещена кверху. Проведена ревизия ВЧП через верхнюю стенку с использованием эндоскопа Элмед 70° диаметром 4 мм. В область дефекта установлена предварительно смоделированная нетканная титановая конструкция (рис. 8). 
Мягкие ткани ушиты послойно, на кожу нижнего века наложен косметический шов. В полость носа на 10 мин были введены марлевые турунды, пропитанные 0,1% раствором оксиметазолина. Затем под контролем торцевого жесткого эндоскопа Элмед диаметром 4 мм инфильтрировали слизистую оболочку полости носа (перед крючковидным отростком, у основания и передний конец средней носовой раковины) 1% раствором лидокаина с адреналином 1:100 000. Распатором провели щадящую медиализацию средней носовой раковины, с помощью разработанного инструмента для мобилизации крючковидного отростка выполнили расширение полулунной щели за счет медиального смещения крючковидного отростка.
На 2-е сутки была выполнена контрольная МСКТ, которая подтвердила стабильное положение нетканной титановой конструкции и отсутствие реактивных изменений слизистой оболочки ВЧП. Произведено снятие косметического шва на нижнем веке, зрачки на одном уровне. Пациент отмечает отсутствие диплопии.
Заключение
Целью лечения орбитального перелома помимо освобождения заключенных мягких тканей является восстановление анатомии глазницы и предотвращение серьезных риногенных внутриглазничных осложнений. Клиническая оценка в сочетании с соответствующим рентгенологическим исследованием прооперированных пациентов подтверждает эффективность и безопасность использования нетканной титановой конструкции и аллогенного деминерализованного костного трансплантата при реконструкции нижней стенки орбиты. На основании экспериментального исследования сделан вывод о том, что использование пористого титана предпочтительнее при больших дефектах нижней стенки орбиты. Это связано с более низким темпом деструкции имплантата по сравнению с костным трансплантатом. В целом же выбор способа реконструкции дефекта нижней стенки орбиты типа blow-out должен осуществляться с учетом опыта хирурга и наличия соответствующего материала.
Авторы заявляют об отсутствии конфликта интересов.
Концепция и дизайн исследования: Д.Щ., А.И.К., В.К.
Сбор и обработка материала: Д.Щ., А.Щ., А.С.К.
Перелом нижней стенки глазницы
«Взрывные» переломы нижней стенки глазницы являются наиболее распространенным видом переломов глазницы и занимают второе место (после травм носа) по частоте встречаемости среди всех повреждений средней зоны лица. В большинстве случаев являются односторонними, хотя описаны не столь редкие (до 5 %) случаи возникновения двусторонних «взрывных» переломов нижней стенки орбиты.
Предполагаемые механизмы
Хотя первое описание и фоторегистрация травматического энофтальма, возникшего в результате тупой травмы глазницы у двенадцатилетнего мальчика, датированы 1889 г., причинно-следственная связь энофтальма с орбитальным переломом была установлена R. Pfeiffer лишь в 1943 г. Термин «blow-out» для обозначения растрескивания нижней стенки орбиты без вовлечения подглазничного края предложен J. M. Converse и B. Smith в 1956 г.

При обширных оскольчатых дефектах нижней стенки мягкие ткани не столько ущемляются, сколько смещаются вниз под воздействием силы тяжести и реактивного отека. Не столь многочисленные сторонники «механической» гипотезы, сформулированной R. Le Fort (1901), считают основным механизмом взрывного растрескивания дна орбиты волнообразные деформации, передающиеся с подглазничного края.
Гидравлический механизм вызывает гораздо более протяженные переломы, захватывающие не только всю нижнюю, но и медиальную стенку глазницы, пролапс мягких тканей и энофтальм. По мнению некоторых авторов, в возникновении перелома играют роль оба механизма, и противопоставлять их в корне неверно. Одновременная инициация обоих механизмов травмы, их сосуществование, взаимодополнение с доминированием в каждом конкретном случае какогото одного варианта и объясняет многообразие орбитальных фрактур.
Для изолированного «взрывного» перелома дна глазницы требуется меньше энергии, чем для повреждения медиальной стенки или возникновения инферо-медиального перелома. Этот, казалось бы, нелогичный, но давно известный клиницистам факт нашел свое объяснение в работе H. Takizawa с соавт. (1988). На основе экспериментов и последующего компьютерного моделирования авторы наглядно продемонстрировали, что очень важную роль играет не только толщина, но и контур (профиль) стенок глазницы. В частности, аркообразная крыша орбиты гораздо более устойчива к деформации, чем практически плоское дно, которое легче деформируется и ломается. Медиальная стенка еще более тонкая, но ее сзади наподобие контрфорсов укрепляют ячейки решетчатой кости. Поэтому для перелома медиальной стенки требуется больше механической энергии, чем для разрушения глазничного дна.
Способствуют повреждению дна орбиты такие анатомические образования, как нижняя глазничная щель, подглазничная борозда и канал, а также рефлекторное сокращение круговой мышцы глаза и наличие под орбитой большой воздухоносной полости. Именно недоразвитием верхнечелюстной пазухи и продолжающимся ростом глазницы объясняется редкость возникновения переломов дна орбиты у детей до 7–8 лет. Если фрактура все же возникает, то реже чем у взрослых требует хирургического лечения.
Классификация
Согласно рентгенологической классификации G. F. Fueger, A. T. Milauskas и W. Britton (1966), «взрывные» переломы подразделяются на шесть основных типов, некоторые из которых содержат подтипы:
Симптомы

Диагностика
Диагностике «взрывного» перелома нижней стенки глазницы способствуют весьма характерные жалобы, из которых наиболее важной является двоение при вертикальных движениях глаз, встречающееся у 58 % пациентов.
Первичное положение взора, а также изменение выраженности диплопии при движениях глазного яблока позволяет предположить зону ущемления нижней прямой мышцы.
В 1970 г. S. Lerman были сформулированы весьма интересные закономерности, касающиеся диплопии при «взрывных» переломах.
В качестве возможной причины девиации глазного яблока кверху рассматривается парез нижней прямой мышцы, смещение нижнего мышечного комплекса в зону перелома, неестественный угол прикрепления дислоцированной нижней прямой мышцы к склере.
В постановке диагноза помогает детальная оценка механизма травмы. При этом следует обратить внимание на два фактора, в значительной мере определяющих клиническую картину перелома: размер ранящего агента и энергетическую составляющую травмы. Если площадь тупого твердого предмета меньше размеров входа в глазницу, у пациента возможно развитие субконъюнктивального разрыва склеры. Если размеры ранящего снаряда больше размеров орбитального входа, то возможны два варианта:
Таким образом, анализ обстоятельств травмы имеет важное практическое значение, ибо позволяет предугадать характер повреждения и заподозрить те изменения, которые во время первичного осмотра могут маскироваться отеком и гематомой периокулярных тканей.
Объективное исследование начинается с наружного осмотра. На вероятный перелом дна орбиты указывают такие симптомы, как выраженный отек и гематома век, гипосфагма, хемоз бульбарной конъюнктивы.
Общепринятым является мнение, что при наличии у пациента подобной симптоматики достоверная оценка положения глазного яблока в орбите (в трех плоскостях) и объема его движений становится возможной лишь через 2–3 недели после травмы, так как реактивный отек и гематома мягких тканей глазницы могут скрыть энофтальм величиной до 3 мм.
Аксиальная дистопия (эно- или экзофтальм) определяется относительно здорового глаза с помощью экзофтальмометра Hertel-Krahn. Выбирается такой базис, чтобы упоры экзофтальмометра плотно прижались к передней поверхности латеральных краев орбиты. Врач оценивает своим левым глазом выстояние правого глаза пациента и наоборот. При оценке правого глаза испытуемого левый глаз врача открыт, а пациент должен смотреть на закрытый правый глаз врача. Используя свой левый глаз, исследователь сводит в одну параллельные линии в зеркале и по нанесенной на нем шкале оценивает выстояние роговицы.
Экзофтальм при повреждении нижней стенки глазницы возможен лишь в остром периоде травмы и обусловлен отеком и/или гематомой орбитальных тканей. Типичным для «взрывного» перелома симптомом является западение глазного яблока.
Энофтальм свидетельствует об увеличении объема орбиты, что характерно для «взрывного» перелома со
значительным смещением отломков (классический, инферомедиальный, тотальный).
K. Yab с соавторами (1997) на основании анализа КТ-грамм пациентов с глазничными переломами установили, что пока прирост орбитального объема не превысит 2 мл, энофтальм сохраняется на уровне 1 мм. Затем степень западения глазного яблока растет пропорционально увеличению объема глазницы, но при изолированном переломе нижней стенки никогда не превышает 4 мм.
Вертикальная дистопия (гипофтальм) оценивается относительно горизонтальной линии, проходящей через центр зрачка здорового глаза. Как правило, опущение глазного яблока свидетельствует о протяженном переломе нижней стенки глазницы. Наиболее выраженным вариантом гипофтальма являются казуистические случаи вывиха глазного яблока в верхнечелюстную пазуху.
Латеральная дистопия (во фронтальной плоскости) измеряется путем сравнения расстояния от середины переносицы до носовой части лимба. Разница между здоровой и поврежденной стороной свидетельствует о сопутствующем переломе медиальной стенки орбиты.
Тотальное ограничение подвижности обычно свидетельствует об отеке или гематоме орбиты. Диагностической ценностью обладает факт уменьшения супрадукции или инфрадукции на поврежденной стороне в сравнении с подвижностью парного глаза. Следует помнить, что очевидные ограничения моторики глазного яблока встречаются редко.
Для выявления не столь явных глазодвигательных расстройств проводится проба с «провоцированной» диплопией, основанная на оценке относительного положения в пространстве изображений, принадлежащих фиксируемому и отклоненному (пораженному) глазу.
Врач и пациент находятся на расстоянии 1,5–2 м и обращены лицом друг к другу. В руках у врача карманный фонарь, который он передвигает вправо, влево, вверх, вниз и в промежуточные положения, спрашивая при этом у пострадавшего, видит он одно или два изображения лампочки. Если пациент видит два изображения, то его просят сообщить, в каком положении относительно друг друга они находятся, каково расстояние между ними и когда оно увеличивается или уменьшается.
При оценке результатов исследования пользуются следующими правилами:
Дифференциальная диагностика между основными причинами расстройств моторики (парез веточки глазодвигательного нерва или ущемление мышцы в зоне перелома) осуществляется с помощью тракционного теста, который выполняют следующим образом

Противопоказанием к выполнению тестов является наличие у пациента болевого синдрома, блефароспазма, орбитальной гематомы или отека тканей, когда высока вероятность получения ложноположительных результатов.
Несмотря на то, что «взрывной» перелом демпфирует резко возросшее внутриорбитальное давление, в 30-40 % случаев подобные травмы сочетаются с различными повреждениями глаза, нередко (20-30 %) тяжелыми.
По данным L. Tong с соавторами (2001), из них 40 % приходятся на контузионные разрывы склеры. В 38 % случаев перелому нижней стенки глазницы сопутствуют повреждения за пределами костей лица, прежде всего черепа и головного мозга. Вообще, при «взрывном» переломе вероятность травмы глазного
яблока в 2,5 раза выше, чем при скулоорбитальном.
Поэтому в обязательном порядке следует убедиться в целости глазного яблока, являющейся непременным условием реконструкции нижней стенки орбиты. К сожалению, травмы глаза и периорбитальной области на этапе приема пациентов с переломами средней зоны лица нередко просматриваются.
При отсутствии (реальном или кажущемся) предметного зрения оценивается восприятие интенсивности обычного белого цвета здоровым и пораженным глазом. Для оценки состояния зрительного нерва проводится проба на различение красного цвета. Окрашивание тестового объекта (им может быть
просвечиваемая фонариком ногтевая фаланга указательного пальца или колпачок красного цвета от флакона с мидриатиком) в оранжевый или коричневатый оттенки является плохим прогностическим признаком.
Если пациент находится в бессознательном состоянии, то единственным интегральным показателем функционирования зрительного анализатора оказывается состояние зрачков, в частности их форма и размеры. Корэктопия (деформация и смещение зрачка) характерна для проникающего ранения глазного яблока или контузионного разрыва склеры.
При оценке зрачка следует помнить, что его диаметр не находится в тесной корреляции с остротой зрения, так как она является функцией зрительного нерва (n. II), а величина зрачка определяется взаимодействием симпатических волокон глазной ветви тройничного нерва (n. VI) и парасимпатических волокон, находящихся в нижней ветви глазодвигательного нерва (n. III).
Как следствие, слепой глаз может иметь нормальный диаметр зрачка и, наоборот, максимальный мидриаз не препятствует высокой остроте зрения.
Далее анализируются зрачковые реакции на яркий свет. Афферентный зрачковый дефект, или зрачок Маркуса–Гунна (ослабленная прямая реакция зрачка на свет при сохраненной содружественной), является наглядным подтверждением травмы зрительного нерва. Суть симптома заключается в парадоксальной реакции зрачка при быстром перемещении светового потока со здорового глаза на больной, зрачок которого при освещении не только не сужается, а расширяется вследствие утраты прямой реакции из-за нарушения афферентной части дуги зрачкового рефлекса.
Следующим этапом является исследование центрального поля зрения с помощью сетки Амслера и ориентировочное определение границ поля зрения.
Затем с помощью фонарика осматривается передний отрезок. Завершается обследование офтальмоскопией глазного дна в условиях медикаментозного мидриаза. Фармакологическое воздействие на зрачок, так же как и детальное описание его исходного состояния, должно быть обязательно зафиксировано в истории болезни. Без крайней необходимости не стоит расширять зрачок контрлатерального здорового глаза.

Косвенные признаки перелома:
При тяжелом общем состоянии пациента и невозможности выполнить корональную КТ помогает трансантральная (через доступ к верхнечелюстной пазухе по Caldwell–Luc) эндоскопия нижней стенки глазницы, выполняемая в палате под местной анестезией и обладающая достаточной информативностью.
Лечение
Вначале консервативное и включает антибиотики, если перелом затрагивает верхнечелюстную пазуху. Пациента следует проинформировать о нежелательности сморкания. Последующее нацелено на предотвращение постоянной вертикальной диплопии и/или косметически неприемлемого анофтальма.
Существуют три фактора, определяющих риск данных осложнений:
Большинство переломов относят к одной из следующих категорий:
Показания к операции
«Взрывные» переломы, от которых пациент не страдает в функциональном или косметическом плане, не подлежат хирургическому лечению. Остальные случаи требуют оперативного пособия.
Показаниями к пластике нижней стенки глазницы в течение первых трех суток с момента травмы являются:
Более двух третей американских пластических хирургов выполняют подобное вмешательство в первые 14 суток, а половина британских хирургов оперируют перелом нижней стенки орбиты через 6–10 дней после травмы
Показанием к операции является каждый из перечисленных ниже критериев в отдельности или их сочетание:
Энуклеация с имплантацией орбитального вкладыша, выполняемая на фоне сопутствующего обширного дефекта нижней стенки глазницы, в обязательном порядке должна завершаться остеопластикой. В противном случае у пациента разовьется анофтальмический эно- и гипофтальм.
Лечение «взрывных» переломов нижней стенки глазницы должно быть ранним, одномоментным и исчерпывающим. Используемый в ходе операции имплантат должен удовлет-ворять ряду требований, к числу которых относятся:
В наибольшей степени этим требованиям соответствуют современные небиологические пористые материалы, к числу которых относятся пористый полиэтилен, коралловый гидроксиапатит и разработанный в Росии пористый поли-тетрафторэтилен, не уступающий по своим химическим и физико-механическим свойствам лучшим зарубежным аналогам.
Окончательная оценка результатов операции по таким критериям, как подвижность глазного яблока и его положение в орбите, наличие или отсутствие диплопии, выполняется не ранее, чем через 6 месяцев после вмешательства. КТ после операции при явной положительной динамике выполнять нецелесообразно, дабы избавить пациента от дополнительной лучевой нагрузки.
Интегральным показателем отдаленного успеха считается правильное положение глазного яблока в орбите и отсутствие диплопии.
Антибиотикотерапия
Отдельного рассмотрения заслуживает вопрос о необходимости антибиотикотерапии при «взрывных»переломах нижней стенки глазницы. Оказалось, что в литературе отсутствует описание стандартизированных схем приема антибиотиков данной категорией пациентов.
Учитывая отсутствие единого мнения по этому поводу, предлагают использовать общехирургические стандарты назначения антибиотиков в зависимости от типа раны:
Наличие трансплантата или инородного тела в ране (состояние после остеопластики дна орбиты) существенно повышает риск инфекции и также является показанием к профилактической антибиотикотерапии.
К какому же классу ран отнести «взрывной» перелом? Придаточные пазухи носа считаются стерильными. Поэтому взрывной перелом, соединяющийся с интактным синусом, можно рассматривать как чистую рану (I тип); если перелом развился на фоне синусита, то рана инфицирована (IV тип).
В идеале антибиотикотерапия должна быть начата в первые три часа после травмы, что зачастую нереально. Очень эффективной профилактикой гнойных осложнений является интраоперационная антибиотикотерапия, например, внутривенное введение 1,5 г цефуроксима (зинацефа), начатое уже в ходе вводной анестезии. Если вмешательство длится более четырех часов, то осуществляется повторная инфузия препарата.
В ходе вмешательства вводится 2 г амоксициллина или 600 мг клиндамицина. В первые двое суток послеоперационного периода каждые 8 часов в/в вводится 1 г амоксициллина или (при аллергии на пенициллин) 600 мг клиндамицина, затем на протяжении 5 дней трехкратная в/в инфузия
600 и 300 мг соответственно.
Не вызывает сомнений целесообразность включения в схему лечения орбитальных переломов глюкокортикоидов, так как они существенно ускоряют регресс отека мягких тканей глазницы и связанной с ним диплопии, не замедляя темпы остеогенеза.