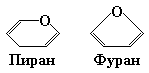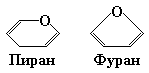пиранозная и фуранозная форма
Пиранозные и фуранозные кольцевые структуры моносахаридов



Моносахариды с числом атомов углерода 5 и более существуют в растворе преимущественно в виде замкнутых циклических структур, причем их карбонильная группа находится не в свободном состоянии, а образует ковалентную связь с одной из гидроксильных групп, связанных с атомом углерода основной цепи. Довольно часто встречающиеся шестичленные циклические формы моноз, например, D-глюкозы, из-за их сходства с шестичленным гетероциклическим соединением пираном (рис. 7.3) получили название пираноз. Устойчивые пиранозные кольца могут образовывать только альдозы, содержащие пять и более атомов углерода. Однако многие гексозы и большинство пентоз существуют также в виде циклических соединений с пятичленными кольцами. Из-за сходства таких колец с пятичленным гетероциклическим соединением фураном (рис. 7.3) их называют фуранозами.
Рис. 7.3. Структурные формулы шести- и пятичленного гетероциклов –
пирана и фурана, соответственно
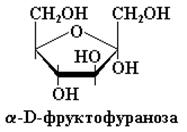
Для изображения циклических форм моносахаридов обычно пользуются так называемыми перспективными формулами Хеуорса. В таких формулах часть кольца, расположенную ближе к читателю, изображают жирными линиями (рис. 7.4). Примером может служить изображение шести- и пятичленного вариантов структуры глюкозы и фуранозной формы фруктозы с помощью перспективных формул Хеуорса (рис. 7.4).
а) 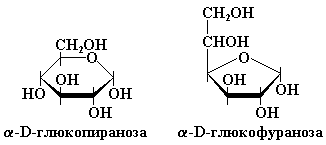
Рис. 7.4. Пиранозная и фуранозная перспективные формулы молекул D-глюкозы (а) и фуранозная форма молекулы D-фруктозы (б)
Пиранозные и фуранозные кольцевые структуры моносахаридов
Моносахариды с числом атомов углерода 5 и более существуют в растворе преимущественно в виде замкнутых циклических структур, причем их карбонильная группа находится не в свободном состоянии, а образует ковалентную связь с одной из гидроксильных групп, связанных с атомом углерода основной цепи. Довольно часто встречающиеся шестичленные циклические формы моноз, например, D-глюкозы, из-за их сходства с шестичленным гетероциклическим соединением пираном (рис. 7.3) получили название пираноз. Устойчивые пиранозные кольца могут образовывать только альдозы, содержащие пять и более атомов углерода. Однако многие гексозы и большинство пентоз существуют также в виде циклических соединений с пятичленными кольцами. Из-за сходства таких колец с пятичленным гетероциклическим соединением фураном (рис. 7.3) их называют фуранозами.
Рис. 7.3. Структурные формулы шести- и пятичленного гетероциклов –
пирана и фурана, соответственно
Для изображения циклических форм моносахаридов обычно пользуются так называемыми перспективными формулами Хеуорса. В таких формулах часть кольца, расположенную ближе к читателю, изображают жирными линиями (рис. 7.4). Примером может служить изображение шести- и пятичленного вариантов структуры глюкозы и фуранозной формы фруктозы с помощью перспективных формул Хеуорса (рис. 7.4).
а) 
Рис. 7.4. Пиранозная и фуранозная перспективные формулы молекул D-глюкозы (а) и фуранозная форма молекулы D-фруктозы (б)
Аномерия
Образование пиранозных колец, как, например, в случае молекулы D-глюкозы, обусловлено протеканием простой реакции между альдегидными и гидроксильными группами, что приводит к образованию полуацеталя. Полуацетали содержат асимметрический атом углерода и могут существовать в двух стереоизомерных формах. По своей природе D-глюкопираноза представляет собой внутримолекулярный полуацеталь, который образуется при взаимодействии ОН-группы у пятого атома углерода с альдегидобразующим первым углеродным атомом, который в результате циклизации становится асимметричным. Таким образом, D-глюкопираноза может существовать в виде двух дополнительных стереоизомеров, для обозначения которых используют буквы α и β. В итоге при циклизации число асимметрических атомов углерода в молекуле D-глюкозы становится на один больше. Стереоизомерные формы моносахаридов, отличающиеся друг от друга только конфигурацией полуацетального углеродного атома, такие как α-D-глюкоза и β-D-глюкоза, называются аномерами. Для того, чтобы различать эти изомеры пользуются простым правилом: если ОН-группа у аномерного атома углерода расположена под плоскостью кольца в формуле Хеуорса, то такая форма называется a-аномером, если такая ОН-группа находится над плоскостью кольца – b-аномером (рис. 7.5).
Рис. 7.5. Перспективные формулы Хеуорса α- и β-аномеров D-глюкопиранозы
Характерной особенностью явления аномерии является то, что в растворе моносахаридов постоянно протекает динамический процесс перехода от одной аномерной формы к другой, носящий название мутаротации. Это связано с тем, что циклическая форма моносахарида может раскрываться, и углевод какое-то время существует в форме линейной молекулы, при переходе вновь к циклической форме возможно образование уже другого аномера.
Следует иметь в виду, что в действительности шестичленное пиранозное кольцо не лежит в одной плоскости, как это кажется при использовании формул Хеуорса. У большинства сахаров оно имеет форму кресла, а у некоторых – форму лодки; эти конформации изображаются при помощи, так называемых, конформационных формул (рис. 7.6).


Рис. 7.6. Две изомерные формы пиранозного кольца (лодка и кресло),
изображенные при помощи конформационных формул
Биологические свойства и функции многих сложных углеводов, о которых будет сказано далее, определяются в значительной степени особенностями конформации образующих их простых шестиатомных сахаров.
Сложные углеводы
Сложные углеводы представляют собой группу углеводов с разнообразным строением и специфическими функциями. К ним относят олигосахариды и полисахариды. Под термином олигосахариды понимают определенную группу углеводов, построенных из разного числа моносахаридных звеньев от 2 до 15-20 (по мнению разных авторов, число моносахаридных остатков в олигосахаридах может достигать 30). Из сказанного выше следует, что простейшими олигосахаридами являются дисахариды, состоящие всего из двух остатков моносахаридов.
Дисахариды
Дисахариды состоят из двух ковалентно связанных друг с другом моносахаридов. У большинства дисахаридов химическая связь между моносахаридными единицами называется гликозидной связью. Она образуется между гидроксильной группой одного из сахаров и гидроксильной группой аномерного атома углерода другого сахара. Дисахариды, так же как и моносахариды, широко распространены в природе. Наиболее часто встречающимися дисахаридами являются: мальтоза, целлобиоза, лактоза, сахароза и трегалоза (см. таблицу в «Приложении 2»).
Мальтоза или солодовый сахар содержит два остатка D-глюкозы, соединенных гликозидной связью между аномерным атомом углерода одного остатка глюкозы и четвертым атомом углерода второго остатка. Аномерный атом углерода в гликозидной связи между двумя остатками D-глюкозы имеет a-конфигурацию, соответственно эта связь обозначается как a(1® 4).
Дисахарид целлобиоза также состоит из двух остатков D-глюкозы, но они соединены друг с другом b(1® 4)-связью.
Еще один дисахарид лактоза или молочный сахар, при гидролизе которой образуется D-галактоза и D-глюкоза, присутствует только в молоке. В молекуле лактозы галактоза и глюкоза связаны b(1®4) связью. Наличие в молекуле лактозы потенциально свободной карбонильной группы (в остатке глюкозы) делает ее восстанавливающим сахаром.
Сахароза (свекловичный или тростниковый сахар) – дисахарид, состоящий из глюкозы и фруктозы. В отличие от мальтозы, целлобиозы и лактозы у сахарозы нет свободного аномерного атома углерода, поскольку оба аномерных атома моносахаридных остатков связаны друг с другом a(1® 2)a-связью. По этой причине сахароза не является восстанавливающим дисахаридом.
Еще одним невосстанавливающим дисахаридом является трегалоза, часто встречающаяся в молодых грибах. Трегалоза состоит из двух остатков глюкозы, соединенных a(1® 1)-связью.
Олигосахариды
Другие олигосахариды, отличные от дисахаридов, устроены более сложно и реже встречаются в свободном виде. Наиболее простыми представителями являются мальтотриоза (состоит из трех остатков глюкозы), а также олигосахариды бобовых растений раффиноза (состоит из сахарозы и присоединенного к ней остатка галактозы) и стахиоза (отличается от раффинозы присутствием еще одного остатка галактозы).Важную группу более высокомолекулярных олигосахаридов составляют олигосахариды женского молока, например, лакто-N-фукопентаоза, которые играют важную роль в формировании кишечной флоры у новорожденных. Большая часть олигосахаридов не встречается в свободной форме, а является составной частью гликопротеидов в виде боковых цепей, присоединенных к полипептидным цепям.
Полисахариды
В природе большинство углеводов представлено полисахаридами с высокой молекулярной массой. Биологическая роль ряда полисахаридов состоит в том, что одни обеспечивают накопление моносахаридов, другие служат структурными элементами клеточных стенок и соединительной ткани. Полисахариды отличаются друг от друга, как природой составляющих их моносахаридных остатков, так и длиной и степенью ветвления цепей. Их разделяют на два типа: гомополисахариды, состоящие из остатков одного и того же моносахарида, и гетерополисахариды, содержащие остатки двух или большего числа видов моносахаридов. Полисахариды могут иметь линейную или разветвленную структуру.
Гомополисахариды
К числу наиболее известных и важных с биологической точки зрения гомополисахаридов относят крахмал, гликоген, целлюлозу, пектины и хитин. Важнейшим резервным полисахаридом в клетках растений является крахмал, а в клетках животных – гликоген. Крахмал представляет собой смесь двух полимеров глюкозы:
| a-амилозы (15-20% от общего количества) и амилопектина (80‑85%). a-амилоза имеет неразветвленную спиральную структуру, в которой остатки глюкозы соединены a(1® 4)-связями (рис. 7.7). |  Рис. 7.7. Структура фрагмента a-амилозы Рис. 7.7. Структура фрагмента a-амилозы |
| Молекулярная масса цепей a-амилозы колеблется от нескольких тысяч до 500 000. Амилопектин также имеет высокую молекулярную массу, но в отличие от a-амилозы его цепи сильно разветвлены (одно ответвление примерно на каждые 20 остатков глюкозы). В неразветвленных участках остатки глюкозы соединены a(1 ® 4)-связями, а в точках ветвления – связями a(1 ® 6). |  Рис. 7.8. Фрагмент структуры амилопектина. В точках ветвления возникает a(1® 6)-связь Рис. 7.8. Фрагмент структуры амилопектина. В точках ветвления возникает a(1® 6)-связь |
Гликоген – основной резервный полисахарид в клетках животных. Основная масса гликогена накапливается у животных в клетках печени и клетках скелетной мускулатуры. Подобно амилопектину, гликоген является разветвленным полисахаридом, состоящим из остатков D-глюкозы, связанных друг с другом a(1® 4)-связями, но по сравнению с амилопектином он значительно более разветвлен (примерно одна точка ветвления на 10 остатков D‑глюкозы) и компактен. В местах ветвления образуются a(1® 6)-связи.
Декстринами называют вещества, образующиеся при гидролизе крахмала под действием амилаз. Амилазы расщепляют только a(1® 4)-связи. Устойчивое по отношению к амилазам «ядро» амилопектина, содержащее большое число a(1® 6)-связей называют остаточным декстрином.
Целлюлоза –линейный, неразветвленный гомополисахарид, состоящий из 10 000 и более остатков D-глюкозы. Она нерастворима в обычных растворителях и в воде и построена из a-D-глюкопиранозных звеньев, соединенных b(1® 4) связями, образующих длинные вытянутые цепи, стабилизированные поперечными водородными связями. Если наиболее распространенными внутриклеточными биополимерами следует считать белки, то целлюлоза, бесспорно, это не только самый распространенный внеклеточный структурный полисахарид в растительном мире, но и вообще самый распространенный в природе биополимер.
Рис. 7.9. Фрагмент структуры молекулы целлюлозы. Полимерные цепи целлюлозы располагаются параллельно и соединяются водородными связями
Многие млекопитающие, в том числе человек, не способны переваривать целлюлозу, так как их пищеварительная система не содержит ферментов, расщепляющих b-связи. В кишечнике жвачных и многих других травоядных животных присутствуют микроорганизмы, способные расщеплять b-связи, и для этих животных целлюлоза является важным источником пищевых калорий. В толстом кишечнике человека также содержится ряд штаммов бактерий, способных воздействовать на целлюлозу, но их количество мало, и с их помощью человек переваривает только незначительную часть поступающей в его организм целлюлозы.
В основе пектиновых соединений лежат, так называемые пектовые кислоты, которые построены, в основном, из остатков a-D-галактуроновой кислоты, связанных a(1®4)-связью.
Рис. 7.10. Фрагмент структуры молекулы пектина. Полимерные цепи пектина образованы, связанными друг с другом остатками a-D-галактуроновой кислоты
В пектине и протопектине разное число атомов водорода карбоксильных групп остатков a-D-галактуроновой кислоты (выделены звездочками) замещается метильными группами (–СН3). Собственно пектин содержится в значительном количестве в растительных соках. Протопектин является обычным компонентом клеточной стенки и менее растворим, чем пектин.
Хитин, наряду с целлюлозой и пектинами, также является одним из важнейших полисахаридов, выполняющих структурную функцию. Он входит в состав клеточных стенок грибов и участвует в формировании твердого наружного покрова (экзоскелета) насекомых и ракообразных. Мономером хитина является N‑ацетилглюкозамин, молекулы которого связаны друг с другом b(1®4)‑гликозидной связью.
Рис. 7.11. Фрагмент структуры молекулы хитина. N-ацетил-D-глюкозамин является основным строительным блоком хитина и многих других структурных полисахаридов
Группа гетерополисахаридов будет рассмотрена нами в теоретической части к следующей лабораторной работе.
Пиранозные и фуранозные кольцевые структуры моносахаридов
Моносахариды с числом атомов углерода 5 и более существуют в растворе преимущественно в виде замкнутых циклических структур, причем их карбонильная группа находится не в свободном состоянии, а образует ковалентную связь с одной из гидроксильных групп, связанных с атомом углерода основной цепи. Довольно часто встречающиеся шестичленные циклические формы моноз, например, D-глюкозы, из-за их сходства с шестичленным гетероциклическим соединением пираном (рис. 7.3) получили название пираноз. Устойчивые пиранозные кольца могут образовывать только альдозы, содержащие пять и более атомов углерода. Однако многие гексозы и большинство пентоз существуют также в виде циклических соединений с пятичленными кольцами. Из-за сходства таких колец с пятичленным гетероциклическим соединением фураном (рис. 7.3) их называют фуранозами.
Рис. 7.3. Структурные формулы шести- и пятичленного гетероциклов –
пирана и фурана, соответственно
Для изображения циклических форм моносахаридов обычно пользуются так называемыми перспективными формулами Хеуорса. В таких формулах часть кольца, расположенную ближе к читателю, изображают жирными линиями (рис. 7.4). Примером может служить изображение шести- и пятичленного вариантов структуры глюкозы и фуранозной формы фруктозы с помощью перспективных формул Хеуорса (рис. 7.4).
а) 
Рис. 7.4. Пиранозная и фуранозная перспективные формулы молекул D-глюкозы (а) и фуранозная форма молекулы D-фруктозы (б)
Пиранозная и фуранозная форма
Создано в интеллектуальной издательской системе Ridero
Биохимия – это наука о структуре молекул, входящих в состав живых организмов, а также о процессах их превращений внутри организма или клетки.
Термин «биохимия» эпизодически употреблялся с середины XIX века, в классическом смысле он был предложен и введён в научную среду в 1903 году немецким химиком Карлом Нейбергом.
Биохимия является продолжением органической химии. Собственно многие молекулы (спирты, гетероциклы и другие) являются объектами исследований специалистами в области органической химии.
Одной из важных целей биохимии является изучение структуры, физико-химических свойств и функций молекул, которые входят в состав живых объектов. Многие молекулы являются объектами исследования и биохимиков и органических химиков. Кроме того, изучение молекул, входящих в состав живых организмов показало, что этих молекул огромное множество, прежде всего белков. И их свойства и функции также очень многообразны. Это с одной стороны увеличивает объем изучаемой информации, а с другой приводит к тому, что для освоения новых данных остается меньше времени. Именно поэтому биохимики, можно сказать, вынужденно ограничились изучением тех групп соединений, которые выявлены только в живых объектах, оставив остальные группы соединений органическим химикам.
Именно так появился раздел биохимии, который можно назвать «Структурная биохимия». Структурная биохимия изучает структуру, физические и химические свойства, а также функции исследуемых молекул. Как показал анализ, только для живых организмов характерны молекулы, относящиеся к четырем классам: углеводы (моносахариды и их полимеры полисахариды), нуклеотиды и их полимеры нуклеиновые кислоты, аминокислоты и их полимеры белки, липиды, у которых не выявлены полимерные формы, зато существуют надмолекулярные структуры, которые называют мембранами.
В данном учебнике изучается «Структурная биохимия», в которой рассматриваются четыре класса соединений, характерных только для биологических объектов. В учебнике изложены: классификация молекул и их структура в в зависимости от класса, физико-химические свойства и функции данных соединений. Также рассмотрены отдельные свойства молекул, определяющие их особые свойства, например особенности структуры, свойств и функционирования мембран, как особенных свойств и функций липидов и белков, их образующих.
Углеводы широко представлены в растениях и животных, где они выполняют как структурные, так и метаболические функции. В растениях в процессе фотосинтеза из углекислого газа и воды синтезируется глюкоза, которая далее запасается в виде крахмала или превращается в целлюлозу – структурную основу растений. Животные способны синтезировать ряд углеводов из жиров и белков, но большая часть углеводов поступает с пищей растительного происхождения.
Углеводы – это альдегидные или кетонные производные полиатомных (содержащих более одной ОН-группы) спиртов или соединения, при гидролизе которых образуются эти производные.
Их можно классифицировать следующим образом:
Моносахариды – углеводы, которые не могут быть гидролизованы до более простых форм. Их можно подразделить на триозы, тетрозы, пентозы, гексозы, гептозы и октозы в зависимости от числа содержащихся в их молекуле атомов углерода; их можно разделить также на альдозы и кетозы в зависимости от присутствия альдегидной или кетонной группы.
Дисахариды при гидролизе дают две молекулы моносахарида (одинаковых или различных).
Олигосахариды при гидролизе дают 3—6 моносахаридов или, что чаще, полисахариды, в состав которых входит несколько десятков моносахаридных остатков.
Полисахариды дают при гидролизе более 6 молекул моносахаридов. Они могут быть линейными или разветвленными. Если полисахарид состоит из одинаковых мономеров, то их их называют гомополисахаридами, если из разных, то гетерополисахаридами. Также следует отметить, что большая часть полисахаридов содержит более тысячи мономерных остатков. Примерами служат крахмал и декстрины.
Моносахариды – углеводы, которые не могут быть гидролизованы до более простых форм. Их можно подразделить на триозы, тетрозы, пентозы, гексозы, гептозы и октозы в зависимости от числа содержащихся в их молекуле атомов углерода; их можно разделить также на альдозы и кетозы в зависимости от присутствия альдегидной или кетонной группы. Отсчет атомов углерода начинают либо от входящего в состав альдегидной группы (первый атом), либо от ближайшего к кетонной группе.
Стереоизомерия или D и L изоформы:
В многих органических молекулах есть атом углерода с которым связаны четыре различные группировки, и такую молекулу можно представить как молекулу метана, в виде тетраэдра, в верхушках которого располагаются группировки. Такой атом называется хиральным, в случае моносахаридов принадлежность к D или L форме определяется расположением гидроксильной (ОН) группировки, относительно хирального атома углерода. Если ОН-группа слева, то это L-форма, если справа, то D-форма. Но полностью этому правилу соответствует только глицероальдегид, имеющий только один хиральный атом (Рисунок 1 А). Во всех других углеводах хиральных атомов несколько, и каждый из них может быть признан для определения принадлежности к одной из форм стереоизомеров. Было принято решение признать атомом, определяющим стереоизомерию, последний хиральный атом молекулы (предпоследний атом углерода в молекуле). Но изменение положения гидроксильной группы только у данного атома углерода не приведет к образованию полностью зеркального отображения, что является основным условием для существования двух форм стереоизомеров. Поэтому появилось понятие ряда углеводов, то есть все углеводы могут быть выведены или синтезированы из минимального углевода (триозы), и, следовательно, эта триоза является предшественником или родительским соединением, так как единственная триоза, обладающая оптическими свойствами – глицероальдегид, то именно эта молекула является родительским соединением для всех остальных. Принадлежность к одному их стреоизомеров родительского соединения, определяет принадлежность к D или L-форме всех остальных моносахаридов, синтезируемых из данного родительского соединения (Рисунок 2). В ходе синтеза углеводов с числом атомов больше чем три (глицероальдегид), присоединение каждого следующего атома углерода
Рисунок 1. Структурные формулы стереоизомеров углеводов, * – отмечены асимметрические (хиральные) атомы. А – глицероальдегид * – отмечен асимметрический атом, определяющий принадлежность к D или L форме, Б – стереоизомеры глюкозы, крупной * отмечены асимметрические атомы углерода, определяющие принадлежность к стереоизомерам
происходит по альдегидной группе, и, следовательно, хиральный атом родительского соединения оказывается все дальше от первого атома углерода, то есть остается последним асимметричным или просто предпоследним атомом углерода (рисунок 2). Присутствие асимметрических атомов углерода является причиной оптической активности соединения. Если пучок плоскополяризованного света проходит через раствор оптического изомера, плоскость поляризации света поворачивается либо вправо (правовращающий изомер, +), либо влево (левовращающий изомер, – ). Соединение обозначают D ( – ), D (+), L ( – ) или L (+); это обозначение показывает наличие структурного родства с D- или L- глицеральдегидом, но не обязательно тот же знак оптического вращения. Например, природной формой фруктозы является D ( – ) – изомер. Если D- и L-изомеры присутствуют в равных количествах, их смесь не проявляет оптической активности – активности изомеров компенсируют одна другую. Такие смеси называют рацемическими (или DL-смесями). Соединения, получаемые синтетическим путем, оказываются рацемическими, поскольку в этом случае вероятности образования каждого из изомеров одинаковы.