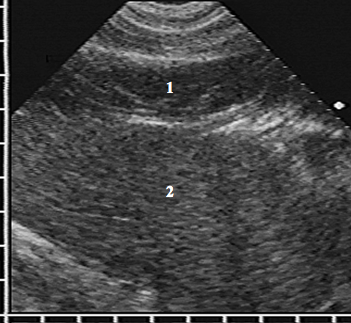
плевральные наслоения в правом кардиодиафрагмальном углу
Заболевания плевры: диагностика и лечение
Заболевания плевры часто встречаются в общей практике и могут отражать широкий диапазон лежащих в их основе патологических состояний, затрагивающих легкие, грудную стенку, а также системных болезней. Самое распространенное их проявление
Заболевания плевры часто встречаются в общей практике и могут отражать широкий диапазон лежащих в их основе патологических состояний, затрагивающих легкие, грудную стенку, а также системных болезней. Самое распространенное их проявление заключается в образовании плеврального выпота, и у подавляющего большинства таких больных необходимы рентгенологическое подтверждение и дальнейшее обследование. Последние достижения, касающиеся методов получения изображения органов грудной клетки, терапии и хирургии, позволили усовершенствовать диагностику и лечение больных с патологией плевры.
Плевра дает грудной клетке возможность придавать легким необходимую форму и приводить их в движение с минимальными затратами энергии. Для чего два плевральных листка (париетальный и висцеральный) должны скользить один по другому — этому процессу способствует небольшое количество (0,3 мл/кг) жидкости.
Плевральная жидкость фильтруется из мелких сосудов париетальной плевры в плевральную полость и реабсорбируется лимфатическими сосудами этого же листка. Экспериментальные данные показывают, что объем и состав плевральной жидкости в норме очень стабильны, и выпот возникает только в тех случаях, если скорость фильтрации превышает максимальный отток лимфы либо нарушено обратное всасывание [1].
Плевральный выпот
Плевральные выпоты традиционно подразделяются на транссудаты (общий белок 30 г/л). В промежуточных случаях (а именно, когда содержание протеина составляет 25–35 г/л) разграничить экссудат и транссудат помогает определение содержания в плевральной жидкости лактатдегидрогеназы (ЛДГ) и градиента альбумина между сывороткой и плевральной жидкостью.
Наиболее часто встречающиеся причины и характерные признаки плевральных выпотов приведены в таблицах 1 и 2. Их дифференциация важна потому, что «низкобелковые» выпоты (транссудаты) не требуют дальнейших диагностических мероприятий; необходимо лишь лечение вызвавшей их патологии, в то время как при обнаружении плеврального экссудата, безусловно, нужна дополнительная диагностика.
Выпоты могут быть односторонними или двусторонними. Последние часто выявляются при сердечной недостаточности, но могут также возникать при гипопротеинемических состояниях и при коллагенозах с поражением сосудов. Имеют очень большое значение тщательный сбор анамнеза, включая профессию, данные о путешествиях за границу и о факторах риска тромбоэмболии, а также внимательное полноценное физикальное обследование.
При физикальном обследовании обнаруживается ограничение дыхательных движений грудной клетки, «каменная» тупость при перкуссии, приглушение дыхания при аускультации и часто — зона бронхиального дыхания сверху от уровня жидкости.
Небольшие выпоты следует дифференцировать с утолщением плевры. Помочь в этом может выполнение рентгенограммы в положении лежа (при этом жидкость движется под действием силы тяжести), а также ультразвуковое исследование (УЗИ) или рентгеновская компьютерная томография (КТ).
И УЗИ, и КТ являются ценными методами, которые все чаще используются для дифференциации между плевральной жидкостью, «окутанным» легким (плевральными бляшками, обычно возникающими при воздействии асбеста) и опухолью. Эти методы позволяют также выяснить, является ли плевральная жидкость осумкованной, и наметить оптимальное место для плевральной пункции и биопсии.
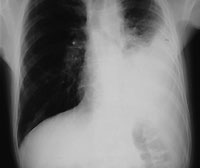 |
| Рисунок 1. Рентгенограмма органов грудной клетки: виден расширенный пищевод с уровнем жидкости и левосторонний плевральный выпот. Эти изменения были расценены как вторичная эмпиема, возникшая на фоне аспирационной пневмонии |
Плевральная пункция с аспирацией и биопсия показаны всем больным с выпотом, при этом удается получить гораздо больше диагностической информации, чем только при аспирации, и избежать проведения повторной инвазивной процедуры (см. рис. 1).
Другие исследования, помогающие в установлении диагноза, включают повторную рентгенографию органов грудной клетки после аспирации для выявления лежащей в основе выпота патологии легких, КТ, изотопное сканирование легких (с определением соотношения вентиляции и перфузии), внутрикожные пробы с туберкулином, серологические исследования на ревматоидные и антиядерные факторы.
Если вышеперечисленные методы не позволяют выявить причину возникновения плевральных выпотов, проводится торакоскопия с помощью видеотехники. Она позволяет не только осмотреть плевру, но также выявить опухолевые узлы и осуществить прицельную биопсию. Эта процедура наиболее ценна для диагностики мезотелиомы. Как бы то ни было, у 20% больных с экссудативными плевральными выпотами посредством обычных исследований не удается диагностировать причину развития данного состояния.
Лечение патологии, провоцирующей развитие плеврального выпота, например сердечной недостаточности или тромбоэмболии легочных артерий, часто приводит к его исчезновению. Некоторые состояния, включая эмпиему и злокачественные опухоли, требуют особых мер, о которых речь пойдет ниже.
Парапневмонические выпоты и эмпиема
Приблизительно у 40% больных с бактериальными пневмониями развивается сопутствующий плевральный выпот [11]; в таких случаях необходимо провести плевральную пункцию, чтобы удостовериться, что нет эмпиемы, и предотвратить либо уменьшить степень последующего утолщения плевры.
Однако у 15% пациентов парапневмонические выпоты вторично инфицируются, развивается эмпиема, то есть образуется гной в плевральной полости (см. рис. 2).
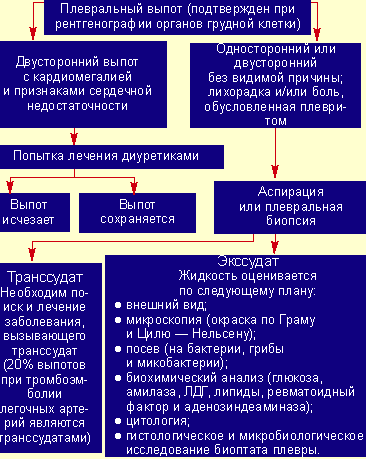 |
| Рисунок 2. Исследования при плевральном выпоте |
Другие причины эмпиемы включают хирургические вмешательства (20%), травмы (5%), перфорации пищевода (5%) и субдиафрагмальные инфекции (1%) [12].
 |
| Таблица 3. Микроорганизмы: возбудители эмпиемы |
При эмпиемах большая часть высеваемых культур представлена аэробными микроорганизмами. Анаэробные же бактерии высеваются в 15% случаев эмпием, обычно являющихся осложнением аспирационных пневмоний; остальные случаи обусловлены разнообразными другими микроорганизмами (см. табл. 3). Если до плевральной пункции назначались антибиотики, посевы часто не дают роста.
Диагноз подтверждается на основании рентгенологических признаков осумкованного плеврита или в случае обнаружения гноя в плевральном пунктате (см. табл. 2).
Кроме того, под контролем УЗИ или КТ следует наладить дренаж из наиболее низкой части эмпиемы и соединить его с подводным клапанным механизмом. В прошлом рекомендовалось использовать дренажи относительно большого диаметра, однако сегодня применение более узких трубок признано эффективным при меньшей травматичности для пациентов.
Рекомендации относительно целесообразности применения фибринолитиков основаны на результатах небольших неконтролированных исследований, согласно которым частота ликвидации спаек составила 60–95% [13, 14], а потребность в хирургических вмешательствах значительно уменьшилась. Тем, что до сих пор не проведено контролированных исследований, объясняется некоторая неопределенность относительно того, когда, как долго и в каких дозах следует применять фибринолитические препараты. В настоящее время под эгидой Совета медицинских исследований (Medical Research Council) проводится работа, результаты которой позволят ответить на эти вопросы.
Если в результате дренирования из межреберного доступа (с фибринолитиками или без них) не удается добиться адекватного отведения жидкости, если эмпиема сохраняется, организуется и сопровождается утолщением плевры и сдавлением легкого, то показано хирургическое вмешательство.
Торакоскопия обычно успешна на ранних стадиях заболевания, но при обширных плевральных спайках может окончиться неудачей. В этих случаях показана торакотомия и декортикация. Хотя такое хирургическое вмешательство высокоэффективно в отношении лечения эмпиемы (>90%), с ним связан существенный операционный риск, особенно у ослабленных больных.
Открытый дренаж, при котором требуется резекция ребра, — довольно малопривлекательная процедура, она проводится только в том случае, когда больной не может перенести более инвазивную операцию.
Без лечения эмпиема может прорваться наружу через грудную стенку («прободающая» эмпиема) или в бронхиальное дерево с образованием бронхоплеврального свища либо вызвать обширный плевральный фиброз, который ограничивает подвижность легких. К редким осложнениям относятся абсцесс головного мозга и амилоидоз, может также возникнуть деформация фаланг типа «барабанных палочек».
Поражение плевры при злокачественных новообразованиях
Рак легких — это наиболее частая причина возникновения злокачественного плеврального выпота, особенно у курильщиков. Лимфома может возникнуть в любом возрасте и составляет 10% от всех злокачественных выпотов. Метастазы в плевру наиболее часто встречаются при раках молочной железы (25%), яичников (5%) или желудочно-кишечного тракта (2%) (см. рис. 3). В 7% случаев первичная опухоль остается неизвестной.
Важно понимать, что при первичном бронхогенном раке наличие плеврального выпота не обязательно исключает операбельность. У 5% таких больных выпот развивается вследствие обструкции бронхов и дистальной инфекции, и заболевание остается потенциально излечимым.
Поэтому, когда встает вопрос о возможности проведения операции, чрезвычайно важно установить причину плеврального выпота.
Выпоты, обусловленные злокачественной инфильтрацией плевры, обычно быстро накапливаются вновь. Для того чтобы избежать необходимости проведения повторных плевральных пункций, выпот необходимо полностью («насухо») удалить при первичном дренировании через межреберную трубку, а плевральная полость должна быть облитерирована путем введения вызывающих воспаление препаратов, например талька, тетрациклина или блеомицина, при этом в конце концов развивается плевродез. В настоящее время наиболее эффективным средством в этом отношении считается тальк: при его применении успех достигается у 90% больных [17].
Однако эффективный плевродез приводит к значительному болевому синдрому в послеоперационном периоде, который часто требует применения сильных анальгетиков; рекомендуется при этом избегать нестероидных противовоспалительных препаратов, поскольку они снижают эффективность операции.
Непосредственная абразия плевры во время операции с плеврэктомией или без нее применяется у молодых пациентов с довольно длительным сроком выживания, у которых не удался химический плевродез.
При обширном, мучительном для больного плевральном выпоте и неэффективности химического плевродеза альтернативным методом является установка плевроперитонеального шунта по Denver. Удивительно то, что при такой операции не наблюдается обсеменения опухоли по брюшине, однако в реальную проблему могут вылиться развитие инфекции и окклюзия шунта.
Патология плевры, связанная с асбестом
В 2002 году в Великобритании смертность от мезотелиомы, согласно прогнозам, достигнет пика в 2020 году и составит 3000 [5].
В большинстве стран среди заболевших преобладают мужчины, что подтверждает ведущую роль профессионального фактора в развитии этого заболевания.
Возраст на момент контакта с асбестом, а также продолжительность и интенсивность этого контакта тоже имеют важное значение. Наибольшему риску подвергаются представители профессий, требующих непосредственного контакта с асбестом, особенно рабочие строительной индустрии, в то время как для людей, проживающих в зданиях, содержащих асбест, риск гораздо ниже.
Заболевание проявляется болями в груди и плевральным выпотом, который имеет кровянистую окраску и вызывает одышку. В Великобритании пациенты с этой болезнью имеют право на компенсацию, как и при других заболеваниях и увечьях, полученных на производстве (см. табл. 4).
Во всех случаях необходимо гистологическое исследование, в ходе которого используются либо материал, получаемый при аспирации плеврального содержимого и биопсии под контролем УЗИ (что позволяет подтвердить диагноз у 39% таких больных), либо ткань, взятая при торакоскопии (диагноз подтверждается у 98% пациентов) [6]. Торакоскопия также позволяет определить степень распространенности опухоли в плевральной полости, поскольку очень ограниченное заболевание на ранней стадии может быть излечено хирургическим путем, в то время как при поражении висцеральной плевры прогноз неблагоприятный.
После таких диагностических вмешательств часто наблюдается обсеменение опухоли по плевре, профилактика этого состояния предполагает облучение области биопсии или дренажа.
Большинство пациентов впервые поступают к врачу уже с неоперабельной опухолью. В такой ситуации ни один из методов не обеспечивает возможности излечения больного, однако сегодня проводятся попытки применения радикальной операции, фотодинамической терапии, внутриплевральной системной химиотерапии и лучевой терапии. И хотя генная терапия пока не приносит успеха, иммунотерапия может признана перспективной. Неблагоприятными диагностическими факторами являются: низкие функциональные резервы сердечно-сосудистой и дыхательной систем, лейкоцитоз, перерождение в саркому (по данным гистологического исследования) и мужской пол. В течение одного года выживают от 12 до 40% больных, в зависимости от перечисленных прогностических факторов.
Спонтанный пневмоторакс
Спонтанный пневмоторакс может быть первичным (без явного предшествующего заболевания легких) или вторичным (когда имеются признаки легочного заболевания, например легочного фиброза). К малораспространенным причинам пневмоторакса относятся: инфаркт легкого, рак легкого, ревматоидные узелки или абсцесс легкого с образованием полости. Субплевральные эмфизематозные буллы, обычно расположенные в области верхушек легкого, или плевральные буллы обнаруживаются у 48–79% больных с якобы спонтанным первичным пневмотораксом [18].
Среди курильщиков частота пневмоторакса гораздо выше. Относительный риск развития пневмоторакса в девять раз выше у женщин-курильщиц и в 22 раза — у курящих мужчин. Более того, выявлена зависимость «доза — эффект» между числом выкуренных за день сигарет и частотой пневмоторакса [19].
В диагностике небольших по объему, преимущественно верхушечных, пневмотораксов могут помочь снимки на выдохе, которые, однако, используются редко. Следует различать большие эмфизематозные буллы и пневмоторакс.
Алгоритм лечения представлен на рисунке 5. Чрескожная аспирация — это простая, хорошо переносимая, альтернативная по отношению к межреберному дренажу по трубке процедура, в большинстве случаев ей следует отдавать предпочтение. Аспирация позволяет достичь удовлетворительного расправления легкого у 70% больных с нормальной легочной функцией и только у 35% пациентов с хроническими заболеваниями легких [20].
Средняя частота рецидивов после единственного первичного спонтанного пневмоторакса, независимо от первичного лечения, составляет 30%, большинство их возникает в первые 6–24 месяцев.
Пациентов следует предупреждать о возможности развития повторных пневмотораксов: в частности, им не рекомендуется летать на самолетах в течение шести недель после полного разрешения пневмоторакса. Операция обычно требуется в тех случаях, когда в течение недели наблюдается упорное накопление воздуха.
Рецидивирующий пневмоторакс, особенно если поражены оба легких, следует лечить либо путем химического плевродеза или, что более предпочтительно, с помощью париетальной плеврэктомии либо плевральной абразии.
Последние из названных операций можно проводить с помощью торакоскопии под контролем видеоизображения, которая позволяет проследить за ходом процедуры с помощью монитора, сократить пребывание в стационаре и ускорить возвращение пациента к нормальному образу жизни. Хирургическое лечение позволяет уменьшить частоту рецидивов до 4% в сравнении с 8% после плевродеза тальком [22].
В представленной статье мы рассказали о нескольких аспектах, связанных с заболеваниями плевры, в том числе о последних достижениях в этой области. Плевральный выпот — это самое частое проявление патологии плевры, требующее тщательного обследования. Если после обычных методов исследования причина заболевания остается неясной, нужно предпринять все необходимые меры для исключения тромбоэмболии легочных артерий, туберкулеза, реакции на введение лекарств и поддиафрагмальных патологических процессов.
Хелен Парфри, бакалавр медицины, бакалавр химии, член Королевской коллегии врачей
Больница Западного Саффолка
Эдвин Р. Чайлверс, бакалавр медицины, бакалавр естественных наук, доктор философии, профессор
Кембриджский университет, Школа клинической медицины, отделение терапии больницы Адденбрука и Папворта
Ультразвуковая дифференциальная диагностика патологии правого кардиодиафрагмального угла
1 Нижегородская государственная медицинская академия, 603005, г. Нижний Новгород, пл. Минина, д. 10/1
2 Приволжский окружной медицинский центр ФМБА России, 603109, г. Нижний Новгород, ул. Ильинская, д. 14
Сафонов Дмитрий Владимирович — доктор медицинских наук, профессор кафедры лучевой диагностики, тел. +7-910-795-59-25, e-mail: safonovdv@inbox.ru 1
Павлунин Александр Васильевич — доктор медицинских наук, профессор, заведующий кафедрой фтизиатрии, тел.+7-903-605-03-49, e-mail:pavluninav@jandex.ru 1
Сафонова Татьяна Дмитриевна — студентка лечебного факультета, тел.+7-910-395-50-44, e-mail:tanja-94@inbox.ru 1
Муртазалиева Марина Саидовна — кандидат медицинских наук, заведующая амбулаторным центром трансплантологии и гепатологии, тел.+7-910-891-53-73, e-mail:mar93832607@jandex.ru 2
С цельюразработки дифференциальной ультразвуковой диагностики патологических образований правого кардиодиафрагмального угла обследованы 156 больных. Проведен сравнительный анализ эхокартины абдомино-медиастинальных липом (АМЛ) и целомических кист перикарда (ЦКП). Предложена оригинальная методика их дифференциальной ультразвуковой диагностики. АМЛ имела вид дополнительного образования треугольной формы с неоднородной эхоструктурой за счет множественных коротких линейных сигналов на гипоэхогенном фоне, при продольном сканировании прослеживался ее переход в предбрюшинную клетчатку в виде узкой ножки. ЦКП лоцировалась как овальное образование с однородным анэхогенным содержимым, ограниченным тонкой эхогенной капсулой и без связи с передней брюшной стенкой. Ультразвуковая дифференцировка АМЛ и ЦКП предоставляет хирургу возможность целенаправленно выбирать тактику лечения и определять способ оперативного лечения.
Ключевые слова: ультразвуковое исследование, правый кардиодиафрагмальный угол, абдоминомедиастинальная липома, целомическая киста перикарда, грыжа щели Ларрея.
1 Nizhny Novgorod State Medical Academy, 10/1 Minina square, Nizhny Novgorod, Russian Federation 603005
2 The Volga District Medical Center of Federal Medical and Biological Agency of Russia, 14 Ilyinskaya St., Nizhny Novgorod, Russian Federation 603109
Ultrasonic differential diagnosis of pathology of the right cardiodiaphragmatic angle
SaphonovD.V. — D. Med. Sc., Professor of the Department ofX-ray Diagnostics, tel. +7-910-795-59-25, e-mail: safonovdv@inbox.ru 1
Pavlunin A.V. — D. Med. Sc., Professor, Head of the Department of Phthisiatry, tel.+7-903-605-03-49, e-mail:pavluninav@jandex.ru 1
Saphonova T.D. — Studentof Medical Faculty, tel.+7-910-395-50-44, e-mail:tanja-94@inbox.ru 1
Murtazalieva M.S. — Candidate of Medical Science, HeadoftheOutpatientCenterofTransplantationandHepatology, tel.+7-910-891-53-73, e-mail:mar93832607@jandex.ru 2
In order to develop the differential ultrasound diagnosis of pathologic formations of the right cardiodiaphragmatic angle were examined 156 patients. The comparative analysis of echopicture of abdomino-mediastinal lipoma and coelomic pericardial cysts was made. An original method of differential ultrasound diagnosis was offered. AML had an appearance of a formation of triangular shape with heterogeneous echostructure due to multiple short linear signals at the hypoechoic background, in the course of longitudinal scanning is traced its transition into the preperitoneal tissue in the form of a narrow peduncle. Coelomic pericardial cyst is an oval formation with uniform anechoic content, limited by thin echogenic capsule and with no relation to the anterior abdominal wall. Ultrasound differentiation of abdomino-mediastinal lipoma and coelomic pericardial cyst allows the surgeon to choose the therapeutic approach and to determine the manner of surgical treatment.
Key words: ultrasound investigation, right cardiodiaphragmatic angle, abdominomediastinal lipoma, coelomic pericardial cyst, hernia, Larrey’s cleft.
Под кардиодиафрагмальным углом понимают пространство в переднем нижнем средостении, ограниченное спереди грудной стенкой, медиально — перикардом, снизу — мышечной частью купола диафрагмы, в которой выделяют грудино-реберный треугольник, или треугольник Ларрея. Он представляет собой слабое место диафрагмы, где мышечные пучки выражены слабо, а париетальную брюшину от диафрагмальной плевры отделяет лишь тонкий слой жировой клетчатки [1]. Задней границей условно считают диафрагмальный нерв и перикардодиафрагмальные сосуды, проходящие вдоль перикарда. В норме правый кардиодиафрагмальный угол занимает воздушная легочная ткань. Каудальнее нижнего края легкого распространяется передний ребернодиафрагмальный плевральный синус с незначительным количеством субплевральной жировой клетчатки.
Топографо-анатомические особенности правого кардиодиафрагмального угла определяют разнообразие патологических образований, возникающих в этой зоне, которые по структуре можно разделить на тканевые и жидкостные. К первым относятся абдоминомедиастинальные липомы (АМЛ) и встречающиеся значительно реже грыжи щели Ларрея (ГЩЛ); ко вторым — целомические кисты перикарда (ЦКП).
Патоморфологически ЦКП представляет собой тонкостенную полость с жидкостью, расположенную вплотную к сердцу обособленно от полости перикарда или сообщающуюся с ней. АМЛ по существу является ложной грыжей, состоящей только из предбрюшинной клетчатки, проникшей через щель Ларрея — Морганьи в правый кардиодиафрагмальный угол (рис. 1).
Рисунок 1.
Образование абдоминомедиастинальной липомы (схема)
1 — сердце; 2 — легочная ткань; 3 — диафрагма; 4 — абдоминомедиастинальная грыжа; 5 — плевральная складка; 6 — грудина; 7 — печень; 8 — белая линия живота; 9 — брюшина [Таgliacozzo S., 1964, цит. по Розенштраух Л.С., Виннер М.Г. Дифференциальная рентгенодиагностика заболеваний органов дыхания и средостения. Руководство для врачей: В 2 т. — Т. 2. — М.: Медицина, 1991. — С. 173].
По мнению Е.А. Немиро и Н.А. Балыня [2], ее можно расценивать как провоцирующий фактор в развитии истинной грыжи щели Ларрея — Морганьи или ретрокостостернальной диафрагмальной грыжи по классификации Б.В. Петровского [3]. Проникая через расширенную грудино-реберную щель, АМЛ расширяет ее и тянет за собой брюшину в виде конуса, который в последующем становится грыжевым мешком. При повышении внутрибрюшного давления грудино-реберный треугольник постепенно расширяется, что ведет к местному истончению мышц диафрагмы и их атрофии, а в дальнейшем к увеличению отверстия в диафрагме, через которое проникает большой сальник. Реже вместе с ним в грыжевой мешок вовлекаются петли тонкой кишки или часть поперечной ободочной кишки [4]. Парастернальные грыжи в большинстве случаев располагаются справа от грудины, так как слева бóльшая часть треугольника Ларрея прикрыта перикардом и сердцем, образуя своего рода защиту.
Основным методом диагностики патологии переднего правого кардиодиафрагмального угла традиционно является рентгенография грудной клетки в двух проекциях, позволяющая выявить тенеобразующий объект у правого контура сердца непосредственно позади грудной стенки [5, 6]. При необходимости выполняется рентгеноскопия с контрастированием пищевода и желудка. Диагностика основана на оценке характера тени, что не всегда позволяет правильно решить вопрос о причине ее возникновения (рис. 2).
Рисунок 2.
Рентгенография грудной клетки в двух проекциях: а — АМЛ; б — ЦКП
Патологическая тень в правом кардиодиафрагмальном углу. Схожая рентгенологическая картина тени (стрелки) не позволяет уверенно дифференцировать АМЛ и ЦКП
В качестве дополнительного диагностического метода рекомендуется использовать компьютерную томографию. Эхография даже не упоминается как способ визуализации образований данной локализации, хотя пристеночное расположение объекта исследования с возможностью сканирования как из межреберных промежутков, так и субкостально предоставляет хорошие условия для использования ультразвукового метода в качестве информативной, радиологически безопасной альтернативы рентгенологическому методу [7].
Цель исследования — разработка дифференциальной ультразвуковой диагностики патологических образований правого кардиодиафрагмального угла с определением структуры тенеобразующего объекта.
Материал и методы
С 2000 года на базе отделения торакальной хирургии городской клинической больницы № 5 г. Нижнего Новгорода с помощью УЗИ грудной клетки диагностировано 120 АМЛ, 28 ЦКП, 6 ГЩЛ, обусловивших затемнение правого кардиодиафрагмального угла. Верификация осуществлялась при хирургическом лечении, а при отсутствии показаний к нему при длительном динамическом наблюдении.
Рентгенография грудной клетки в двух проекциях выполнялась на аппаратах Chirodur 125C (Чехия) и EDR-750 (Германия). УЗИ проводилось на сканере SIM7000 Chellenge(Esaote, Италия) секторными датчиками 3,5 и 7,5 МГц по разработанной нами методике [8]. УЗИ грудной клетки не требовало специальной подготовки больного и выполнялось в вертикальном положении пациента на свободном дыхании и при задержке дыхания на вдохе или выдохе. Для сканирования в межреберьях предпочтительнее датчики с небольшой апертурой — секторные или микроконвексные, но исследование можно проводить и обычным конвексным датчиком.
Предложенная методика дифференциальной ультразвуковой диагностики патологии правого кардиодиафрагмального угла, в первую очередь абдомино-медиастинальной липомы, складывалась из двух последовательных этапов. Для удобства сканирования пациент вставал перед врачом лицом или с небольшим поворотом вправо, при необходимости пациентки отводили молочную железу вверх и латерально так, чтобы обеспечить доступ датчика к межреберьям по правой парастернальной линии.
Первым этапом являлось выявление патологического образования в правом кардиодиафрагмальном углу и оценка его ультразвукового изображения. Сначала проводили горизонтальное сканирование кардиодиафрагмального угла и расположенного в нем патологического объекта, для чего датчик устанавливался по правой парастернальной линии над реберной дугой перпендикулярно к поверхности грудной клетки. В такой плоскости получалось наиболее четкое изображение контуров сердца и диафрагмы. Покачивая датчик вверх-вниз, проводили поперечное сканирование кардиодиафрагмального угла, при необходимости слегка поворачивая датчик вокруг горизонтальной оси для получения максимального по площади изображения объекта, и производили измерение его поперечного (ширина) и переднезаднего (толщина) размера.
АМЛ в такой плоскости имела треугольную форму, поскольку принимала форму занятого пространства кардиодиафрагмального угла. Ее поперечный размер определяли на уровне наибольшей ширины жировой ткани как расстояние от диафрагмы до контура сердца. На этом же уровне измеряли толщину АМЛ как расстояние от ее костальной поверхности до наиболее удаленной вглубь средостения точки. При необходимости более полного осмотра наружной границы кардиодиафрагмального угла датчик по межреберью смещался латеральнее правой парастернальной линии либо ось сканирования направлялась вправо.
После осмотра в горизонтальной плоскости датчик в межреберье поворачивали на 90° по часовой стрелке для получения сагиттального сечения патологического объекта и измерения его вертикального размера. Применительно к АМЛ в этой плоскости оценивалась толщина жировой ткани на разных уровнях и определялась верхняя граница с воздушной легочной тканью.
Затем датчик устанавливался на переднюю брюшную стенку под местом прикрепления правой реберной дуги к грудине со значительным краниальным наклоном, при этом ось сканирования направлялась вверх и немного вправо к середине ключице. Тем самым получали продольное косое сечение кардиодиафрагмального угла, ориентированное снизу вверх, соответственно распространению АМЛ в средостение. Покачивая датчик вокруг горизонтальной оси, выбирали наибольший вертикальный размер АМЛ в виде пространства, заполненного жировой тканью и ограниченного медиально правым контуром сердца, латерально — куполом диафрагмы, сверху — поверхностью воздушного легкого. В этой плоскости определяли высоту АМЛ как расстояние от ее нижней до верхней границы, понимая под этим максимальное распространение предбрюшинной клетчатки в переднее средостение. Информативность исследования из субкостальной позиции датчика снижалась при значительно выраженной подкожно-жировой клетчатке, когда не представлялось возможным ориентировать плоскость сканирования под необходимым углом наклона.
На втором этапе исследования выявлялась взаимосвязь патологического образования в правом кардиодиафрагмальном углу с передней брюшной стенкой или органами брюшной полости. Тем самым у АМЛ подтверждалось наличие ножки в виде сообщения избыточной жировой ткани в средостении с предбрюшинной клетчаткой, а при ГЩЛ — переход жировой клетчатки большого сальника, а при больших грыжах и петли кишки, из брюшной полости в грудную клетку через грыжевые ворота в диафрагме. Для этого датчик в сагиттальной плоскости из межреберья или субкостальной позиции под визуальным контролем направляли каудально, при необходимости смещая его далее вниз вдоль передней брюшной стенки. Подобным образом при АМЛ на уровне щели Ларрея в диафрагме прослеживалась жировая ткань, а ниже ее переход в предбрюшинную клетчатку, расположенную перед печенью. Для лучшей визуализации ножки на уровне диафрагмы в ряде случаев требовалось небольшое вращение датчика вокруг горизонтальной оси до четкого выявления места проникновения жировой ткани через щель Ларрея. Возможен и обратный способ визуализации ножки АМЛ путем смещения датчика вверх вдоль передней брюшной стенки в межреберье, прослеживая снизу вверх переход предбрюшинной клетчатки в жировую ткань в кардиодиафрагмальном углу.
Результаты
Трансторакальное УЗИ проводилось без предварительного изучения рентгенографической картины грудной клетки. Во всех случаях ультразвуковое определение тенеобразующей структуры в правом кардиодиафрагмальном углу было выполнено верно, точность дифференциальной диагностики АМЛ и ЦКП составила 100%. Это обусловлено значительной разницей акустических свойств жировой ткани и жидкости, а также связано с оценкой взаимосвязи патологического объекта с предбрюшинной клетчаткой, что невозможно сделать рентгенологически.
Эхокартина АМЛ складывалась из двух компонентов — избыточного количества жировой ткани в правом кардиодиафрагмальном углу и ножки, соединяющей ее с предбрюшинной клетчаткой. Жировая ткань занимала пространство между печенью и сердцем и имела вид дополнительного образования примерно треугольной формы с неоднородной эхоструктурой за счет множественных мелких гиперэхогенных сигналов на гипоэхогенном фоне (рис. 3).
Рисунок 3.
Эхограмма правого кардиодиафрагмального угла в поперечной плоскости сканирования.
АМЛ в горизонтальном сечении имеет вид гипоэхогенного образования (1) треугольной формы с неоднородной эхоструктурой за счет множественных мелких гиперэхогенных сигналов, заполняющего пространство между печенью (2) и сердцем (3)
Она не имела эхоскопически видимой капсулы и ограничивалась непосредственно диафрагмой и сердцем, а ее эхоструктура идентична ультразвуковому изображению предбрюшинной клетчатки (рис. 4 клетчатка).
Рисунок 4.
Эхограмма передней брюшной стенки по средней линии тела, продольное сканирование
Предбрюшинная клетчатка (1) в виде гипоэхогенного слоя с неоднородной эхоструктурой за счет множественных мелких гиперэхогенных сигналов, печень (2)
На глубоком вдохе при смещении купола диафрагмы вниз АМЛ слегка изменяла свою форму, а реверберации от воздушной легочной ткани частично перекрывали ее верхний край. В горизонтальной плоскости сканирования ширина и глубина выявленных липом колебались от 4,0х3,5 см до 8,0х7,0 см, но чаще их размеры не превышали 6,0х5,0 см.
Важным диагностическим признаком АМЛ являлась визуализация ножки в виде узкого гипоэхогенного участка на уровне диафрагмы, без какой-либо границы переходившего каудально в предбрюшинную клетчатку, а краниально — в саму липому. Иногда на протяжении ножки наблюдалось небольшое локальное сужение в виде «зарубки» непосредственно в месте проникновения сквозь щель Ларрея (рис. 5, ножка). Частота обнаружения зависела от толщины ножки, которая составила в среднем 8,2±1,5 мм, и была видна у 85 (70,8%) больных.
Рисунок 5.
Эхограмма правого кардиодиафрагмального угла в продольной плоскости сканирования
Ножка АМЛ (1) в виде узкого гипоэхогенного участка с «зарубкой», переходящего краниально в АМЛ (2), а каудально — в предбрюшинную клетчатку (3), печень (4)
Отмечено, что у пациентов со значительно повышенной массой тела хорошо выраженная паракардиальная клетчатка средостения могла имитировать АМЛ вследствие типичной для жировой ткани эхоструктуры. Но в отличие от последней медиастинальная клетчатка не имела ножки и не распространялась ниже уровня диафрагмы, кроме того, она лоцировалась по обе стороны сердца и ее размеры не превышали 3,0х2,5 см.
УЗИ при грыже щели Ларрея имело разную информативность в зависимости от содержимого грыжевого мешка. Небольшое количество наблюдений пока не позволяет создать обобщенную эхокартину данного заболевания, но следует отметить, что наибольшие диагностические сложности возникали при наличии в грыжевом выпячивании пряди большого сальника, который по акустическим свойствам не отличался от предбрюшинной жировой клетчатки. У 3 больных такая грыжа эхоскопически была расценена как АМЛ и не диагностирована до операции. Для дифференцирования этих заболеваний необходимо более внимательно оценивать ту структуру, в которую переходила ножка дополнительной жировой ткани: в предбрюшинную клетчатку, расположенную поверхностно от непрерывной гиперэхогенной линии брюшины, или в большой сальник глубже нее, в который клетчатка из правого кардиодиафрагмального угла переходила с наличием участка перерыва гиперэхогенной линии брюшины.
Однако петли тонкой кишки отчетливо визуализировались в грыжевом мешке, особенно при ущемлении с развитием острой тонкокишечной непроходимости. В таких случаях выше печени и диафрагмы в кардиодиафрагмальном углу лоцировалась изогнутая трубчатая структура с жидким содержимым и неоднородной малоподвижной взвесью, отграниченная эхогенной стенкой, а в брюшной полости наблюдалась типичная эхокартина острой тонкокишечной непроходимости. При неущемленной грыже о присутствии в ней петли тонкой кишки можно судить по наличию в грыжевом содержимом подвижных гиперэхогенных сигналов с акустической тенью и реверберациями «хвоста кометы», обусловленных отражением ультразвука от скоплений газа, смещавшихся при перистальтических сокращениях.
Целомические кисты перикарда располагались паракардиально чаще вдоль правого, реже вдоль левого контура сердца, преимущественно на уровне желудочков и только при крупных размерах достигали предсердий. Вследствие такого вариабельного расположения при их диагностике необходимо использовать не только предложенные доступы для визуализации правого кардиодиафрагмального угла, но и стандартные эхокардиографические позиции. Методически исследование практически не отличалось от ультразвукового способа диагностики АМЛ, только большее внимание уделялось осмотру паракардиального пространства вдоль левых отделов сердца [9].
Для ультразвукового изображения ЦКП характерно непосредственное соприкосновение с контуром сердца на достаточном протяжении и овальная или каплевидная форма, при которой продольная ось образования располагалась вертикально или параллельно длинной оси сердца (рис. 6).
Рисунок 6.
Эхограмма правого кардиодиафрагмального угла в поперечной плоскости сканирования
Целомическая киста перикарда (1) в виде анэхогенного овального образования вдоль стенки правого желудочка (2), паракардиальная жировая клетчатка (3)
Однако при локализации в правом кардиодиафрагмальном углу киста часто принимала форму того пространства, которое она занимала между сердцем и диафрагмой, то есть примерно треугольную со сглаженными углами. Размеры ЦКП колебались в более широких пределах, чем размеры АМЛ, и составляли от 4 до 20 см в наибольшем измерении. При импульсноволновой допплерографии в полости ЦКП наблюдалась неспецифическая передаточная пульсация за счет сократительных движений сердца.
Поскольку в кисте содержалась прозрачная жидкость, то она имела однородную анэхогенную структуру, что принципиально отличало ее от гипо- или среднеэхогенных тканевых образований. Только у 3 (10,7%) больных отмечена рыхлая мелко- или среднезернистая взвесь на анэхогенном фоне, что соответствовало мутной жидкости в полости кисты. Подавляющее большинство ЦКП представляли собой анэхогенные замкнутые полости без сообщения с перикардиальной или плевральной полостью. Установить связь полости кисты с полостью перикарда удалось только у двух пациентов, что не позволяет рассматривать этот признак как обязательный компонент эхосемиотики. Естественно, отсутствовала и связь с предбрюшинной клетчаткой.
Важным диагностическим признаком являлось наличие у кисты тонкой и четкой эхогенной стенки. Она лучше прослеживалась на тех участках, где не соприкасалась с интенсивно отражавшими ультразвук структурами, то есть с воздушной легочной тканью, перикардом или диафрагмой. Обычно это был переход от поверхности сердца к передней грудной стенке или диафрагме, где стенка кисты отходила от поверхности этих органов и отграничивала анэхогенную жидкость в полости кисты от паракардиальной жировой клетчатки (рис. 7).
Рисунок 7.
Эхограмма правого кардиодиафрагмального угла в поперечной плоскости сканирования
Тонкая эхогенная стенка (1) отграничивает паракардиальную жировую клетчатку (2) от полости целомической кисты перикарда (3) на участке между сердцем (4) и грудной стенкой (5)
Эхографическое исследование правого кардиодиафрагмального угла, несмотря на высокую информативность в дифференцировке находящихся в нем образований, является дополнительным методом лучевой диагностики патологии данного отдела средостения. Ведущим диагностическим скрининговым методом обоснованно остается рентгенография грудной клетки в двух проекциях. Однако на этапе уточняющей диагностики следующим исследованием предпочтительнее использовать эхографию грудной клетки в качестве более простого, доступного и радиологически безопасного метода по сравнению с компьютерной томографией [10]. Обследование поддиафрагмального пространства входит в компетенцию врачей ультразвуковой диагностики, проводящих исследование органов брюшной полости. Технически овладеть сканированием парастернальной наддиафрагмальной зоны не сложно, поэтому оценку состояния правого кардиодиафрагмального угла следует шире вводить в клиническую практику.
Заключение
Ультразвуковое исследование переднего правого кардиодиафрагмального угла предоставляет новые возможности для дифференциальной диагностики расположенных в нем патологических процессов. Уверенная ультразвуковая дифференцировка АМЛ и ЦКП предоставляет хирургу возможность целенаправленно выбирать тактику лечения и определять способ оперативного лечения, а также обусловливает оптимальное применение торакоскопических вмешательств и трансмиоректального доступа как наиболее эффективного и наименее травматичного способа лечения в каждой конкретной ситуации. Сочетание трансторакальной ультразвуковой диагностики и современных оперативных возможностей создает единый лечебно-диагностический комплекс, оптимизирующий хирургическое лечение патологии правого кардиодиафрагмального угла.
1. Синельников Р.Д., Синельников Я.Р. Атлас анатомии человека: Учеб. пособие. — В 4 т. — Т. 1. — М.: Медицина, 1996. — С. 216-218.
2. Немиро Е.А., Балыня Н.А. Парастернальные (абдомино-медиастинальные) липомы и диафрагмальные грыжи // Вестник рентгенологии и радиологии. — 1970. — № 2. — С. 3-9.
3. Петровский Б.В., Каншин Н.Н., Николаев Н.О. Хирургия диафрагмы. — Л.: Медицина, 1966. — 547 с.
4. Муртазалиева М.С. Диагностика и хирургическое лечение патологических образований переднего правого кардиодиафрагмального угла с использованием трансмиоректального доступа: автореф. дис. … канд. мед. наук: 14.01.17, 14.01.13. — Н. Новгород, 2010. — 21 с.
5. Розенштраух Л.С., Виннер М.Г. Дифференциальная рентгенодиагностика заболеваний органов дыхания и средостения. Руководство для врачей: В 2 т. — Т. 2. — М.: Медицина, 1991. — 384 с.
6. Власов П.С. Лучевая диагностика заболеваний органов грудной полости. — М.: Видар-М, 2006. — 312 с.
7. Королев Б.А., Сафонов Д.В., Павлунин А.В., Муртазалиева М.С. Парастернальные диафрагмальные грыжи: особенности диагностики и выбора оперативного доступа // Анналы хирургии. — 2010. — № 1. — С. 26-30.
8. Способ диагностики абдоминомедиастинальной липомы: пат. 2317775 Рос. Федерация: МПК 51 А61В 8/00 / Сафонов Д.В., Павлунин А.В., Муртазалиева М.С.; заявитель и патентообладатель Нижегородская гос. медицинская академия. — № 2006102031/14; заявл. 27.07.2007; опубл. 27.02.2008. Бюл. № 6.
9. Способ дифференциальной диагностики абдоминомедиастинальной липомы и целомической кисты перикарда: пат. 2317776 Рос. Федерация: МПК 51 А61В 8/00 / Сафонов Д.В., Павлунин А.В., Муртазалиева М.С.; заявитель и патентообладатель Нижегородская гос. медицинская академия. — № 2006102032/14; заявл. 27.07.2007; опубл. 27.02.2008. Бюл. № 6.
10. Wernecke K. Mediastinale Sonographie: Untersuchungstechnik, diagnostische Effizienz und Stellenwert in der bildgebenden Diagnostik des Mediastinums. — Berlin; Heidelberg; New York: Springer-Verlag, 1991. — 111 s.
1. Sinel’nikov R.D., Sinel’nikov Ya.R. Atlas anatomii cheloveka: ucheb. posobie [Atlas of Human Anatomy: Textbook. allowance]. In 4 vol. Vol. 1. Moscow: Meditsina, 1996. Pp. 216-218.
2. Nemiro E.A., Balynya N.A. Parasternal (abdomino-mediastinal) lipomas and diaphragmatic hernia. Vestnik rentgenologii i radiologii, 1970, no. 2, pp. 3-9 (in Russ.).
3. Petrovskiy B.V., Kanshin N.N., Nikolaev N.O. Khirurgiya diafragmy [Surgery of the diaphragm]. Leningrad: Meditsina, 1966. 547 p.
4. Murtazalieva M.S. Diagnostika i khirurgicheskoe lechenie patologicheskikh obrazovaniy perednego pravogo kardiodiafragmal’nogo ugla s ispol’zovaniem transmiorektal’nogo dostupa: avtoref. dis. … kand. med. nauk [Diagnosis and surgical treatment of pathological formations front right corner kardiodiafragmal using transmiorektal access. Synopsis of diss. of PhD med. sci]. Nizhnii Novgorod, 2010. 21 p.
5. Rozenshtraukh L.S., Vinner M.G. Differentsial’naya rentgenodiagnostika zabolevaniy organov dykhaniya i sredosteniya. Rukovodstvo dlya vrachey: V 2 t. [Differential x-ray diagnosis of diseases of the respiratory system and mediastinum. Guide for Physicians: In 2 volumes]. Vol. 2. Moscow: Meditsina, 1991. 384 p.
6. Vlasov P.S. Luchevaya diagnostika zabolevaniy organov grudnoy polosti [Ray diagnosis of diseases of the chest cavity]. Moscow: Vidar-M, 2006. 312 p.
7. Korolev B.A., Safonov D.V., Pavlunin A.V., Murtazalieva M.S. Parasternal diaphragmatic hernia : diagnostic features and a choice of operative access. Annaly khirurgii, 2010, no. 1, pp. 26-30 (in Russ.).
8. Safonov D.V., Pavlunin A.V., Murtazalieva M.S. Abdominomediastinalnoy method for diagnosing lipomas: pat. 2317775 Ros. Federatsiya: MPK51 A61V 8/00; zayavitel’ i patentoobladatel’ Nizhegorodskaya gos. meditsinskaya akademiya. № 2006102031/14; zayavl. 27.07.2007; opubl. 27.02.2008. Byul. no. 6 (in Russ.).
9. Safonov D.V., Pavlunin A.V., Murtazalieva M.S. A method of differential diagnosis of lipoma and abdominomediastinalnoy coelomic pericardial cyst: pat. 2317776 Ros. Federatsiya: MPK51 A61V 8/00; zayavitel’ i patentoobladatel’ Nizhegorodskaya gos. meditsinskaya akademiya. No. 2006102032/14; zayavl. 27.07.2007; opubl. 27.02.2008. Byul. no. 6 (in Russ.).
10. Wernecke K. Mediastinale Sonographie: Untersuchungstechnik, diagnostische Effizienz und Stellenwert in der bildgebenden Diagnostik des Mediastinums. Berlin; Heidelberg; New York: Springer-Verlag, 1991. 111 p.