плотность водорода по отношению к воздуху
Теплопроводность, плотность и теплофизические свойства водорода H2
Плотность водорода
В таблице представлены значения плотности водорода H2 в зависимости от температуры и давления.
Как известно, водород является самым легким газом на планете. При высоких температурах его плотность чрезвычайно мала и кубометр этого газа в таких условиях будет весить всего несколько грамм.
При нагревании водород становится менее плотным, его плотность снижается. Однако при росте давления, плотность водорода будет увеличиваться пропорционально давлению.
В таблице представлена плотность газообразного водорода в кг/м 3 при нормальном атмосферном давлении в зависимости от температуры при отрицательных и положительных ее значениях.
| t, °С | -73 | -53 | -33 | -13 | 7 | 27 | 77 | 127 | 177 | 227 |
|---|---|---|---|---|---|---|---|---|---|---|
| ρ, кг/м 3 | 0,1211 | 0,1101 | 0,1010 | 0,0932 | 0,0865 | 0,0808 | 0,0692 | 0,0606 | 0,0539 | 0,0485 |
| t, °С | 277 | 327 | 377 | 477 | 577 | 727 | 927 | 1027 | 1127 | 1227 |
| ρ, кг/м 3 | 0,0441 | 0,0404 | 0,0373 | 0,0323 | 0,0285 | 0,0242 | 0,0202 | 0,0186 | 0,0173 | 0,0162 |
Плотность водорода в следующей таблице приведена в размерности в кг/м 3 при температуре от 0 до 1000 °С и давлении от 1 до 100 бар.
| ↓ t, °С / P, бар → | 1 | 10 | 20 | 40 | 60 | 80 | 100 |
|---|---|---|---|---|---|---|---|
| 0 | 0,0870 | 0,8654 | 1,720 | 3,398 | 5,033 | 6,627 | 8,181 |
| 100 | 0,0637 | 0,6342 | 1,232 | 2,499 | 3,712 | 4,900 | 6,064 |
| 300 | 0,0415 | 0,4136 | 0,824 | 1,637 | 2,431 | 3,229 | 4,009 |
| 500 | 0,0308 | 0,3068 | 0,612 | 1,219 | 1,820 | 2,416 | 3,007 |
| 700 | 0,0244 | 0,2439 | 0,487 | 0,970 | 1,450 | 1,927 | 2,400 |
| 1000 | 0,0187 | 0,1865 | 0,373 | 0,743 | 1,111 | 1,478 | 1,842 |
Теплофизические свойства водорода
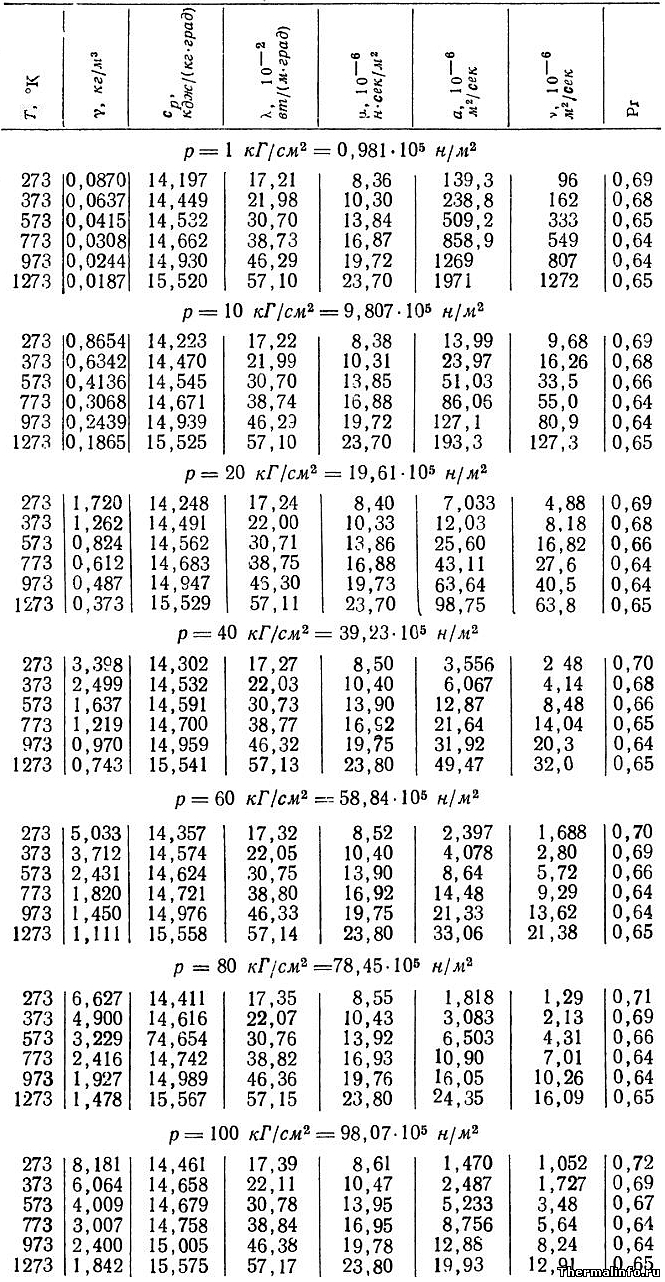
В таблице даны теплофизические свойства водорода в зависимости от температуры и давления.
Свойства указаны в интервале температуры от 0 до 1000°С, давление водорода в таблице изменяется от 1 до 100 бар.
В таблице приведены следующие свойства водорода:
Некоторые свойства водорода сильно зависят от температуры и давления. Так, с повышением давления и при снижении температуры, значительно увеличивается плотность водорода.
Теплоемкость водорода с ростом температуры увеличивается слабо. По данным таблицы также видно, что удельная теплоемкость водорода от давления практически не зависит.
Значение теплопроводности, вязкости и температуропроводности водорода увеличиваются с ростом его температуры. С повышением давления водорода уменьшается величина его температуропроводности. Число Прандтля водорода почти не зависит от температуры и давления.
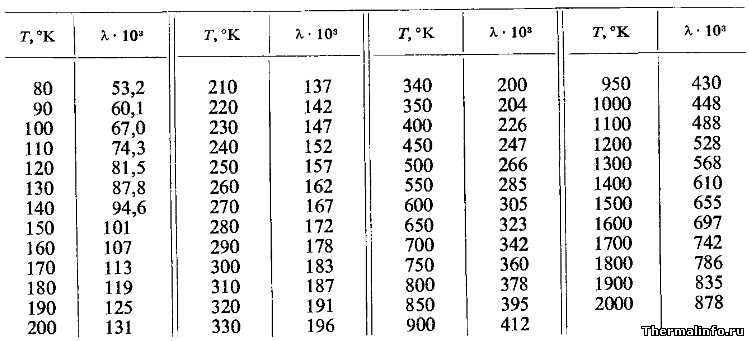
Теплопроводность водорода при атмосферном давлении
Например, при 270 К (-3°С) теплопроводность водорода равна 0,167 Вт/(м·град).
По данным таблицы видно, что с ростом температуры теплопроводность водорода увеличивается.
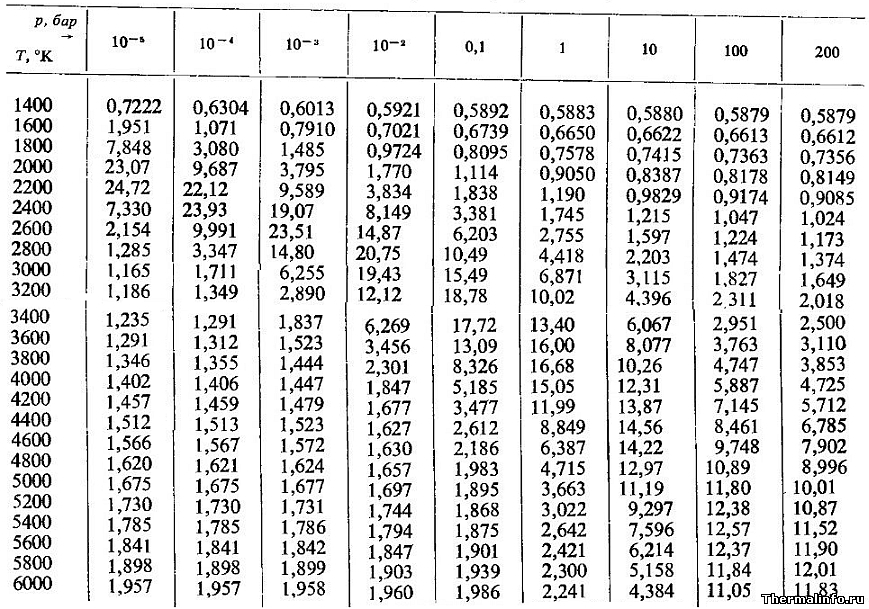
Теплопроводность водорода при высоких температурах
В таблице представлена теплопроводность водорода при высоких температурах в зависимости от давления. Размерность теплопроводности в таблице Вт/(м·град).
Например при температуре 6000 К и давлении 200 бар водород имеет теплопроводность 11,83 Вт/(м·град), что сравнимо с теплопроводность такого металла, как висмут.
Источники:
Плотность водорода
Плотность водорода и другие его физические свойства
Его температуры плавления и кипения лежат весьма низко (см. таблицу). В воде он растворим незначительно – 2:100 по объему. Характерна для водорода растворимость в некоторых металлах.
Водород – самый легкий из всех газов, он в 14,5 раз легче воздуха; масса 1 л водорода при нормальных условиях равна 0,09 г. Молекулы водорода движутся быстрее всех остальных. Поэтому водород характеризуется наибольшей скоростью диффузии, т.е. скорее всех других газов распространяется в пространстве, проходит сквозь различные мелкие поры и т.д. Этим же обусловлена и его высокая теплопроводность. Так, при прочих равных условиях нагретый предмет охлаждается водородом в семь раз быстрее, чем воздухом.
Плотность вещества – это отношение его массы к объему:
Таблица 1. Физические свойства водорода.
Температура плавления, o С
Температура кипения, o С
Энергия ионизации атома, эВ
Сродство атома к электрону, эВ
Межъядерное расстояние в молекуле, нм
Стандартная энтальпия диссоциации молекул при 25 o С, кДж/моль
Распространенность водорода в природе
Водород является одним из наиболее распространенных элементов – его доля составляет около 1% от массы всех трех оболочек земной коры (атмосферы, гидросферы и литосферы), что при пересчете на атомные проценты дает цифру 17,0.
Основное количество этого элемента находится в связанном состоянии. Так, вода содержит около 11% (масс.), глина – около 1,5% и т.д. В виде соединений с углеродом водород входит в состав нефти, горючих природных газов и всех организмов.
Свободный водород состоит из молекул H2. Он часто содержится в вулканических газах. Частично он образуется также при разложении некоторых органических остатков. Небольшие количества его выделяются зелеными растениями. Атмосфера содержит около 0,00005% (об.) водорода.
Краткое описание химических свойств и плотность водорода
Водород проявляет сильные восстановительные свойства при повышенных температурах, реагирует с металлами, неметаллами и оксидами металлов.
Чтобы смесь, состоящая из водорода и натрия / кальция прореагировала, необходимо нагреть её до температуры 300 o С или 500 – 700 o С соответственно:
Водород при определенных условиях реагирует с солями, кислотными оксидами и другими сложными веществами. Так, реакция взаимодействия с сульфатом натрия протекает при нагревании (500 – 600 o С) и участии катализатора (Fe2O3):
В реакции с диоксидом углерода катализатором выступает оксид меди (I), а требуемая температура нагрева равна 200 o С:
Примеры решения задач
| Задание | Плотность паров простого вещества фосфора по водороду – 62. Определите формулу фосфора. |
| Решение | Отношение массы данного газа к массе другого газа, взятого в том же объеме, при той же температуре и том же давлении, называется относительной плотностью первого газа по второму. Данная величина показывает, во сколько раз первый газ тяжелее или легче второго газа. |
Молярная масса газа равна его плотности по отношению к другому газу, умноженной на молярную массу второго газа:
Тогда, молярная масса газа фосфора будет равна:
Относительная атомная масса фосфора равна 30,9738 а.е.м. Тогда, в состав молекулы фосфора входит Mgas /Ar(P) атомов фосфора:
Значит формула молекулы фосфора P4.
| Задание | Плотность газа по воздуху – 0,59. Массовая доля элемента азота в нем – 82,35%, а водорода – 17,65%. Выведите формулу газа. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: |
ω (Х) = n × Ar (X) / M (HX) × 100%.
Обозначим число атомов азота в молекуле через «х», число атомов водорода через «у».
Найдем соответствующие относительные атомные массы элементов азота и водорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел).
Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения:
x:y = 5,88 : 17,65= 1 : 3.
Значит простейшая формула соединения азота и водорода имеет вид NH3.
Значение молярной массы газа можно определить при помощи его плотности по воздуху:
Mgas = 29 × 0,59 = 17,11 г/моль.
Чтобы найти истинную формулу соединения азота и водорода найдем отношение полученных молярных масс:
M(NH3) = Ar(N) + 3 × Ar(H) = 14 + 3 × 1 = 14 + 3 = 17 г/моль.
Таким образом формула вещества будет иметь вид NH3. Это аммиак.