позитивные аспекты эффектов активных форм кислорода
Активный кислород: друг или враг, или О пользе и вреде антиоксидантов
Активный кислород: друг или враг, или О пользе и вреде антиоксидантов
Пероксид водорода: мощный окислитель, способный повреждать клеточные структуры, но в то же время регулятор важнейших клеточных процессов
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Долгое время активные формы кислорода считались вредными побочными продуктами обмена веществ. За последнее десятилетие, однако, учёные показали, что живые организмы не только могут использовать активный кислород в своих целях, но и целенаправленно его вырабатывают. Возникает вопрос: нужно ли бороться с активными формами кислорода с помощью антиоксидантов?
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучший обзор».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Вот уже много лет производители продуктов питания и косметики твердят о пользе для нашего здоровья антиоксидантов. В связи с этим в головах людей прочно укрепляется точка зрения, что эти чудодейственные вещества являются своего рода панацеей от многих болезней и даже предотвращают процесс старения. Однако недавние исследования показывают, что всё не так однозначно, как считалось ранее.
Со времён изобретения сине-зелёными бактериями кислородного фотосинтеза [1] мы живём в чрезвычайно агрессивной окислительной среде. Правда, сам по себе кислород не очень страшен для нас, живых организмов, поскольку, чтобы пошла реакция окисления, необходимо преодолеть высокий энергетический барьер (или, говоря другими словами, нас нужно было бы поджечь). Однако иногда в процессах неполного окисления кислород превращается в так называемые активные формы (АФК), и тогда эти молекулы становится поистине страшным окислителем, взаимодействуя с любой органикой, встретившейся на пути: белками, жирами, углеводами, нуклеиновыми кислотами. И в наших клетках ежесекундно вырабатываются тысячи таких молекул — как побочные продукты дыхания, реакций синтеза и распада биомолекул.
К счастью, в нашем организме предусмотрены системы защиты от нежелательного окисления. Существуют специальные ферменты, занимающиеся нейтрализацией активных форм кислорода и их восстановлением до воды. Окислительные повреждения белков и ДНК, которые ещё можно обратить, восстанавливаются специальными ферментами репарации, а молекулы, подвергнувшиеся необратимым изменениям, уничтожаются. Таким образом, наш организм наделён природными антиоксидантами и способен сам постоять за себя.
Но иногда антиоксидантные системы организма дают сбой, и тогда активные формы кислорода могут причинить ощутимый урон. Опасность заключается ещё и в том, что процесс накопления окислительных повреждений обладает положительной обратной связью: повреждения молекул, отвечающих за регуляцию выработки и деградации АФК, порождают ещё большее увеличение содержания АФК в клетке. Так, известно, что при старении, травмах и некоторых заболеваниях (например, болезнях Альцгеймера и Паркинсона) повышается уровень окислительных повреждений в мозге [2], [3].
В свете сказанного понятно, почему врачи и фармацевты возлагают большие надежды на использование природных и синтетических антиоксидантов для лечения (или хотя бы облегчения протекания) болезней, сопровождающихся окислительными повреждениями тканей. И действительно, исследования на модельных животных показали, что использование антиоксидантов способствует смягчению симптомов некоторых заболеваний и даже может увеличивать среднюю продолжительность жизни. Так, в лаборатории академика В.П. Скулачёва были получены искусственные антиоксиданты, широко известные под названием «ионы Скулачёва» и способные встраиваться в мембраны митохондрий — одного из основных источников активных форм кислорода в клетке. С помощью этих антиоксидантов удалось обратить вспять некоторые вызванные старением нарушения у лабораторных животных [4].
И всё же, за последний десяток лет отношение учёных к активным формам кислорода кардинально изменилось. Всё началось с открытия в клетках иммунной системы фермента NADPH-оксидазы, единственная функция которого — осуществлять продукцию активных форм кислорода для борьбы с патогенными организмами. С его помощью макрофаги «поливают» нежелательных гостей токсичными молекулами супероксида, пероксида водорода, гипохлорита и др. в ходе так называемого «окислительного взрыва». Каково же было удивление учёных, когда этот фермент и ещё целых шесть его «родственников» (изоформ) были обнаружены практически во всех тканях организма!
Сейчас известно, что активные формы кислорода участвуют в регуляции многих процессов в клетке, влияя на скорость деления клеток и дифференцировку, а также на другие клеточные функции. Некоторая ирония заключается в том, что развитию «полезных» функций АФК способствовали свойства, следующие из его токсичности — высокая способность взаимодействовать с биомолекулами и наличие систем для его быстрого разрушения в клетке. Иными словами, активный кислород можно использовать как сигнальный маяк, быстро включая или выключая по необходимости. Таким образом, наш организм научился извлекать выгоду даже из такого, казалось бы, «вредного» побочного продукта, как активные формы кислорода.
Как же осуществляется такая регуляция? Для слаженной работы нашего организма клеткам необходимо обмениваться между собой информацией посредством гормонов, факторов роста и других специальных молекул. Эти вещества узнаются и связываются белками-рецепторами, о чём последние извещают клетку с помощью целого каскада ферментативных реакций. Особую роль в этих процессах играет осуществляемая специальными ферментами — киназами [5], [6] — реакция фосфорилирования белков. Она заключается в том, что к некоторым аминокислотным остаткам белка — тирозину и серину — присоединяется фосфатная группа, что приводит к его активации или, наоборот, подавлению активности. Этому процессу противостоит реакция дефосфорилирования, осуществляемая ферментами-фосфатазами и вызывающая в точности обратное действие. Баланс этих двух реакций и определяет уровень активности регулируемого белка в клетке. Например, инсулин — гормон, отвечающий за регуляцию потребления глюкозы клетками, — связывается с инсулиновыми рецепторами, находящимися на поверхности практически всех клеток организма, что приводит к появлению тирозинкиназной активности рецептора. Это запускает цепочку ферментативных процессов, в результате которых на мембране клеток увеличивается число белков-переносчиков глюкозы, и потребление клеткой глюкозы увеличивается [7].
Оказалось, что активные формы кислорода способны обратимо окислять остатки цистеина в каталитических участках некоторых фосфатаз и подавлять их активность. Это приводит к смещению уровня фосфорилированности регулируемых ими белков, что, конечно, влияет на передаваемый клетке сигнал. Так, выделение активных форм кислорода было зафиксировано при связывании клеточными рецепторами инсулина, и было показано, что подавление их продукции добавлением антиоксидантов ослабляет действие гормона на клетку [7].
В многочисленных исследованиях было показано, что активные формы кислорода участвуют в синтезе некоторых соединений (например, тиреоидных гормонов), регуляции подвижности клеток соединительных тканей, роста сосудов и нервных окончаний и т.д.
Ещё один совсем недавно открытый эффект — участие АФК в регуляции процессов в мозге, лежащих в основе обучения и памяти. Как известно, основная функция нервных клеток — получать и передавать электрические сигналы посредством межклеточных контактов — синапсов. Именно здесь определяется, будет ли входящий с другого нейрона электрический сигнал передан дальше следующим нейронам, или же он пропадёт бесследно. При этом мозг — динамичная структура, причём в нём не только постоянно образуются новые и рассасываются ненужные клеточные контакты, но и проводимость самих синапсов может меняться [8]. Без этих процессов мы не смогли бы обучиться никаким навыкам или, например, запомнить сведения, приведённые в данной статье.
Так вот, на клеточных культурах, а потом и в исследованиях на модельных животных было показано, что активные формы кислорода не только влияют, но и необходимы для регулирования проводимости синапсов. Так, чрезмерная продукция антиоксидантных белков в мыши приводила к развитию когнитивных нарушений у этих животных [9].
Рисунок 1. Механизм регуляции сигнальных каскадов пероксидом водорода. Активация различных клеточных рецепторов активирует NADPH-оксидазу, выделяющую пероксид водорода. Он, в свою очередь, инактивирует тирозин-фосфатазы и активирует тирозин-киназы, регулируя тем самым степень фосфорилирования многих клеточных ферментов и, следовательно, их активность.
Таким образом, за последние десятилетия активный кислород превратился в глазах учёных из опасного побочного продукта в важный компонент сигнальных путей клетки. В связи с этим и нам нужно пересмотреть свое отношение к антиоксидантам как к безусловно полезным веществам, которых чем больше — тем лучше. Антиоксидантов, получаемых с потреблением свежих фруктов и овощей, вполне достаточно для ежедневных нужд организма. А к активному использованию антиоксидантов в медицине надо относиться внимательно, имея в виду возможные побочные эффекты при чрезмерном подавлении продукции активных форм кислорода.
Позитивные аспекты эффектов активных форм кислорода
Глава 1. Активные формы кислорода и их роль в норме
и в условиях оксидативного стресса
Рис. 1. Электронные структуры некоторых активных форм кислорода;
Общим для всех этих соединений является их высокая реакционная способность. АФК отличаются друг от друга реакционной способностью, временем жизни и выполняемыми функциями (табл. 1).
Таблица 1. Основные виды АФК ( Беленичев и др., 2009)
Время полужизни при
О 2
Хороший восстановитель, умеренный окислитель. Обладает свойствами внутриклеточного мессенджера : сигнальный механизм при взаимодействии различных подтипов глутаматных и аспартатных рецепторов, регуляция активности хлорных каналов, индукция образования пор в митохондриальной мембране. Участвует в окислительной модификации S Н- и N Н2-групп низкомолекулярных соединений. Вазоконстриктор. Антисептик
Мощный окислитель. Чрезвычайно активен в реакциях акцептирования и переноса электронов. Участвует в окислительной модификации нуклеиновых кислот, белков, липидов, простагландинов. Диффундирует на очень малые расстояния
Эффективен при взаимодействии с липидами, приводит к их окислительной модификации. Окислительные свойства на уровне НО •
В физиологических условиях АФК образуются преимущественно в следующих системах [4]:
· при синтезе простагландинов как по циклооксигеназному пути – в процессе превращения PgG2 в PgН2 ( пероксидазная функция Pg Н-синтазы ), так и по липоксигеназному пути – в процессе превращения гидроперекиси арахидоновой кислоты в оксикислоту ; этот процесс контролируется рядом пептидных гормонов ( ангиотензин ), цитокинов (TNF-β) и ростовых факторов;
· при спонтанном или катализируемом моноаминоксидазой окислении дофамина и адреналина (при спонтанном окислении образуется О 2 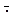
Действие АФК в организме фактически направлено на 3 типа клеточных мишеней: белки, нуклеиновые кислоты и липиды. В норме они активно участвуют в их метаболизме, а при патологических состояниях – в их окислительной деструкции.
Окислительная модификация белков, нуклеиновых кислот, липидов при участии АФК постоянно наблюдается в тканях и играет важную роль в распаде этих соединений. Это один из этапов обновления химического состава тканей.
В последнее время большое внимание уделяется изучению роли АФК в процессах метаболизма белков. Белки в силу особенностей своего строения являются одними из основных ловушек АФК. В связи с разнообразием химического строения, особенностями структурной организации белков процесс окислительной модификации белков носит сложный и специфический характер, что сопряжено с образованием большого количества окисленных продуктов радикальной и нерадикальной природы. Окислительное повреждение белков может быть связано с первичным нарушением или самого скелета полипептидной цепи, или отдельных аминокислотных остатков. Разделить эти процессы можно сугубо условно, т. к. окисление полипептидной цепи влечет за собой окисление остатков аминокислот и, наоборот, окислительная модификация радикалов отдельных аминокислот может сопровождаться либо агрегацией, либо фрагментацией белков. Наиболее чувствительными к окислению являются серосодержащие (метионин, цистеин) и ароматические (гистидин, триптофан, тирозин и фенилаланин ) аминокислотные остатки белков. Однако селективное повреждение этих лабильных аминокислотных остатков и механизм их окисления зависят от природы АФК.
Ответственным за протеолиз окисленных белков является мультикаталитический протеосомный комплекс, который существует в АТФ-независимой 19-20 S и АТФ-стимулируемой 26 S формах в клетках млекопитающих.
АФК вызывают окислительную модификацию нуклеотидов и нуклеиновых кислот, особенно ДНК. Это приводит к образованию гидропероксидов ROOH (так, из тимина образуется 5-СН2ООН-урацил), а затем и гидроксипроизводных ROH или R ( OH )2, основными из которых являются 8-ОН-2′-дезоксигуанозин и тимингликоль (их определение в тканях и моче используют как индексы окислительной модификации ДНК).
Существует большое количество данных, свидетельствующих о том, что живые организмы не только приспособились к сосуществованию со свободными радикалами, но фактически развили механизмы для выгодного использования их. Об этом свидетельствуют обнаруженные в последнее время новые функции АФК – регуляторные. Имеются определенные экспериментальные данные, свидетельствующие о том, что действия ряда первичных мессенджеров осуществляются либо через активацию процессов генерации АФК и повышение их уровня в тканях, либо через ингибирование компонентов АОЗ.
Следует отметить, что образование АФК различными изоформами НАДФН-оксидазы играет важную роль в регуляции каскада межклеточной сигнализации в различных типах нефагоцитирующих клеток, включая фибробласты, эндотелиальные клетки, гладкомышечные клетки сосудов, миоциты и клетки тироидной ткани.
Кроме того, установлено, что АФК образуются в клетках, стимулированных цитокинами, такими, как трансформирующий фактор роста р-1 (TGF-J31), интерлейкин-1, ФН О- α; пептидными факторами роста – тромбоцитарный фактор роста PDGF, основной фактор роста фибробластов bFGF ( basic fibroblast growth factor ); эпидермальный фактор роста EGF ( epidermal growth factor ); агонистами рецепторов ангиотензина II, тромбина и лизофосфатидной кислоты. Цитокины стимулируют освобождение АФК из многих типов клеток, включая фибробласты, эпителиальные и эндотелиальные клетки.
Таким образом, АФК играют важную роль в регуляции физиологических функций в тканях, вызывая стимуляцию различных сигнальных трансдукционных процессов, поэтому говорить о токсическом действии АФК не совсем верно. В нормально функционирующем организме АФК следует рассматривать с позиций их биологической значимости. С одной стороны, это продукты нормально протекающих окислительно-восстановительных реакций, с другой – специфические регуляторы метаболических процессов.
Свободнорадикальные реакции свойственны нормально метаболизирующей клетке. Окисление биомолекул идет со значительной скоростью, но стационарная концентрация продуктов окисления довольно мала вследствие наличия сложной системы взаимодействующих путей ее регуляции. Организм обладает многоуровневой стратегией защиты от повреждающего действия АФК. Защита осуществляется путем снижения образования первой АФК – О 2 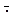
Ключевым ферментом антиокислительной защиты является супероксиддисмутаза (СОД), т. к. при ее участии прерывается цепь свободнорадикальных процессов в начале своего зарождения на стадии одноэлектронного восстановления кислорода с образованием О 2 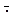

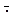
Глутатионпероксидаза (ГПО) эффективно расщепляет не только Н2О2, но и гидроперекисные соединения, образовавшиеся при ПОЛ:
2 GSH + ROOH → 2 GSSG + ROH + Н2О.
Таким образом, АОЗ тканей включает различные по своему химическому строению соединения. Однако действие всех компонентов ферментативной и неферментативной АОЗ в нормально функционирующем организме четко сбалансировано между собой, что обеспечивает поддержание количества оксидантов тканей на физиологическом уровне.
Для оксидативного стресса в первую очередь характерно нарушение в соотношении ант и- и прооксидантной систем в сторону повышения последней, отсутствие мобилизации активности АОЗ и нарушение сбалансированности самих компонентов этой системы. Начальные этапы запуска реакции генерации АФК при различных патологических состояниях могут отличаться, но уже на следующих этапах направленность и интенсивность свободнорадикальных процессов теряют свою специфичность и зависят от состояния и степени мобилизации АОЗ.
Т. к. нервная ткань является особенно чувствительной к АФК, что обусловлено высоким уровнем метаболизма, уникальным липидным составом и минимальным клеточным обновлением, окислительный стресс может способствовать инициации и прогрессированию ряда нейродегенеративных заболеваний. В настоящее время установлена роль окислительного стресса в развитии различных нейродегенеративных расстройств, таких, как амиотрофический латеральный склероз, болезнь Паркинсона, болезнь Альцгеймера, сосудистая деменция и др.
Немаловажным фактором усиления продукции АФК при гипоксии является увеличение содержания Fe 2+ в цитоплазме. Освобождению ионов железа из белок-связанной формы может способствовать О 2 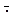
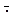
На более поздних стадиях ишемического поражения наблюдается приток в ткань нейтрофилов и других фагоцитирующих клеток, продуцирующих АФК, которые можно считать важными источниками образования активных метаболитов кислорода при гипоксии. Гипоксия непосредственно является одной из причин повышения адгезивных свой ств гр анулоцитов, а повреждение эндотелия сосудов вследствие активации фагоцитирующих клеток крови считают одним из основных факторов патогенеза реперфузионных или реоксигенационных нарушений.
Следует отметить, что на модели ишемии/ реперфузии печени мышей установлена критическая роль в продукции АФК Rac 1-регулируемой НАДФН-оксидазы, отличной от НАДФН-оксидазы фагоцитов.
При патологических состояниях на фоне интенсивной генерации радикальных продуктов снижается АОЗ. Снижение активности ферментов-антиоксидантов может быть связано с мутацией и окислительной деструкцией соответствующих форм ДНК. В то же время сами АФК могут ингибировать активность ферментов-антиоксидантов. Так, Н2О2 тормозит активность СОД, а О 2 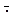
В условиях окислительного стресса наблюдается истощение компонентов неферментативной АОЗ, которые при нейтрализации радикальных продуктов переходят в неактивное состояние или образуют радикальные продукты разной степени токсичности. Процесс восстановления антирадикальной способности этих соединений в условиях оксидативного стресса снижен.
Таким образом, при состоянии оксидативного стресса наблюдаются глубокие изменения в метаболизме белков, липидов, нуклеиновых кислот, углеводов, водно-электролитном обмене, которые могут являться причиной тяжелых поражений тканей при ряде патологических состояний. Оценка интенсивности свободнорадикальных процессов при состоянии оксидативного стресса, их роли в патогенезе ряда заболеваний может быть произведена только при комплексном анализе пр о- и антиоксидантных систем. Более того, в каждом конкретном случае выбор исследуемых звеньев свободнорадикального окисления и компонентов АОС должен быть целенаправленным, необходимым, достаточным и адекватным поставленным задачам. Это особенно важно в клинических и патофизиологических исследованиях.
2. Болдырев А.А. Роль активных форм кислорода в жизнедеятельности нейрона // Успехи физиол. наук. – 2003. – № 3. – С. 21–34.
5. Зенков Н.К., Ланкин В.З., Меньщикова Е.Б. Окислительный стресс. Биохимический и патофизиологический аспекты. – М.: Наука / Интерпериодика, 2001. – 343 с.
12. Drőge W. Free radicals in the physiological control of cell function // Physiol. Rev. – 2002. – V. 82. – P. 47–95.



