Синдром ниймеген у детей что это
Ниймеген синдром
OMIM 251260
Наша команда профессионалов ответит на ваши вопросы
Синдром хромосомных поломок Ниймеген (NBS) – наследственное моногенное заболевание, характеризующееся триадой симптомов: микроцефалия, комбинированный иммунодефицит, повышенная ломкость хромосом. У больных наблюдается микроцефалия, разная степень задержки умственного развития. Отмечаются характерные деформации лицевого скелета по типу «птичьего лица» (скошенный лоб, выступающая средняя часть лица, плохо развитая нижняя челюсть). Эти признаки в разных комбинациях и разной степени выраженности отмечаются у всех больных. Наблюдается задержка физического развития. У многих больных отмечаются признаки врожденного иммунодефицита с первых лет жизни в виде тяжелых хронических пневмоний, синуситов, бронхоэктазов, отитов. Больные страдают частыми инфекциями. NBS наследуется по аутосомно-рецессивному типу.
Ген NBN, мутации в котором приводят к развитию NBS, картирован на хромосоме 8q21. Он имеет длину 50 т.п.н. и состоит из 16 экзонов. Ген кодирует белок, названный нибрином, состоящий из 754 аминокислотных остатков и имеющий молекулярную массу 95 кДа. Нибрин участвует в регуляции клеточного цикла, восстановлении разрывов двухцепочечной ДНК.
У большинства больных найдена одна мутация – 657del5 в экзоне 6 гена NBN. Данная мутация приводит к сдвигу рамки считывания и появлению преждевременного стоп-кодона. При анализе сцепленных с геном NBN полиморфных маркеров обнаружен специфический гаплотип на хромосомах, несущих мутацию 657del5. Данная мутация и гаплотип найдены у представителей славянских народов, что свидетельствует об эффекте основателя. Делеция обнаружена у 90% больных NBS. Популяционная частота носительства в Германии 657del5 1:866, частота заболевания 1:3000000. Кроме мутации 657del5, обнаружены другие мутации как в 6, так и в других экзонах гена NBN, приводящие к развитию NBS.
В Центре Молекулярной Генетики проводится анализ ДНК больных на наличие мутации 657del5.
Синдром Ниймеген
Синдром Ниймеген — это крайне редкое моногенное заболевание с аутосомно-рецессивным типом наследования, которое характеризуется первичным иммунодефицитом, множественными аномалиями. Патология связана с мутацией гена NBN. Основные признаки синдрома Ниймеген: деформация лицевого скелета в виде «птичьего» лица, частые рецидивирующие бактериальные инфекции, микроцефалия, отставание детей в физическом развитии. Диагностика включает иммунологические и генетические исследования. Основу лечения синдрома составляет пожизненная заместительная терапия иммуноглобулинами, также рассматривается вариант инфузии гемопоэтических стволовых клеток.
МКБ-10
Общие сведения
Синдром назван в честь голландского города Ниймеген, где в 1981 г. была впервые описана клиническая картина заболевания. Генные нарушения, лежащие в основе болезни, картированы в 1998 г. В медицинской литературе описано около 150 случаев синдрома. Однако, согласно данным из национальных регистров (чешского, польского), его истинная распространенность намного выше. В основном синдром Ниймеген встречается на территории Восточной Европы, что обусловлено частым носительством мутации среди здорового славянского населения («эффект основателя»). У неславян распространенность патологии составляет 1:3-5 млн. жителей.
Причины
Патология возникает при дефекте гена NBN (NBS1 — Nijmegen breakage syndrome 1), расположенного на длинном плече 8-й хромосомы. Он кодирует образование белка нибрина, участвующего в работе трехмерного протеинового комплекса MRN, в который, кроме нибрина, входят белки MRE11 и RAD50.
Синдром Ниймеген имеет аутосомно-рецессивный характер наследования: при наличии специфического генного дефекта у обоих родителей риск рождения больного ребенка составляет 25%. В парах, где носителем мутировавшего гена является только отец или мать, больные дети не рождаются, однако у половины потомства в кариотипе есть дефектный ген.
Патогенез
Комплекс MRE11/RAD50/NBN, функционирование которого нарушается у детей, страдающих болезнью Ниймеген, отвечает за репарацию ДНК. Белки регулируют восстановление нормальной двуцепочечной структуры генетического материала после повреждения ионизирующим излучением, процессов мейоза и V(D)G-рекомбинации, которые происходят на раннем этапе образования иммунных клеток.
До 90% больных детей славянского происхождения являются гомозиготными по гипоморфной мутации 657del5, то есть у них происходит делеция 5 пар оснований в шестом экзоне гена NBN. При этом синтезируются два аномальных усеченных протеина — р26-нибрин, р70-нибрин, которые не в состоянии обеспечить нормальное функционирование белка.
У больных из неславянских стран (Великобритании, Германии, Голландии, Италии, Канады, Мексики) выявлено еще 11 вариантов повреждения, локализованных не только в 6 экзоне, но и в других участках мутировавшего гена. Учеными доказана обратная связь между показателями экспрессии белка р70 и развитием онкогематологических заболеваний в рамках синдрома Ниймеген.
Симптомы
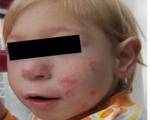
При болезни Ниймеген с рождения отмечаются характерные особенности внешности по типу «птичьего» лица. У детей узкое лицо с высоким лбом, крупный нос, маленькая нижняя челюсть. Также с момента рождения заметны признаки микроцефалии (уменьшенные размеры черепной коробки), часто выявляются расщелины неба, деформации ушных раковин, монголоидный разрез глаз в сочетании с гипертелоризмом.
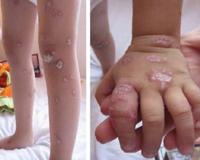
Пороки развития скелета включают клинодактилию, частичную синдактилию, полидактилию, дисплазию тазобедренных суставов. У 50-70% детей определяются дерматологические проявления синдрома: пятна цвета «кофе с молоком», участки витилиго, прогрессирующая депигментация по всему телу.
Патогномоничная особенность синдрома — врожденный дефицит клеточного (Т-лимфоциты) и гуморального (антитела) звеньев иммунитета. Из-за этого с первых месяцев жизни у детей возникают рецидивирующие инфекции дыхательных путей (бронхиты, пневмонии, синуситы), воспалительные болезни уха (отит, мастоидит), бактериальные поражения органов ЖКТ и мочеполовой системы. Реже встречаются вирусные инфекции (цитомегаловирус, вирус Эпштейн-Барр).
Типичны аномалии мочеполовых органов, которые включают гипоплазию/аплазию почек, эктопические почки, уретро-анальную фистулу, у мальчиков зачастую диагностируется крипторхизм, гипоспадия. В мозговой ткани присутствуют арахноидальные кисты, возможно частичное или полное отсутствие мозолистого тела. У детей замедляется физическое развитие, уровень интеллекта в пределах нормы или умеренно снижен.
Осложнения
Наиболее прогностически неблагоприятным последствием синдрома Ниймеген являются злокачественные опухоли, которые диагностируются у 40% детей. Чаще всего поражается лимфоидная ткань: появляются Т- и В-клеточные неходжкинские лимфомы, лимфома Ходжкина, острые лимфобластные лейкозы. Среди солидных неоплазий встречаются медуллобластома, рабдомиосаркома, саркома Юинга. Онкопатология является главной причиной смерти пациентов молодого возраста (до 20 лет).
Особую опасность синдрома Ниймеген представляют рецидивирующие инфекции, которые на фоне иммунодефицита обычно быстро переходят в генерализованные формы. Летальный исход может наступать от септических осложнений. У некоторых детей вследствие затяжных инфекций развивается амилоидоз, вызывающий хроническую почечную недостаточность и заканчивающийся смертью.
Диагностика
О наличии синдрома Ниймеген могут свидетельствовать специфические фенотипические особенности (уменьшенный череп, «птичье» лицо), которые сочетаются с признаками иммунодефицита. Обследованием детей занимается педиатр, для комплексной диагностики привлекают иммунолога-аллерголога, генетика, ортопеда-травматолога. Для подтверждения синдрома назначаются следующие диагностические мероприятия:
Лечение синдрома Ниймеген
Унифицированные протоколы терапии для детей с клиникой синдрома Ниймеген отсутствуют, поскольку на современном этапе развития медицины этиотропное лечение не разработано. Основной задачей врачей является контроль иммунного статуса пациента, предупреждение осложнений, улучшения качества жизни. Для этого используется несколько направлений лечения:
Прогноз и профилактика
Синдром Ниймеген нередко заканчивается смертью пациентов в молодом возрасте от онкопатологии, септических процессов. Однако благодаря интенсивной заместительной терапии иммуноглобулинами, проведению ТГСК удается продлить жизнь больных. Профилактика появления синдрома у детей включает медико-генетическое консультирование пар с отягощенной наследственностью на этапе планирования зачатия, в процессе беременности.
Синдром Ниймеген.
Цель: изучить этиологию, эпидемиологию, диагностику, патогенез и лечение данного синдрома.
Синдром Ниймеген (NBS)– это генетическое заболевание с хромосомной нестабильностью, которое определяется микроцефалией, комбинированным первичным иммунодефицитом, увеличенной чувствительностью к радиоактивному излучению и высокой предрасположенностью к лимфоидным опухолям.
Этиология. Главный фактор развития синдрома Ниймеген у детей – это повреждения, расположенные на 8-й хромосоме гене NBS1, несущие ответственность за синтез такого белка, как нибрин. Этот протеин способен восстанавливать обрывы в ДНК и при его нехватке возобновление ДНК не наблюдается. Собственно, поэтому у ребенка с таким повреждением в генах развиваются симптомы, типичные для синдрома Ниймеген.
Эпидемиология. NBS наиболее распространен в чешской и польской популяциях и практически не обнаруживается у представителей «неславянских» народов (в Германии – 1 на 3 млн).
Патогенез и клиническая картина. Ген NBN кодирует белок- нибрин, который принимает участие в регуляции клеточного цикла, в регенерации разрывов двухцепочечной ДНК. У пациентов обнаруживается микроцефалия, различная степень задержки умственного развития. Замечаются характерные аномалии лицевого скелета по типу «птичьего лица» (скошенный лоб, выступающая средняя часть лица, плохо развитая нижняя челюсть). Эти признаки в всевозможных комбинациях и различной степени эксплицитности встречаются у всех больных. Отмечается задержка физического развития. У большинства больных подчеркиваются признаки врожденного иммунодефицита с первых лет жизни в форме тяжелых хронических пневмоний, синуситов, бронхоэктазов, отитов. Кожные выявления заболевания — это в первую очередь аномалии пигментации: пятна гипо- и гиперпигментации (витилиго и цвет кофе с молоком), псориаз, кожные телеангиоэктазии, пигментные невусы и гемангиомы, саркоидоз с поражением кожи, раннее поседение и выпадение волос. Иногда отмечаются костные недостатки: клинодактилия мизинцев и/или парциальная синдактилия, дисплазия тазобедренных суставов, полидактилия; дефект развития почек, крипторхизм, гипоспадия, агенезия мозолистого тела, арахноидальные кисты, гидроцефалия, гипоплазия трахеи, расщелины губ и неба, атрезия хоан, кардиоваскулярные дефекты. Хромосомная нестабильность содержит специфические транслокации, зачастую выявляемые между локусами генов иммуноглобулинов и TCR на хромосомах 7 и 14. Схожие транслокации свойственны для больных атаксией-телеангиоэктазией и пациентов с синдромом, похожим атаксии-телеангиоэктазии. Больные высокорадиочувствительны, у них высокий риск малигнизации, обнаруживается иммунодефицит (гипогаммаглобулинемия, дефицит синтеза специфических антител и повышенный уровень IgM) и нарушение роста.
Диагностика. Чтобы обнаружить синдром Ниймеген проводятся следующие мероприятия:
разбор жалоб и проявлений заболевания – частые инфекции ЛОР-органов, дыхательных путей, мочеполовой системы;
анализ анамнеза жизни – факты об отставании в росте и весе, склонность к инфекционным заболеваниям;
осмотр больного – «птичье лицо», маленький размер головы, монголоидный разрез глаз, отсутствие верхнего века, аномалии развития пальцев, пятна «кофе с молоком», хрипы в легких, увеличение печени и селезенки;
клинический анализ крови – признаки иммунодефицита (лейкопения, лимфопения);
иммунологические тесты – понижение популяций CD3+, CD19+, CD4+ (клеток иммунной системы), понижение уровня иммуноглобулинов А и G;
Ультразвуковое исследование(УЗИ) – спленомегалия, гепатомегалия;
Отдельное или мультигенетическое тестирование – мутации в гене NBS1.
Лечение. Пациентам с синдромом Ниймеген назначаются симптоматическое лечение, а наблюдение у специалиста должно осуществляться всю жизнь.
Рекомендуется внедрять в рацион продукты, богатые витамином Е и фолиевой кислотой. Кроме этого, эти витамины назначаются в виде БАДов, так как их дефицит наблюдается у всех пациентов с NBS.
Для лечения инфекционных заболеваний назначается стандартный план терапии того или иного недуга, заключающийся в приеме антивирусных, антибактериальных или антимикотических средств. Но в добавок для уравнивания иммунного дефицита больным осуществляют введение иммуноглобулинов IVIg (внутривенно) или SCIg (подкожно).
При онтогенезе лимфоидных опухолей пацинету назначаются протоколы приема химиотерапии. При надобности выполнении облучения выполняется особенная осторожность, так как в литературе имеется описание развития тяжелых осложнений и наступления смертельных исходов в ответ на радиолучевую терапию. Полная клиническая ослабление опухолей в течении 5 лет достигается неоднократно. Однако у ряда пациентов обнаруживаются повторы или развитие других онкологических процессов. Спустя достижения первой ремиссии некоторым больным может выполняться трансплантация гемопоэтических стволовых клеток.
Для предотвращения иммунодефицита при синдроме Неймеген процедуры должны проводиться на протяжении всей жизни больного. Таким пациентам рекомендуется наблюдение у иммунолога и обязательный мониторинг иммунологических биомаркеров. Если у больного наблюдается относительная стабильность, то анализы сдаются не менее одного раза в год. Раз в 3-4 месяца такие тесты выполняются в тех случаях, когда у больного проявляются явные ухудшения в состоянии иммунной системы.
Из-за дефицита IgG многим пациентам рекомендуется гамма-глобулиновая заместительная терапия. Вакцинация живыми или вирусными вакцинами для больных с NBS не проводится.
Журнал «Здоровье ребенка» 4(7) 2007
Вернуться к номеру
Синдром Ниймеген (клиническое наблюдение)
Авторы: Л.Д. НИКОНЕЦ, В.В. ПЕРЕТЯТЬКО, Т.В. ЛЕНАРТ, Ю.В. ЗИБОРОВА, Областная детская клиническая больница, г. Донецк
Версия для печати
В статье представлена клинико-иммунологическая характеристика девочки с NBS из восточной области Украины, установлено гомозиготное носительство мутации 657 del 5 в гене NBS1.
синдром Ниймеген, иммунодефицит.
Синдром Ниймеген (синдром хромосомных поломок Ниймеген, Nijmegen breakage syndrome, NBS) — это синдром хромосомной нестабильности, распространенный у славян, который характеризуется микроцефалией, комбинированным первичным иммунодефицитом, повышенной чувствительностью к радиоактивному излучению и высокой предрасположенностью к лимфоидным опухолям [1]. Синдром Ниймеген входит в группу заболеваний с хромосомной нестабильностью, куда относятся анемия Фанкони, пигментная ксеродерма, синдром Блума и атаксия-телеангиэктазия [2, 9]. Необычное название связано с голландским городом Ниймеген, в университетской клинике которого в 1981 году заболевание было впервые описано Weemaes [3]. Фенотипические отличия синдрома хромосомных поломок Ниймеген — микроцефалия, комбинированный иммунодефицит, характерные изменения лицевого скелета по типу «птичьего» лица: скошенный лоб, гипоплазия нижней челюсти, выступающая вперед средняя часть лица с большим носом. У большинства больных отмечается монголоидный разрез глаз, диспластичные уши, короткая шея, гипертелоризм [4]. Болезнь наследуется по аутосомно-рецессивному типу. Ген синдрома Ниймеген был картирован в длинном плече хромосомы 8 в 1998 г. и назван NBS1. Этот ген кодирует синтез нибрина — белка с молекулярной массой 95 кДа, участвующего в восстановлении разрывов двунитевой ДНК. Нибрин (р95) обеспечивает взаимодействие между двумя белками: h Mre 11 u Rad 50 и контролирует репарацию парных разрывов двуспиральной ДНК, индуцированных ионизирующим излучением или нормальными процессами — мейотическими реакциями и митотической VDG реаранжировкой в зрелых лимфоцитах [5]. На основе восстановленной впоследствии ДНК обеспечивается синтез разнообразных специфических антител, Т-клеточных рецепторов. Синтез антител и рецепторов обеспечивает не только сам по себе иммунный ответ, но и созревание Т- и В-лимфоцитов. Двунитевые разрывы ДНК также регулярно возникают в процессе кроссинговера при мейозе (пациенты с атаксией-телеангиэктазией страдают бесплодием [6], вызванным недостаточностью функций яичников). Процессы, напоминающие рекомбинацию генов иммуноглобулинов у пациентов с синдромом Ниймеген, происходят при созревании нейронов головного мозга, что, вероятно, и вызывает микроцефалию, умственные нарушения [7].
Из 55 больных, описанных в регистре синдрома Ниймеген, 44 являются носителями одной и той же мутации в гене NBS1 — делеции 5 пар оснований в экзоне 6 гена NBS1 — 657 del 5 или 657–661 del АСААА. Эта мутация приводит к сдвигу рамки считывания и появлению преждевременного стоп-кодона, что определяет полное отсутствие синтеза нибрина [4, 5]. Данная мутация гена NBS1 выявлена у 90 % больных с этим синдромом, и все больные — славяне [6].
Кроме того, при этом заболевании описано еще 5 спонтанных мутаций, которые встречаются и описаны в Германии, Канаде, Италии, Мексике, Англии, Голландии, России [8].
Эти 5 мутаций, возникающие при синдроме Ниймеген, располагаются как в 6-м, так и в других экзонах и описаны лишь у отдельных семей. Высказывается предположение о существовании мутаций, ведущих к инактивации нибрина или к снижению его синтеза, что ведет к более мягким фенотипическим проявлениям.
Одним из основных клинических проявлений NBS являются рецидивирующие инфекции с 2–3-летнего возраста: частые OРВИ, реже — отиты, энтероколиты, инфекции мочевой системы, стоматиты, хронический бронхит, что связано с дефектами в гуморальном и клеточном звеньях иммунитета. Выявляют умеренную лейкопению и лимфопению. Снижены количество клеток CD3+, CD19+, CD4+, соотношение CD4+/CD8+, уровни IgA, IgG, возможны дефицит субкласса IgG2.
Отмечается высокая частота онкозаболеваний: у 60 % больных в Польском и 73 % в Чешском национальных реестрах NBS. Риск возникновения онкозаболеваний у больных с NBS в 50 раз выше, чем среднепопуляционный, лимфомы — в 1000 раз выше, чем в среднем в популяции [1]. Большинство опухолей лимфоидных органов возникают в возрасте до 20 лет: неходжкинские лимфомы, лимфобластный лейкоз, лимфома Ходжкина. Описаны острый миелобластный лейкоз, миомы, менингиомы, медуллобластомы, нейробластомы, рабдомиосаркомы, гонадобластомы, рак кишечника, саркома Юинга.
Кожные проявления заболевания — это в первую очередь аномалии пигментации: пятна гипо- и гиперпигментации (витилиго и цвет кофе с молоком), псориаз, кожные телеангиэктазии, пигментные невусы и гемангиомы, саркоидоз с поражением кожи, раннее поседение и выпадение волос [1].
Иногда наблюдаются костные дефекты: клинодактилия мизинцев и/или парциальная синдактилия, дисплазия тазобедренных суставов, полидактилия; пороки развития почек, крипторхизм, гипоспадия, агенезия мозолистого тела, арахноидальные кисты, гидроцефалия, гипоплазия трахеи, расщелины губ и неба, атрезия хоан, кардиоваскулярные дефекты.
При цитогенетическом обследовании выявляют аберрации хромосом.
Больным с NBS необходимо ограничивать лучевые нагрузки, в том числе рентгенологические обследования. Компьютерная томография противопоказана. Методом выбора является магнитно-резонансная томография.
Лечение больных с синдромом NBS включает заместительную терапию внутривенными иммуноглобулинами при уровне IgG меньше 2,5–3,0 г/л. Детям с дефицитом IgG2 внутривенные иммуноглобулины назначают в дозе 400–600 мг/кг 1 раз в месяц. Больным с рецидивирующими и хроническими инфекциями респираторного тракта назначают постоянные или периодические курсы антибиотикотерапии.
Больная А., 11 лет. Родилась от 8-й беременности, третьих срочных родов с массой 2900 г. Прародители по материнской линии с Волыни. Мать, отец, старшая сестра здоровы. Старший брат с микроцефалией умер в 7 лет от лимфосаркомы. У бабушки по материнской линии был рак пищевода, у деда — рак легких, у дяди — рак желудка.
Больная отставала в физическом развитии с первого года жизни. Была привита по возрасту без реакций и осложнений. Реакции Манту отрицательные. После вакцинации и ревакцинации БЦЖ рубца нет. В 8 месяцев диагностирована микроцефалия, фурункулез, диарея. С 3 лет болела рецидивирующими бронхитами. С 5 лет постоянный кашель. С 6 лет — рецидивирующие ячмени. С 7 лет — артриты коленных, локтевых, лучезапястных, голеностопных суставов. В 9 лет перенесла гнойный эндобронхит, хронический колит. Тогда же впервые исследованы гуморальный и клеточный иммунитет: IgG — 3,4 г/л, IgA — 1,1 г/л, IgM — 0,5 г/л, СД3+ — 1190 кл/мл, СД4+ — 770 кл/мл, СД8+ — 390 кл/мл, СД22+ — 300 кл/мл, СД4+/СД8+ — 1,94.
В 11 лет больная обследована в Донецкой областной детской клинической больнице. Состояние тяжелое из-за дыхательной недостаточности. Отстает в физическом развитии: масса 18 кг, рост 126 см. Микроцефалия, «птичье» лицо. На спине 3 пигментных пятна цвета кофе с молоком. На туловище, конечностях келлоидные рубцы после ожогов. Ногтевые пластинки по типу «часовых стекол», фаланги пальцев кистей по типу «барабанных палочек». Межфаланговые суставы кистей, пястно-фаланговые, коленные, локтевые суставы увеличены в диаметре, отечные, деформированы, движения в них болезненны и ограничены. Над суставами кистей цианоз кожи с атрофией в центре (проявления васкулита). Небные миндалины, периферические лимфоузлы гипоплазированы. Дыхание жесткое с множеством крепитирующих и мелко-пузырчатых влажных хрипов. Одышка смешанного характера. Тоны сердца приглушены, тахикардия. Печень и селезенка выступают из подреберья на 1,0 см. Стул и мочеиспусканин не нарушены.
Общий анализ крови без особенностей.
Иммунограмма: IgG — 0,18–0,44 г/л, IgA — 0,65–0,01 г/л, IgM — 0,6–1,3 г/л, СД3+ — 1440 кл/мл, СД4+ — 560 кл/мл, СД8+ — 540 кл/мл, СД22+ — 120 кл/мл, СД4+/СД8+ — 1,0.
Повышен уровень острофазовых белков, лейкоцитурия.
Рентгенография органов грудной клетки: хронический бронхит; придаточных пазух носа: двусторонний гаймороэтмоидит.
Спиральная компьютерная томография легких: изменения в легких обусловлены интерстициальным процессом, фиброз S5 правого легкого и язычкового сегмента левого легкого.
Спиральная компьютерная томография головного мозга: гипоплазия вещества головного мозга.
УЗИ органов брюшной полости: гепатоспленомегалия, почки без патологии.
ЭхоКГ: недостаточность клапанов легочной артерии, недостаточность трехстворчатого клапана.
Молекулярно-генетическое обследование проведено в Институте наследственной патологии г. Львова: гомозигота по мутации 657 del 5 экзона 6 гена NBS1.
Больная получала следующее лечение: заместительную терапию донорскими иммуноглобулинами, антибиотикотерапию, нестероидные противовоспалительные средства, муколитики.
1. Костюченко Л.В., Акопян Г.Р., Поліщук Р.С. та ін. Синдром Ніймегена: клінічна характеристика, діагностика та можливості терапії // Перинатология и педиатрия. — 2005. — № 1/2 (23). — С.105-111.
2. Shilon J. // Ann. Rev. Jenet. — 1997. — Vol. 31. — P. 635-662.
3. Weemaes C.M., Hustinx T.Y., Scheres J.M. et al. // Acta Paediat. Scand. — 1981. — Vol. 70. — P. 557-564.
4. Varon R., Vissinga C., Platzer M. et al. // Cell. — 1998. — Vol. 93. — P. 467-476.
5. Carney J.P., Maser R.S. Olivares H. et al. // Rad 50 protein complex and Nijmegen breakage syndrome: linkage of double-strand break repair to the cellular DNA damage response // Cell. — 1998. — Vol. 93, № 3. — P. 477-486.
6. The International Nijmegen Breakage Syndrome Study Group // Arch. Dis. Child. — 2000. — Vol. 82. — P. 400-406.
7. Gao J., Sun J., Frank K. M. et al. // Cell. — 1988. — Vol. 95. — P. 891-902.
8. Resnick I., Kondratenko I., Togoev O. et al. // International Workshope on Nijmegen Breakage Syndrome. — Chestochowa, 2000. — P. 9.








2007/118/1_25.png)
2007/118/2_25.jpg)