Синдром пьера робена что это
Синдром пьера робена что это
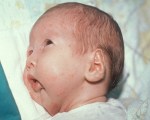
Синдром Пьера Робена — это врожденный порок развития, проявляющийся тремя основными признаками: расщелина нёба, недоразвитие нижней челюсти, «западение» языка.
У новорожденных и грудных детей этот синдром часто сопровождается нарушением двух важнейших функций:
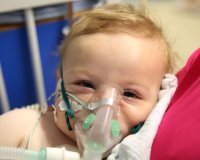
1. Дыхания: на вдохе ребенок хрипит с втяжениями грудной клетки. Иногда ребенок не может дышать вообще и тогда в роддоме ребенку в трахею устанавливают интубационную трубку для обеспечения дыхания. Общее название такого нарушения дыхания — синдром обструктивного апноэ, который является жизнеугрожающим состоянием и может быть причиной синдрома внезапной смерти.
2. Глотания. При этом питание может осуществляться только через желудочный зонд.
Важно отметить, что синдром обструктивного апноэ может наблюдаться и у детей более старших возрастов при заболеваниях, которые сопровождаются недоразвитием костей лицевого скелета: синдромы Франческетти (Тричера-Коллинза), I-II жаберных дуг (гемифациальная микросомия, синдром Гольденхара), Апера, Крузона и др.; артрозах и анкилозах височно-нижнечелюстных суставов, сопровождающихся недоразвитием нижней челюсти.
С такими нарушениями новорожденные дети прямо из родильного отделения переводятся в отделение реанимации, где проводится длительное выхаживание ребенка.
Между тем, длительное пребывание ребенка на трубке и зондовом питании чревато развитием пневмонии, ослаблением глотательного рефлекса. А срок выхаживания может быть неопределенно долгим, пока ребенок не вырастет и просвет верхних дыхательных путей позволит ему самостоятельно дышать и питаться (обычно к 5-6 месяцам).
При синдроме Пьера Робена всему виной недоразвитие (укорочение) нижней челюсти, из-за чего язык смещен назад и перекрывает просвет дыхательных путей (рис. 1). Если удлинить нижнюю челюсть, то язык переместится за ней вперед и откроет дыхательные пути (рис. 2).
Существует метод, позволяющий удлинить нижнюю челюсть — компрессионно-дистракционный остеосинтез.
Метод заключается в том, что на нижнюю челюсть с 2-х сторон устанавливаются аппараты, проводятся распилы челюсти между лапками аппаратов и фрагменты челюсти плотно прижимаются друг к другу — компрессия (рис. 3). С 5-6 суток после операции фрагменты челюсти постепенно, со скоростью 1 миллиметр в сутки, разводятся аппаратами на необходимую величину. Процесс удлинения челюсти аппаратами называется дистракцией, а аппарат соответственно — компрессионно-дистракционным. Между фрагментами кости образуется новая молодая кость — костная мозоль (рис. 4).
Операция проводится под интубационным наркозом. Такое оперативное лечение у новорожденных и младенцев проводится по жизненным показаниям.
Самостоятельное дыхание становится возможным в среднем уже на 4-6 сутки дистракции, которая продолжается до достижения правильного соотношения челюстей. На самостоятельное питание ребенок переводится, как правило, к моменту окончания дистракции или немного позже.
Ребенок выписывается с аппаратами на время (3 месяца) превращения костной мозоли в полноценную кость. Через 3 месяца — повторная госпитализация для удаления аппаратов, которое также проводится под наркозом.
Поскольку страховой полис и финансирование больницы не покрывают стоимость аппаратов, их необходимо приобретать отдельно. Их стоимость — 250-300 € за аппарат отечественного предприятия КОНМЕТ и 1200-1500 € за аппарат немецкого предприятия MARTIN. Все остальное лечение (в том числе и операция) проводятся бесплатно.
Клинический пример
В отделение реанимации из родильного дома поступил ребенок 2-х недель жизни с диагнозом синдром Пьера Робена, синдром обструктивного апноэ тяжелой степени. Питание может осуществляться только через зонд. У ребенка имеется дефицит веса. В связи с выраженными нарушениями дыхания и питания ребенку проведен компрессионно-дистракционный остеосинтез нижней челюсти.
После окончания дистракции ребенок выписан на самостоятельном дыхании и питании.
C возраста 1-1,5 года таким детям проводится уранопластика — операция по устранению расщелины неба. Лечение (в том числе и операция) проводится бесплатно.
Синдром Пьера Робена – это генетически обусловленная аномалия, характеризующаяся гипоплазией нижней челюсти, небной расщелиной и глоссоптозом. Комбинация пороков ЧЛО вызывает затруднения при вскармливании, обструктивное апноэ, диффузный цианоз, риск аспирации пищи и асфиксии. Патология диагностируется по данным рентгенографии и КТ челюсти, фиброларингоскопии, полисомнографии, генодиагностики. Консервативная тактика включает позиционную терапию, СРАР, ортодонтическое лечение. Методы хирургической коррекции порока представлены глоссопексией, пластикой неба, компрессионно-дистракционным остеосинтезом.
МКБ-10
Общие сведения
Синдром (последовательность, аномалия) Робена включает триаду признаков: микрогнатию, глоссоптоз, расщепление твердого и мягкого неба. Врожденная анатомическая деформация описана в 1923 г. французским зубным врачом Пьером Робеном. По разным оценкам, дети с данной аномалией рождаются с популяционной частотой 1:8500-30000, независимо от пола. Ведущей проблемой младенцев с синдромом Робена является обструкция верхних дыхательных путей и критическое нарушение дыхания вследствие недоразвития нижней челюсти и смещения мягких тканей вглубь полости рта.
Причины
Последовательность Пьера Робена может встречаться как изолированный синдром (20-40%) или как часть других генетических патологий. В первом случае челюстно-лицевая аномалия формируется под влиянием неблагоприятных условий внутриутробного развития, в числе которых может быть:
Кроме этого, аномалия Пьера Робена встречается в структуре генетических синдромов с множественными пороками развития. Всего насчитывается порядка 300 таких заболеваний, среди которых синдромы Стиклера, Хангарта, Эдвардса, кампомелическая дисплазия и др. Более чем в 30% случаев синдром Пьера Робена сочетается с ВПС, скелетными аномалиями, дефектами развития глаз и ушных раковин.
Спорадические случаи возникают в результате генетических мутаций de novo. Синдромальная последовательность наследуется по тому же принципу, что и патология, с которой она ассоциирована (сообщается об аутосомно-рецессивном, аутосомно-доминантном, Х-сцепленном варианте). Согласно исследованиям, генетические мутации затрагивают области хромосом 2 (2q24.1-33.3), 4 (4q32-qter), 11 (11q21-q23.1) и 17 (17q21-q24.3).
Патогенез
Синдром Пьера Робена принято называть «последовательностью», поскольку его признаки представляют собой цепочку взаимовлияющих друг на друга событий. Нарушение развития нижней челюсти у плода происходит в период между 7-й и 11-й неделями гестации под воздействием генетических мутаций или экзогенных факторов. Гипоплазия челюсти способствует неправильному положению языка между небными пластинками, которое препятствует их своевременному закрытию и вызывает образование расщелины.
Нижняя ретрогнатия и маленький объем ротовой полости создают условия для смещения языка в сторону задней стенки глотки и возникновения глоссоптоза. Оттянутый назад язык вызывает у новорожденного серьезные затруднения дыхания, вследствие чего часто возникает инспираторная обструкция ВДП.
Классификация
В зависимости от выраженности нарушения глотания и дыхания выделяют три степени тяжести синдрома Пьера Робена:
Симптомы
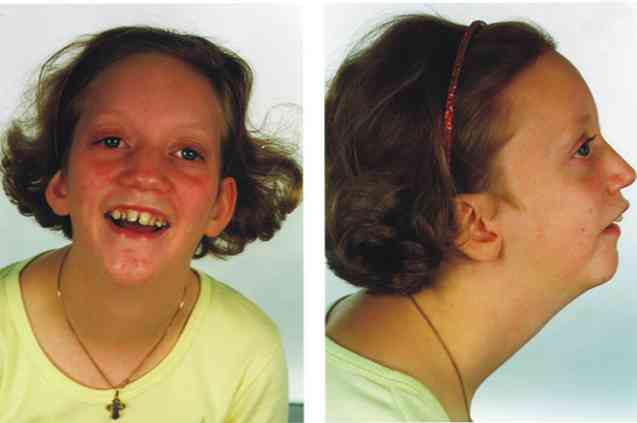
Новорожденные с синдромом Пьера Робена имеют характерное «птичье» лицо, обусловленное гипоплазией нижней челюсти (микрогнатия) и ее смещением назад (ретрогнатия). Объем полости рта полости уменьшен, язык оттянут вглубь (глоссоптоз). Как правило, у пациентов обнаруживается U-образная субмукозная расщелина мягкого неба, также встречается готическое небо.
Смещение языка кзади вызывает проблемы с сосанием в раннем возрасте, из-за чего у ребенка отмечается задержка роста и набора веса, отставание в моторном развитии. Тяжесть дыхательных нарушений варьируется от храпа до опасных эпизодов обструктивного апноэ. В легких случаях дыхательные расстройства возникают только в положении на спине и при беспокойстве ребенка, проходят самостоятельно. В более серьезных ситуациях приступы остановки дыхания длительные (до 20 сек. и более), приводящие к развитию гипоксии и гиперкапнии.
Тяжелые эпизоды апноэ сопровождаются акроцианозом или диффузным цианозом. Постоянная задействованность вспомогательных дыхательных мышц способствует формированию воронкообразной деформации грудной клетки.
Синдромальная последовательность Пьера Робена, как правило, сочетается с врожденными аномалиями других органов: тугоухостью и недоразвитием слухового аппарата, патологией зрительного анализатора (близорукость, катаракта), скелетными деформациями (полидактилия, врожденные ампутации), сердечными пороками. Примерно у половины пациентов обнаруживаются дефекты ЦНС: микроцефалия, гидроцефалия, эпилепсия, задержка психоречевого развития, олигофрения.
Осложнения
Практически все дети с синдромом Пьера Робена страдают речевыми дефектами (открытая ринолалия), нарушением прикуса, рецидивирующими ушными инфекциями. На фоне пролонгированных приступов обструктивного апноэ постепенно формируется гипоксическая энцефалопатия, легочное сердце. В некоторых случаях ребенок может погибнуть от асфиксии. Дисфагические расстройства могут повлечь за собой аспирацию слюны, пищи, желудочного содержимого при срыгивании, что чревато развитием аспирационной пневмонии. Смертность детей составляет порядка 16%, а при наличии сочетанных пороков достигает 41%.
Диагностика
В настоящее время синдром Пьера Робена диагностируется пренатально с помощью скринингового УЗИ в 11-12 недель беременности. После рождения диагноз подтверждается данными клинической картины и инструментальных исследований. Необходимая диагностика:
Лечение синдрома Пьера Робена
Лечебная тактика при аномалии Робена зависит от выраженности респираторных и дисфагических расстройств. Она может заключаться в проведении позиционной терапии, вспомогательной терапии, хирургического лечения. На различных этапах жизни ребенку требуется сопровождение врача-отоларинголога, челюстно-лицевого хирурга, ортодонта, логопеда.
Консервативное лечение
При легкой степени дыхательной обструкции рекомендуется постуральная терапия. Ребенка выкладывают на живот или на бок с приподнятой или зафиксированной головой, обеспечивающей выдвижение вперед языка и нижней челюсти. Персистирующая обструкция может купироваться с помощью назофарингеального воздуховода. Одним из методов с подтвержденной эффективностью является СРАР-терапия, позволяющая осуществлять неинвазивную масочную вентиляцию под постоянным положительным давлением.
При невозможности самостоятельного питания кормление ребенка производится через назогастральный зонд. Тяжелые степени синдрома Пьера Робена требуют установки трахеостомы или интубации трахеи с подключением ребенка к аппарату ИВЛ.
Консервативные методы позволяют купировать симптомы, но ни один из них не устраняет имеющиеся врожденные аномалии. Поэтому такое лечение должно проводиться очень длительно, до тех пор, пока размеры дыхательных путей ребенка не позволят ему дышать самостоятельно без риска обструкции. После нормализации жизненных функций проводится ортодонтическое лечение, логопедическая коррекция.
Хирургическое лечение
Устранение небной расщелины проводится поэтапно: велофарингопластика выполняется в 6-8 мес., уранопластика – в 12-18 мес. В качестве временной меры при подготовке к радикальному лечению может осуществляться глоссопексия – фиксация языка к нижней губе, альвеолярному отростку. Ранее применявшиеся методы вытяжения нижней челюсти, транспозиции жевательных мышц не являются достаточно эффективными.
Радикальным хирургическим вмешательством, позволяющим удлинить нижнюю челюсть, является компрессионно-дистракционный остеосинтез. Операция заключается в проведении двусторонней остеотомии нижней челюсти с фиксацией на костных фрагментах специального аппарата. Активация устройства обеспечивает постепенное перемещение нижней челюсти вместе с комплексом мягких тканей дна полости рта кпереди. Процесс дистракции занимает около 3-х месяцев, в результате чего становится возможным сначала самостоятельное дыхание, а затем – питание.
Прогноз и профилактика
Изолированный синдром Робена имеет более благоприятный прогноз, чем синдромальные формы, ассоциированные с множественными пороками и умственной отсталостью. Также существенное значение имеет своевременность и радикальность лечения. Вместе с тем, на данный момент смертность от асфиксии, других осложнений и сопутствующих аномалий остается достаточно высокой.
Для снижения риска рождения ребенка с синдром Пьера Робена рекомендуется не допускать воздействия тератогенов, инфицирования, дефицита микронутриентов в период гестации. Беременным необходимо вовремя проходить генетические и ультразвуковые пренатальные скрининги.
Синдром Пьера Робена Симптомы, причины, лечение
Синдром Пьера Робина (SPR), также известная как последовательность Пьера Робина, представляет собой расстройство генетического происхождения, классифицируемое как черепно-лицевые синдромы или патологии (Arancibia, 2006).
Клинически синдром Пьера Робена характеризуется тремя основными клиническими признаками: микрогнатия, глоссоптоз и обструкция верхних дыхательных путей и переменное наличие расщелины неба (Sridhar Reddy, 2016).
Что касается этиологического происхождения этой патологии, синдром Пьера-Робена обусловлен наличием специфических мутаций в гене SOX9, большинство из которых диагностированы (Genetics Home Reference, 2016).
В целом, этот синдром вызывает важные медицинские осложнения, в том числе дыхательную недостаточность, проблемы с пищеварением животных или развитие других черепно-лицевых пороков развития (Ассоциация аномалий и порочно-лицевых пороков развития, 2016).
С другой стороны, диагноз синдрома Пьера-Робина обычно не подтверждается до момента рождения, в дополнение к клиническим данным важно выполнять различные рентгенологические тесты для выявления изменений кости (Pierre Robin Australia, 2016).
В настоящее время не существует никакого лечения синдрома Пьера Робина, однако, хирургические подходы часто используются для коррекции опорно-двигательного расстройства. Кроме того, респираторная и желудочно-кишечная адаптации важны для предотвращения опасных для жизни медицинских осложнений (Rethe, Rayyan, Shoenaers, Dormaar, Breuls, Verdonck, Devriednt, Vander Poorten and Hens, 2015)..
Характеристика синдрома Пьера Робина
Кроме того, в медицинской литературе мы можем выделить различные термины, используемые в контексте синдрома Пьера Робина: болезнь Пьера Робина, порок развития Пьера Робина или последовательность Пьера Робина (Национальная черепно-лицевая ассоциация, 2016).
На определенном уровне этот синдром был описан в 1891 году Менерадом и Ланнелонгом. В клинических отчетах они описали двух пациентов, клиническое течение которых характеризовалось наличием недоразвития структуры нижней челюсти, расщелины неба и смещения или ретракции языка (Arancibia, 2006).
Однако только в 1923 году Пьер Робин описал клинический спектр этой патологии, сосредоточив свои исследования на случае ребенка, страдающего аномалией нижней челюсти, аномально большим языком и значительными респираторными проблемами (Детская черепно-лицевая ассоциация, 2016 ).
Хотя эта патология в основном отличается черепно-лицевыми рентгенологическими данными, она характеризуется высокой подвижностью, связанной с медицинскими осложнениями, в основном связанными с сердечной недостаточностью и проблемами с питанием..
В частности, синдром Пьера Робина характеризуется высокой смертностью, связанной с обструкцией дыхательных путей, неврологическими нарушениями или изменениями в сердце (Sridhar Reddy, 2016)..
С другой стороны, многие авторы предпочитают называть эту патологию только последовательностью Пьера, поскольку именно аномалии нижней челюсти приводят к появлению остальных типичных признаков и симптомов (Pierre Robin Australia, 2016).
частота
Распространенность синдрома Пьера Робина оценивается примерно в одном случае на 8500 детей, родившихся живыми, из которых более 80% диагностированных случаев связаны с другими медицинскими осложнениями и специфическими синдромами (Arancibia, 2006).
С другой стороны, в случае США заболеваемость синдромом Пьера Робина составляет 1 случай на 3120 рождений в год (Lee, Thottam, Ford and Jabbour, 2015).
В настоящее время не выявлено различий в распространенности синдрома Пьера Робина, связанного с полом, происхождением, географией или конкретными этническими и расовыми группами..
Кроме того, как мы указывали ранее, синдром Пьера Робена представляет собой одну из черепно-лицевых патологий с высокой вероятностью смертности. В Соединенных Штатах приблизительно 16,6% пострадавших умирают из-за развития медицинских осложнений (Lee, Thottam, Ford and Jabbour, 2015).
По порядку возникновения наиболее частыми вторичными медицинскими патологиями являются: сердечные аномалии (39%), изменения в центральной нервной системе (33%) и аномалии в других органах (24%) (Lee, Thottam, Ford and Jabbour, 2015).
Признаки и симптомы
Последовательность Пьера Робена отличается от других типов черепно-лицевой патологии наличием трех основных клинических признаков: микрогнатия, глоссоптоз и волчья пасть (Детская черепно-лицевая ассоциация, 2016, Genetics Home reference, 2016, Rehté et al., 2015):
micrognatia
Под термином микрогнатия мы подразумеваем наличие патологического изменения развития структуры нижней челюсти, в частности, окончательная форма имеет уменьшенный размер по сравнению с ожидаемой для уровня развития пораженного человека..
Как следствие, неполное развитие этой черепно-лицевой структуры вызовет широкий спектр изменений, связанных с наличием пороков развития, которые влияют на рот и лицо.
Микрогнатия является медицинским признаком, присутствующим примерно у 91% людей, страдающих синдромом Пьера Робина.
glossoptosis
Под термином глоссоптоз мы подразумеваем наличие аномальной ретракции положения языка в структуре полости рта, в частности, языки должны быть размещены за нормальным продуктом микрофотографии и уменьшением объема полости рта..
Аномалии, связанные с положением и структурой языка, могут вызвать серьезные проблемы с питанием, которые могут привести к серьезным заболеваниям..
Кроме того, в других случаях также можно идентифицировать аномально большой язык (макроглоссия), который, среди прочего, затрудняет дыхание, жевание или выработку функционального языка..
Кроме того, глоссоптоз является одним из наиболее частых клинических признаков синдрома Пьера Робина, наблюдаемых примерно в 70-85% диагностированных случаев. В то время как макроглоссия может наблюдаться в меньшем количестве, примерно у 10-15% пострадавших.
Волчья пасть
Этот термин относится к наличию уродства в небных или ротовых областях крыши, то есть может наблюдаться наличие трещин или отверстий, связанных с неполным развитием нижней челюсти.
Как и другие клинические данные, расщелина неба вызовет значительные изменения в диете.
В дополнение к этим признакам и симптомам, также можно определить другие типы изменений, среди которых включены (Arancibia, 2006, Rehté et al., 2015):
— Пороки развития носа.
— Изменения и скелетно-мышечные дефекты, в основном связанные с развитием oligodactyly (сокращение числа пальцев, менее чем 5 или пальцев ноги) клинодактилией (поперечное отклонение положения пальцев), полидактильный (увеличение числа пальцев), hiperlaxity суставы (аномально преувеличенное увеличение подвижности суставов), дисплазия в фалангах (фаланги с недостаточным или неполным развитием костей) или синдактилия (слияние нескольких пальцев)
— Другие изменения: также возможно выявить пороки развития в структуре конечностей или в позвоночнике.
Наиболее частые медицинские осложнения
В дополнение к медицинским функциям, перечисленным выше, могут появляться и другие, связанные с несколькими системами (Arancibia, 2006, Детская черепно-лицевая ассоциация, 2016, Genetics Home reference, 2016, Rehté et al., 2015):
Сердечные изменения
Сердечные изменения представляют собой одно из медицинских осложнений, оказывающих большее влияние на здоровье человека и представляющих важные риски для его выживания. Однако признаки и симптомы, связанные с сердечно-сосудистой системой, обычно поддаются лечению с помощью фармакологического и / или хирургического подхода..
Некоторые из наиболее частых сердечных аномалий включают стеноз сердца, постоянное овальное отверстие, изменение артериальной перегородки или гипертонию..
Неврологические изменения
Генетическое происхождение синдрома Пьера Робена может также включать развитие различных неврологических расстройств, в основном связанных с наличием аномалий центральной нервной системы (ЦНС)..
Таким образом, некоторые из неврологических расстройств, связанных с синдромом Пьера Робина, могут включать гидроцефалию, порок развития Киари, эпилептические эпизоды или задержку в приобретении психомоторных навыков..
Респираторные расстройства
Таким образом, во многих случаях требуется хирургическая коррекция, чтобы освободить дыхательные пути, главным образом коррекция дисплазии нижней челюсти или положение языка.
Силовые аномалии
Как и в случае респираторных расстройств, проблемы с питанием возникают в основном из-за пороков развития нижней челюсти.
Поэтому с самого рождения важно выявить те аномалии, которые затрудняют кормление, чтобы исправить их и, следовательно, снизить вероятность развития медицинских патологий, связанных с недоеданием..
причины
Синдром или последовательность Пьера Робина, имеет генетическое этиологическое происхождение, связанное с изменениями в гене SOX9. Хотя эта аномалия была выявлена в большинстве единичных случаев синдрома Пьера Робина, некоторые из ее клинических характеристик могут быть связаны с другим типом генетических мутаций (Genetics Home Reference, 2016)..
В частности, ген SOX9 играет фундаментальную роль пропорциональных биохимических инструкций, необходимых для производства белка, участвующего в развитии и формировании различных тканей и органов во время развития плода (Genetics Home Reference, 2016).
Кроме того, текущие исследования показывают, что белок SOX9 может регулировать активность других типов генов, особенно тех, которые участвуют в развитии структуры скелета и, следовательно, нижней челюсти (Genetics Home Reference, 2016).
В результате генетические изменения препятствуют адекватному морфологическому развитию определенных структур и, следовательно, появляются кардинальные клинические признаки: микогнатия, глоссоптоз и волчья пасть.
диагностика
Во многих случаях черепно-лицевые структурные пороки развития могут быть выявлены во время беременности с помощью ультразвука, хотя случаи редки.
В этом смысле чаще всего подозрение на синдром Пьера Робина возникает в постнатальном или детском периоде. У многих из тех, кто пострадал, структуры признаков значительно очевидны, поэтому диагноз подтверждается рентгенологическими исследованиями и физическим осмотром..
Тем не менее, в другом случае необходимо предварительно провести респираторное исследование, а затем рентгенологическое исследование, чтобы определить наличие этого синдрома..
Кроме того, другим фундаментальным аспектом в диагностике этой патологии является исследование других областей, особенно сердечной и нервной системы, поскольку могут появиться другие виды опасных для жизни аномалий..
Наконец, диагностическое вмешательство может включать индивидуальное и семейное генетическое исследование для выявления возможных генетических ассоциаций.
лечение
Типичное лечение синдрома Пьера Робина основано на хирургических вмешательствах для коррекции черепно-лицевых пороков развития (Arancibia, 2006):
— Закрытие небных расщелин.
Кроме того, другие фармакологические подходы также используются для лечения патологий сердца, эпилептических эпизодов и других неврологических явлений..
Кроме того, у затронутых людей обычно возникают трудности, связанные с производством языка, поэтому во многих случаях ранний логопедический подход имеет важное значение.