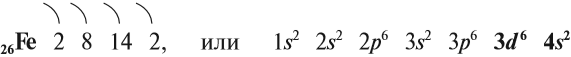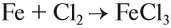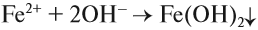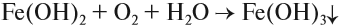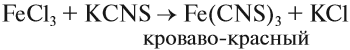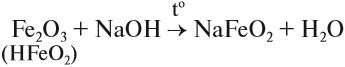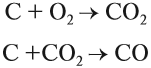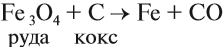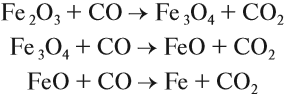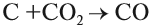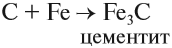Соединения железа в степени окисления 2 проявляют как окислительные так и восстановительные
Металлы VIII группы 4 подгруппы (Fe, Co, Ni)
Железо (Ferrum)
История получения
Железо в старину получали «сыродутным» способом. Железную руду и уголь загружали в печи, имевшие форму длинной трубы. Уголь поджигали, а ветер, дующий в трубу, поддерживал высокую температуру (около 1400 о С), необходимую для восстановления железа из оксидной руды. Полученный металл (крицу) ковали, в процессе ковки от него отделялись куски шлака, и оставалось чистое железо. В некоторых странах этим способом выплавляли металл до XVIII в.
В Средние века благодаря использованию воздушных мехов температуру внутри печей удалось повысить настолько, что металл в них плавился. Чистое железо плавится при 1535 о С, но при содержании всего 4,3% углерода температура плавления снижается до 1135 о С. Расплавленный металл не только растворял значительное количество углерода, но и взаимодействовал с ним с образованием карбида Fe3C (цементита). При охлаждении расплава избыточный углерод кристаллизовался в виде графита. Так вместо ковкого железа люди получили чугун – сплав, содержащий 2,5 – 5% углерода. Чугун использовали для литья пушек, ядер и даже для изготовления посуды. В отличие от железа, чугун хрупок, как стекло. Чтобы сделать его ковким, надо было снизить содержание углерода до 0,3 – 1,7%. Для этого над расплавленным чугуном пропускали воздух, и углерод выгорал, образуя оксиды СО и СО2. Чугун превращался в сталь.
Казалось бы, подобная технология не могла обеспечить высокого качества металла. И всё же именно таким способом на Востоке получали знаменитую дамасскую сталь! Секрет дамасской стали оберегался настолько тщательно, что раскрыть его удалось только в конце XIX в. И он заключается не в специальных добавках, а в особенностях обработки. При выплавке такой стали нужен хороший доступ воздуха, чтобы все примеси серы, кремния и фосфора перешли в шлаки. А затем плав необходимо очень медленно охлаждать. Тогда процесс затвердевания сопровождается образованием разветвленных кристаллов-дендритов, что делает сталь вязкой и тугоплавкой, а пространство между ними заполняется богатыми углеродом компонентами, имеющими очень высокую твёрдость.

В наши дни чугун выплавляют из руды в специальных печах – домнах, а чтобы получить из него сталь, используют установки, называемые конверторами. В конвекторах через расплавленный чугун с добавками руды или ржавого металлического лома продувают воздух. При этом углерод окисляется до угарного газа, который восстанавливает оксид железа (руду и прокалённую ржавчину) до металла:
Но и железо также частично окисляется до оксида FeO. После того как все примеси, содержавшиеся в чугуне, окислились кислородом, в сталь вводят раскислители – активные металлы (Mn, Al, La), которые восстанавливают FeO до металла. Образующиеся при этом оксиды реагируют с кремнезёмом, превращаясь в шлаки:
В последнее время всё большее применение находит гораздо более экономичный «прямой» метод получения железа. Он основан на восстановлении оксидов железа природным газом (метаном):
Затем железо переплавляют в электропечах, при необходимости вводя легирующие добавки, в основном хром или марганец. Таким образом можно получать сталь высокого качества, минуя стадии выплавки чугуна и его передела.
Получить железо – это полдела. Следующая задача – защитить металл от коррозии. Ежегодно от нее «погибает» 15-20% всех изделий из железа. Железо – активный металл, и на влажном воздухе оно окисляется, превращаясь в оксид-гидроксид железа (III), проще говоря, в ржавчину:
Ржавчина – очень рыхлое вещество, поэтому влага и кислород легко проникают сквозь неё и продолжают уничтожать железо. Чтобы предотвратить коррозию, применяют различные покрытия. Обычно используют цинк – металл более активный, чем железо. Другой тип защитных покрытий – полимеры. Чаще всего это лаки и краски, основой которых служат масла и синтетические смолы. При их высыхании образуются очень плотная плёнка, препятствующая проникновению влаги к поверхности металла. Для борьбы с коррозией применяют и ингибиторы – вещества, которые подавляют окисление железа.
Физические свойства

Железо – серебристо-серый металл, обладает большой ковкостью, пластичностью и сильными магнитными свойствами. Температура плавления 1539 о С.
Нахождение в природе
Железо является вторым по распространенности металлом в природе (после алюминия). В свободном состоянии железо встречается только в метеоритах. Наиболее важные природные соединения:
Fe2O3 – красный железняк
FeS2 – железный колчедан (пирит)

Химические свойства
Валентные электроны у атома железа находятся на последнем электронном слое (4s 2 ) и предпоследнем (3d 6 ). В химических реакциях железо может отдавать эти электроны и проявлять степени окисления +2, +3 и иногда +6.
В реакциях железо является восстановителем. Однако при обычной температуре оно не взаимодействует даже с самыми активными окислителями (галогенами, кислородом, серой), но при нагревании становится активным и реагирует с ними:
При очень высокой температуре железо реагирует с углеродом, кремнием и фосфором:
Железо находится в середине электрохимического ряда напряжений металлов, поэтому является металлом средней активности. Восстановительная способность у железа меньше, чем у щелочных, щелочноземельных металлов и у алюминия. Только при высокой температуре раскаленное железо реагирует с водой:
Железо реагирует с разбавленными серной и соляной кислотами, вытесняя из них водород:
При обычной температуре железо не взаимодействует с концентрированной серной кислотой, так как пассивируется ею. При нагревании концентрированная H2SO4 окисляет железо до сульфата железа (III):
Разбавленная азотная кислота окисляет железо до нитрата железа (III):
Концентрированная азотная кислота пассивирует железо.
Из растворов солей железо вытесняет металлы, которые расположены правее его в электрохимическом ряду напряжений:
Соединения железа (II)

Оксид железа (II) FeO – черное кристаллическое вещество, нерастворимое в воде. Оксид железа (II) получают восстановлением оксида железа (II, III) оксидом углерода (II):
Оксид железа (II) – основный оксид, легко реагирует с кислотами, при этом образуются соли железа (II):
Гидроксид железа (II) Fe(OH)2 – порошок белого цвета, не растворяется в воде. Получают его из солей железа (II) при взаимодействии их со щелочами:
Гидроксид железа (II) Fe(OH)2 проявляет свойства основания, легко реагирует с кислотами:
При нагревании Fe(OH)2 разлагается:
Соединения со степенью окисления железа +2 проявляют восстановительные свойства, так как Fe 2+ легко окисляется до Fe 3+ :
Так, свежеполученный зеленоватый осадок Fe(OH)2 на воздухе очень быстро изменяет окраску – буреет. Изменение окраски объясняется окислением Fe(OH)2 в Fe(OH)3 кислородом воздуха:
Восстановительные свойства проявляют и соли двухвалентного железа, особенно при действии окислителей в кислой среде. Например, сульфат железа (II) восстанавливает перманганат калия в сернокислотной среде до сульфата марганца (II):
Качественная реакция на катион железа (II)
Реактивом для обнаружения катиона железа Fe 2+ является гексацианоферрат (III) калия (красная кровяная соль) K3[Fe(CN)6]:
При взаимодействии ионов [Fe(CN)6] 3- с катионами железа Fe 2+ образуется темно-синий осадок – турнбулева синь:
Соединения железа (III)
Оксид железа (III) Fe2O3 – порошок бурого цвета, не растворяется в воде. Оксид железа (III) получают:
а) разложением гидроксида железа (III):
б) окислением пирита (FeS2):
Оксид железа (III) проявляет амфотерные свойства:
а) взаимодействует с кислотами:
б) взаимодействует с твердыми щелочами NaOH и KOH, с карбонатами натрия и калия при высокой температуре:

Гидроксид железа (III) получают из солей железа (III) при взаимодействии со щелочами:
Гидроксид железа (III) является более слабым основанием, чем Fe(OH)2, и проявляет амфотерные свойства (с преобладанием основных). При взаимодействии с разбавленными кислотами Fe(OH)3 легко образует соответствующие соли:
Реакции с концентрированными растворами щелочей протекают лишь при длительном нагревании. При этом получаются устойчивые гидроксокомплексы:
Соединения со степенью окисления железа +3 проявляют окислительные свойства, так как под действием восстановителей Fe +3 превращаются в Fe +2 :
Так, например, хлорид железа (III) окисляет йодид калия до свободного йода:
Качественные реакции на катион железа (III)

а) Реактивом для обнаружения катиона Fe 3+ гексацианоферрат (II) калия (желтая кровяная соль) K4[Fe(CN)6].
При взаимодействии ионов [Fe(CN)6] 4- с ионами Fe 3+ образуется темно-синий осадок – берлинская лазурь:
Применение и биологическая роль железа и его соединений
Важнейшие сплавы железа – чугуны и стали – являются основными конструкционными материалами практически во всех отраслях современного производства.
Хлорид железа (III) применяется для очистки воды. В органическом синтезе FeCl3 применяется как катализатор. Нитрат железа Fe(NO3)3∙9H2O используют при окраске тканей.
Железо является одним из важнейших микроэлементов в организме человека и животных (в организме взрослого человека содержится в виде соединений около 4 г железа). Оно входит в состав гемоглобина, миоглобина, различных ферментов и других сложных железо-белковых комплексов, которые находятся в печени и селезенке. Железо стимулирует функцию кроветворных органов.
Кобальт (Cobaltum) и никель (Niccolum)
По сравнению с известным человеку испокон веков железом, его соседи по периодической системе, кобальт и никель, были открыты, можно сказать, совсем недавно.
История кобальта как химического элемента началась в Саксонии, на серебряных рудниках. Иногда из руды, очень похожей на серебряную, не удавалось получить желанный металл, а при ее обжиге выделялся ядовитый газ. В таком случае говорили, что рудокопы потревожили злого духа Коболда. В 1735 г. шведский химик Георг Брандт установил, что в «злом» минерале содержатся мышьяк (поэтому при обжиге выделялись ядовитые пары) и неизвестный металл. Брандт выделил его и сохранил за ним название «кобальт».
Никель был обнаружен в красноватого цвета руде, содержащей, как потом выяснилось, арсенид никеля. По цвету руды заключили, что в ней должна быть медь, однако попытки ее выплавить оканчивались неудачей. Горняки считали, что это проделки насмешника Ника (Николаса) – хозяина подземных богатств. Когда люди научились отличать «чужую» руду от настоящей медной, они дали ей название «купферникель», т.е. «медь Ника». В 1751 г. именно из этой руды шведский учёный Аксель Фредрик Кронстедт выделил неизвестный ранее оксид зеленого цвета. Восстановив оксид, Кронстедт получил металл, названный им никелем.

Долгое время кобальт не находил применения из-за хрупкости, а никель ограниченно использовался только в ювелирном деле. Лишь в 70-х гг. XIX в. окончательно установили, что хрупкость никеля обусловлена примесями мышьяка и серы. Для получения ковких металлов к плаву добавляют магний, который связывает эти примеси. Чистые кобальт и никель представляют собой твёрдые серебристо-белые металлы, прочные и пластичные. Подобно железу, они легко намагничиваются. Однако спутать с железом их невозможно – оба металла настолько устойчивы к коррозии, что не тускнеют на воздухе и лишь очень медленно растворяются в кислотах. Многие их сплавы обладают уникальными свойствами. Наиболее известны хромо-кобальтовые сплавы – лёгкие и прочные, применяемые для изготовления авиатурбин. Сплав никеля с железом незаменим в микроэлектронике, а медно-никелевый сплав монель – широко используемый конструкционный материал.
Но чаще мы сталкиваемся с другим медно-никелевым сплавом, тем, из которого изготовляют монеты. В США с 1866 г. из него чеканят пятицентовые монеты. С тех пор американцы их так и называют – nickels.

Удивительно, но никель (обычно в виде сплавов с медью) содержался в монетах и металлической посуде, изготовленных в разных частях света еще до новой эры. Некоторые соединения кобальта были известны древним египтянам. Сплавляя обожженные кобальтовые руды с песком и поташом (карбонатом калия) и затем измельчая сплав, получали порошок синего цвета. Его использовали для изготовления цветного непрозрачного стекла.
По химическим свойствам кобальт и никель похожи на железо, но в ряду Fe – Co – Ni устойчивость степени окисления +3 падает. Гидроксиды кобальта(II) и никеля(II) нерастворимы в воде и обладают только основными свойствами.
Скачать:
Скачать бесплатно реферат на тему: «Железо» ЖЕЛЕЗО.docx (228 Загрузок)
Скачать бесплатно реферат на тему: «Железо и его роль» Железо-и-его-роль.docx (222 Загрузки)
Скачать бесплатно реферат на тему: «Кобальт» Кобальт.docx (242 Загрузки)
Скачать бесплатно реферат на тему: «Сталь и чугун» Сталь-и-чугун2.doc (220 Загрузок)
Скачать рефераты по другим темам можно здесь
*на изображении записи фотография минерала «бурый железняк»
Вариант 2
Вопросы:
1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
2. Какие свойства — окислительные или восстановительные — проявляют соединения железа со степенью окисления +2? Почему?
3. Как, исходя из металлического железа, можно получить гидроксид железа(II) и гидроксид железа(III)? Приведите уравнения реакций.
4. Смесь железа и железной окалины Fe3O4 массой 32 г обработали избытком соляной кислоты. При этом выделилось
5,6 л водорода (н. у.). Рассчитайте массовую долю железа и железной окалины в смеси. (Ответ: 43,75% Fe и 56,25% Fe3O4.)
Ответы и решения:
2. Соединения железа со степенью окисления +2 проявляют восстановительные свойства, при этом окисляясь до степени окисления +3, т.к. их атом при этом переходит в более устойчивую форму. В некоторых случаях эти соединения могут проявлять окислительные свойства, когда из них вытесняется металлическое железо.
Урок 11. Железо
Свойства железа и его соединений
Железо — химический элемент восьмой группы, четвёртого периода, следовательно, строение его атома можно изобразить схемой:
Железо — очень распространённый элемент периодической системы. Среди химических элементов, которые входят в состав Земной коры, оно занимает четвёртое место. В центре Земли имеется массивное железно-никелевое ядро, которое обеспечивает естественный магнетизм Земли.
Хотя атом железа в соединениях может проявлять степени окисления +2, +3, +6, в природе встречаются соединения преимущественно трёхвалентного железа:
Все эти руды имеют буро-красную окраску. Интересно, что от этой окраски произошло слово руда: «рудый» означает «рыжий». Дело в том, что железные руды встретились человеку давным-давно, и с освоения этих руд началась наша цивилизация, поскольку для разработки технологии выплавки железа из руды потребовались значительные интеллектуальные усилия, все знания, которых накопил человек.
Атомы железа (II) входят в состав гемоглобина крови. Именно эти атомы связывают кислород и транспортируют его по всем клеткам нашего организма. При этом атом железа становится трёхвалентным, с характерной для этого состояния «кровавой» окраской. Кстати, название руды «гематит» и означает «кровавый».
Железо — серебристо-белый пластичный металл. Это металл средней активности, тем не менее оно может реагировать с активными неметаллами (галогены, кислород, сера, углерод), кислотами, а при особых условиях — с водой. При этом если реакция происходит с сильным окислителем, то образуется соединение трёхвалентного железа. Впрочем, если в результате реакции образуется соединение двухвалентного железа, то на воздухе это соединение быстро окисляется до трёхвалентного состояния. Например, с сильным окислителем хлором образуется хлорид Fe (III):
А при взаимодействии с соляной кислотой, атом хлора которой может проявлять только восстановительные свойства, образуется хлорид железа (II).
Задание 11.1. Составить уравнение реакции взаимодействия железа с серой, водой, соляной кислотой, разбавленной азотной кислотой.
Соли железа (II) и (III) имеют разную окраску: растворы соединений железа (II) бесцветные, а растворы железа (III) — окрашены в жёлтый цвет.
При взаимодействии с щелочами из растворов солей железа можно получить его гидроксиды. Они так сильно отличаются друг от друга по цвету, что эту реакцию можно считать качественной на соединения железа с разной степенью окисления. Так, из солей Fe (II) выделяется белый (в инертной атмосфере) осадок, который на воздухе мгновенно зеленеет:
На воздухе этот осадок «ржавеет», становится буро-оранжевым. Состав полученного осадка очень близок к составу ржавчины:
Наиболее чувствительной качественной реакцией на Fe 3+ является реакция с роданидом калия:
Оксид и гидроксид железа (II) проявляют основные свойства, т. е. реагируют с кислотами, но не реагируют со щелочами. В отличие от них, оксид и гидроксид железа (III) проявляют слабые амфотерные свойства. Это означает, что при обычных условиях эти вещества реагируют с кислотами и не реагируют со щелочами, но при сплавлении они со щелочами реагируют:
Кроме того, они растворяются в горячих, концентрированных растворах щелочей.
Таким образом, на примере свойств соединений железа ещё раз убеждаемся в справедливости закономерности: при возрастании степени окисления атома металла усиливаются и кислотные, и окислительные свойства соединений.
Действительно, для соединений двухвалентного железа характерны восстановительные свойства: они окисляются просто на воздухе. Для соединений трёхвалентного железа характерны окислительные свойства, они могут находиться в растворе длительное время. Единственное, что «угрожает» солям трёхвалентного железа, — гидролиз, поскольку эти соли соответствуют более слабому основанию.
Задание 11.2. Составьте уравнение реакции гидролиза хлорида железа (III).
Получение железа (чугуна и стали)
Производство чугуна основано на восстановительных свойствах углерода. Чугун образуется в домнах, куда загружают смесь кокса и железной руды. В результате горения кокса образуется необходимое для реакции тепло и сильный восстановитель — угарный газ:
Впрочем, и кокс является прекрасным восстановителем:
Угарный газ является основным восстановителем доменного процесса, поскольку ввиду газообразного состояния имеет высокую реакционную способность, способен проникать в любую точку домны. Кроме того, он не образует цементита. Эти реакции восстановления происходят при температуре 450…700 °C:
Полученный углекислый газ, реагируя с избытком кокса, вновь превращается в угарный газ:
и процесс продолжается. Он происходит в верхней части домны. Выделяющееся в твёрдом виде железо опускается в нижнюю часть домны, контактирует с коксом, начинает плавиться, так как температура в этой части печи превышает 1300 °C. Кокс, образуя сплав с железом (чугун), понижает температуру плавления железа на 400°; одновременно с этим часть железа образует цементит:
Для предохранения расплавленного железа от окисления в исходную смесь добавляют флюсы. Это известняк, который является поставщиком углекислого газа и, всплывая на поверхность, образует защитную плёнку.
Полученный чугун содержит до 4,5 % углерода, он используется для получения стали. Цель переработки — удаление примесей углерода, фосфора, серы. Готовая сталь должна содержать 0,3…2 % углерода. Кроме того, в сталь вводят различные добавки, которые изменяют её свойства. Так, нержавеющая сталь содержит около 12 % хрома.
Сталь является основным сплавом машиностроения, но легко ржавеет, так как подвергается коррозии (см. урок 8.4).
Выводы
Железо — главный металл нашей цивилизации. Станки, различные машины и механизмы, строительные конструкции, мосты, трубы — всё состоит из железа, точнее, стали или чугуна. Это достаточно активный металл, поэтому легко образует различные соединения, в которых чаще всего проявляет валентность III. Такие соединения имеют обычно красно-коричневую окраску (ржавчина).