Существуют связи нескольких типов такие как
Типы связей информационных объектов
Одно – однозначные связи
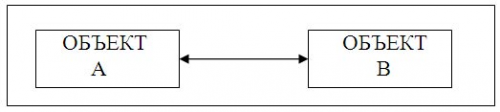
Одно – однозначные связи имеют место, когда каждому экземпляру первого объекта (А) соответствует только один экземпляр второго объекта (В)и наоборот, каждому экземпляру второго объекта (В) соответствует только один экземпляр первого объекта (А). Следует заметить, что такие объекты легко могут быть объединены в один, структура которого образуется объединением реквизитов обоих исходных объектов, а ключевым реквизитом может быть выбран любой из альтернативных ключей, т.е. ключей исходных объектов. Графическое изображение одно – однозначных связей являются группа – староста, фирма – расчетный счет в баке и т.п.
Рис.1 Графическое изображение одно – однозначных отношений объектов
Одно – многозначные связи (1:М)
Одно – многозначные связи (1:М) – это такие связи, когда экземпляру одного объекта (А) может соответствовать несколько экземпляров другого объекта (В), а каждому экземпляра второго объекта (В) может соответствовать только один экземпляр первого объекта (А).
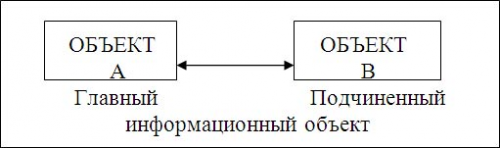
Рис.2 Графическое изображение одно – многозначный связи отношений объектов.
В такой связи объект А является главным объектом, а объект В – подчиненным, т.е. имеет место иерархическая подчиненность объекта В объекту А. Примером одно – многозначных связей являются подразделения – сотрудники, кафедра – преподаватель, группа студент и т.п.
Много – многозначные связи (M:N)
Много – многозначные связи (M:N) – это когда, каждому экземпляру одного объекта (А) могут соответствовать несколько экземпляров второго объекта (В) и наоборот, каждому экземпляру второго объекта (В) может соответствовать тоже несколько экземпляров первого объекта (А).
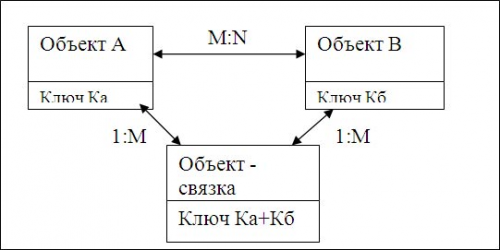
Рис.3 Преобразование связи типа M:N через объект – связку
Объект – связка должен иметь идентификатор, образованный из идентификаторов исходных объектов Ка и Кб.
Примером много – многозначных связей является связь поставщики – товары, если один поставщик поставляет разные наименования товаров, а товар одного наименования поставляется несколькими поставщиками.
Определение связей между информационными объектами
Таблица 1. Объекты справочной информации о студентах, группах и предметах
| Информационный объект | Название реквизитов | Обозначение реквизита | Признак ключа |
| ГРУППА | Номер группы Количество студентов Средний балл в группе | НГ КОЛ ПБАЛ | Уникальный простой |
| СТУДЕНТ | Номер группы Номер студентов Фамилия И.О. Год рождения Адрес Балл при поступлении | НГ НС ФИО ГОДР АДРЕС ПБАЛЛ | Уникальный составной |
| ПРЕДМЕТ | Код предмета Название предмета Всего часов Часов лекций Часов практики Число семестров Программа курса (большой текст) | КП НП ЧАСЫ | Уникальный простой |
Таблица 2. Группировка реквизитов по информационным объектам документа Список преподавателей кафедры
| Реквизиты объекта | Признак ключа | Имя информационного объекта | Семантика объекта |
| ТАБН ККАФ ФИО СТ ЗВ | П,У | ПРЕПОДАВАТЕЛЬ | Сведения о преподавателях кафедр |
| ККАФ НКАФ ТЕЛ ЗАВ | П,У | КАФЕДРА | Сведения о кафедрах |
В таблице приняты обозначения для ключа: П – простой, У – уникальный.
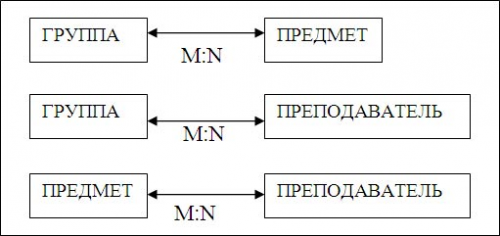
Рис.4 Много – многозначные связи информационных объектов
Рис.5 Информационно – логическая модель предметной области Учебный процесс
В табл.3 перечислены все одно – многозначные связи между объектами, указаны ключи, по которым должны устанавливаться связи, и определены главные и подчиненные информационные объекты в этих связях.
Таблица 3 Связи информационных объектов
| Главный объект | Подчиненный объект | Тип связи | Ключ связи |
| ГРУППА КАФЕДРА ГРУППА ПРЕДМЕТ ПРЕПОДАВАТЕЛЬ СТУДЕНТ ИЗУЧЕНИЕ | СТУДЕНТ ПРЕПОДАВАТЕЛЬ ИЗУЧЕНИЕ ИЗУЧЕНИЕ ИЗУЧЕНИЕ УСПЕВАЕМОСТЬ УСПЕВАЕМОСТЬ | 1:М 1:М 1:М 1:М 1:М 1:М 1:М | НГ К КАФ НГ КП ТАБН НГ+НС НГ+КП+ТАБН+ВИДЗ |
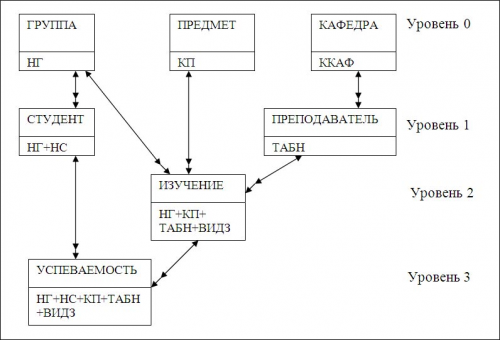
Информационно – логическая модель предметной области Учебный процесс
Информационно – логическая модель приведена в каноническом виде и объекты в ней размещены по уровням. Уровень остальных объектов определяется наиболее длинным путем к объекту от нулевого уровня. Такое размещение объектов дает представление об их иерархической подчиненности, делает модель более наглядной и облегчает понимание одно – многозначных отношений между объектами.
Логическая структура реляционной базы данных
Логическая структура реляционной базы данных Access является адекватным отображением полученной информационно – логической модели, не требующим дополнительных преобразований. Каждый информационный объект модели данных отображается соответствующей реляционной таблицей. Структура реляционной таблицы определяется реквизитным составом соответствующего информационного объекта, где каждый столбец (поле) соответствует одному из реквизитов объекта. Ключевые реквизиты объекта образуют уникальный ключ реляционной таблицы. Для каждого столбца задается тип, размер данных и другие свойства. Строки (записи) таблицы соответствуют экземплярам объекта и формируются при загрузке таблиц.
Связи между объектами модели данных реализуются одинаковыми реквизитами – ключами связи в соответствующих таблицах. При этом ключом связи всегда является уникальный ключ главной таблицы. Ключом связи в подчиненной таблице является либо некоторая часть уникального ключа в ней, либо поле, не входящее в состав первичного ключа (например, код кафедры в таблице ПРЕПОДАВАТЕЛЬ ). Ключ связи в подчиненной таблице называется внешним ключом. В Access может быть создана схема данных, наглядно отображающая логическую структуру базы данных. Определение одно – многозначных связей в этой схеме должно осуществляться в соответствии с построенной моделью данных. Внешний вид схемы данных практически совпадает с графическим представлением информационно – логической модели. Для модели данных, построенной в рассмотренном примере, логическая структура базы данных в виде схемы данных Access приведена на рис.2.7.
На этой схеме прямоугольники отображают таблицы базы данных с полным списком их полей, а связи показывают, по каким полям осуществляется взаимосвязь таблиц. Имена ключевых полей находятся в левой части полного списка полей каждой таблицы.
Система управления базами данных SQLite. Изучаем язык запросов SQL и реляционные базы данных на примере библиотекой SQLite3. Курс для начинающих.
Часть 3.2: Виды связей между таблицами в базе данных. Связи в реляционных базах данных. Отношения, кортежи, атрибуты
Здравствуйте, уважаемые посетители сайта ZametkiNaPolyah.ru. Продолжаем изучать базы данных и наше знакомство с библиотекой SQLite3. Продолжаем изучать теорию реляционных баз данных и в этой части мы познакомимся с видами и типами связей между таблицами в реляционных базах данных. Так же мы познакомимся с такими термина, как: кортеж, атрибут и отношения. Данная тема является базовой и ее понимание необходимо для работы с базами данных и для их проектирования.
Виды связей между таблицами в базе данных. Связи в реляционных базах данных. Отношения, кортежи, атрибуты.
Сразу скажу, что связей между таблицами в реляционной базе данных всего три. Поэтому их изучение, понимание и восприятие пройдет быстро, легко и безболезненно. Приступим к изучению.
Термины кортеж, атрибут и отношение в реляционных базах данных
В своей публикации я буду стараться объяснять теорию баз данных не с математической точки зрения, а на примерах. Грубо говоря, на пальцах. Во-первых, практические примеры позволяют легче усваивать материал. Во-вторых, с математической теорией проще разобраться, когда понимаешь суть происходящего.
Давайте разбираться с тем, что такое: отношение, кортеж, атрибут в реляционной базе данных.
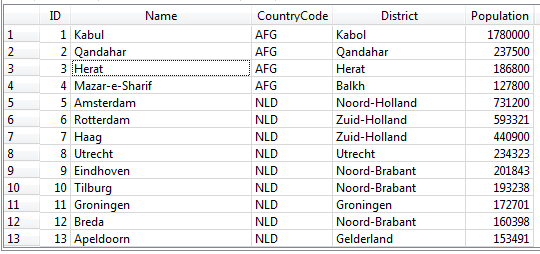
Таблица с данными из базы данных World
У нас есть простая таблица City из базы данных World, в которой есть строки и столбцы. Но термины: таблица, строка, столбец – это термины стандарта SQL.
Кстати: ни одна из существующих в мире СУБД не имеет полной поддержки того или иного стандарта SQL, но и ни один стандарт SQL полностью не реализует математику реляционных баз данных.
В терминологии реляционных баз данных: таблица – это отношение (принимается такое допущение), строка – это кортеж, а столбец – атрибут. Иногда вы можете услышать, как некоторые разработчики называют строки записями. Чтобы не было путаницы в дальнейшем предлагаю использовать термины SQL.
Если рассматривать таблицу, как объект (например книга), то столбец – это характеристики объекта, а строки содержат информацию об объекте.
Виды и типы связей между таблицами в реляционных базах данных
Давайте теперь рассмотрим то, как могут быть связаны таблицы в реляционных базах данных. Сразу скажу, что всего существует три вида связей между таблицами баз данных:
• связь один к одному;
• связь один ко многим;
• связь многие ко многим.
Рассмотрим, как такие связи между таблицами могут быть реализованы в реляционных базах данных.
Реализация связи один ко многим в теории баз данных
Связь один ко многим в реляционных базах данных реализуется тогда, когда объекту А может принадлежать или же соответствовать несколько объектов Б, но объекту Б может соответствовать только один объект А. Не совсем понятно, поэтому смотрим пример ниже.
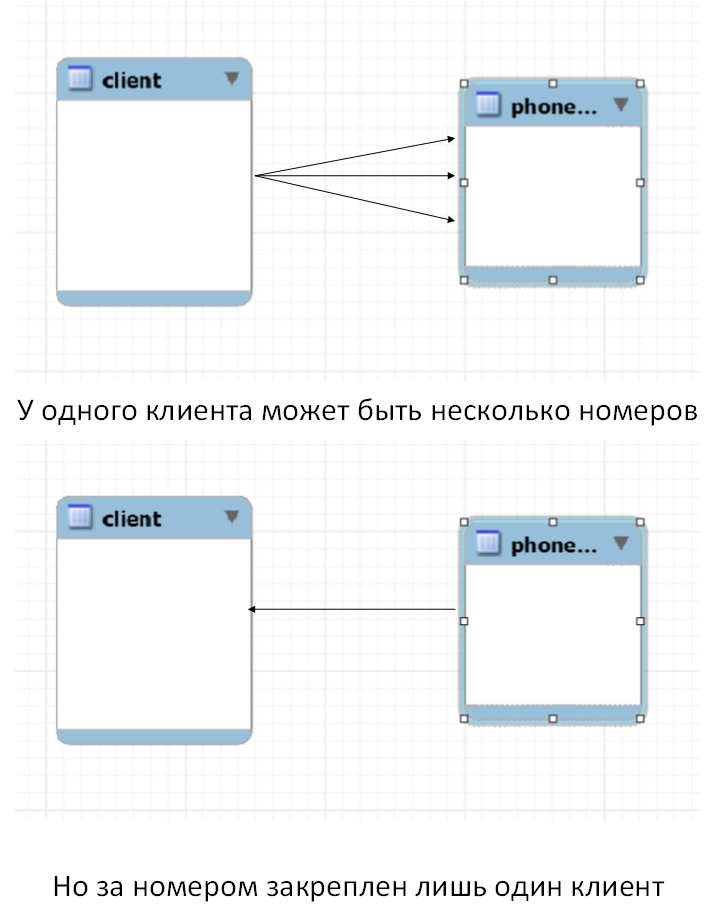
Реализация связи один ко многим в реляционных базах данных
У нас есть таблица, в которой содержатся данные о клиентах и у нас есть таблица, в которой хранятся их телефоны. Мы можем смело утверждать, что у одного клиента может быть несколько телефонов, но в тоже время мы можем быть уверены в том, что один конкретный номер может быть только у одного клиента. Это типичный пример связи один ко многим.
Связь многие ко многим
Связь многие ко многим реализуется в том случае, когда нескольким объектам из таблицы А может соответствовать несколько объектов из таблицы Б, и в тоже время нескольким объектам из таблицы Б соответствует несколько объектов из таблицы А. Рассмотрим простой пример.
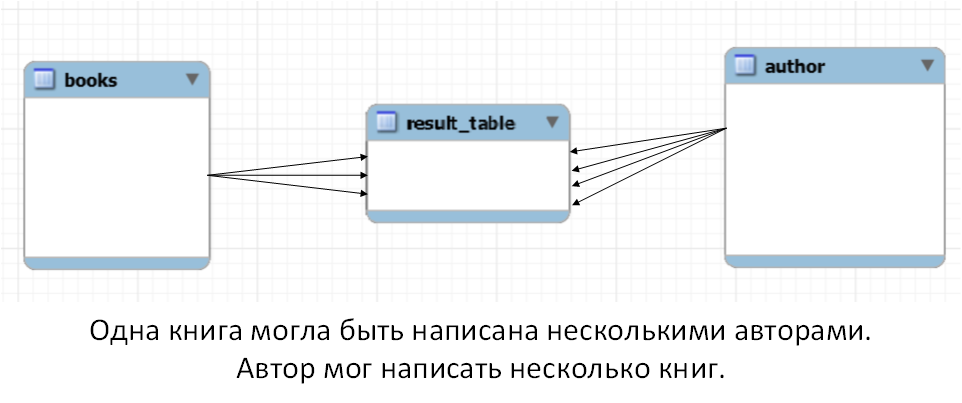
Пример связи многие ко многим
У нас есть таблица с книгами и есть таблица с авторами. Приведу два верных утверждения. Первое: одну книгу может написать несколько авторов. Второе: автор может написать несколько книг. Здесь мы наблюдаем типичную ситуацию, когда связь между таблицами многие ко многим. Такая связь (связь многие ко многим) реализуется путем добавления третьей таблицы.
Связь один к одному
Связь один к одному – самая редко встречаемая связь между таблицами. В 97 случаях из 100, если вы видите такую связь, вам необходимо объединить две таблицы в одну.
Пример связи один к одному
Таблицы будут связаны один к одному тогда, когда одному объекту таблицы А соответствует один объект таблицы Б, и одному объекту таблицы Б соответствует один объект таблицы А. Как я уже говорил: если вы видите, что связь один к одному – смело объединяйте таблицы в одну, за исключением тех случаев, когда происходит модернизация базы данных.
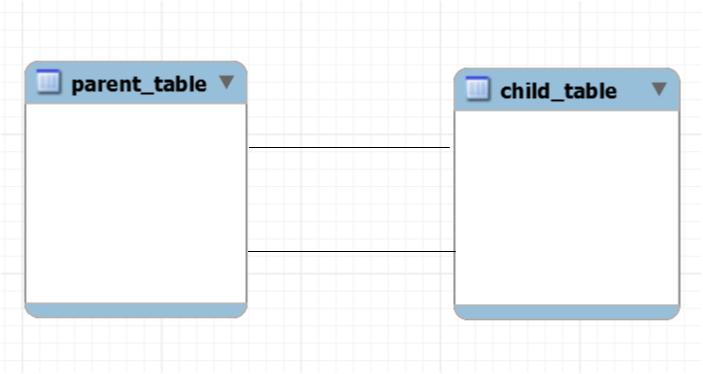
Например, у нас была таблица, в которой хранились данные о сотрудниках компании. Но произошли какие-то изменения в бизнес-процессе и появилась необходимость создать таблицы с теми же самыми сотрудниками, но не для всей компании, а разбив их по отделам. Таблицы отделов будут дочерними по отношению к таблице, в которой хранятся данные обо всех сотрудниках компании, и связаны такие таблицы будут связью один к одному.
Мы рассмотрели все виды связей между таблицами и то, как они реализуются в базах данных. В дальнейшем, когда мы начнем создавать свои базы данных, информация о видах связи между таблицами нам очень поможет.
Химическая связь. Типы химической связи
Диссоциация хлорида натрия в воде
Темы кодификатора ЕГЭ: Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь
Сначала рассмотрим связи, которые возникают между частицами внутри молекул. Такие связи называют внутримолекулярными.
Химическая связь между атомами химических элементов имеет электростатическую природу и образуется за счет взаимодействия внешних (валентных) электронов, в большей или меньшей степени удерживаемых положительно заряженными ядрами связываемых атомов.
Электроотрицательность χ – это способность атома притягивать (удерживать) внешние (валентные) электроны. Электроотрицательность определяется степенью притяжения внешних электронов к ядру и зависит, преимущественно, от радиуса атома и заряда ядра.
Важно отметить, что в различных источниках можно встретить разные шкалы и таблицы значений электроотрицательности. Этого не стоит пугаться, поскольку при образовании химической связи играет роль разность электроотрицательностей атомов, а она примерно одинакова в любой системе.
Если один из атомов в химической связи А:В сильнее притягивает электроны, то электронная пара смещается к нему. Чем больше разность электроотрицательностей атомов, тем сильнее смещается электронная пара.
Основные типы химических связей — ковалентная, ионная и металлическая связи. Рассмотрим их подробнее.
Ковалентная химическая связь
Основные свойства ковалентных связей
Эти свойства связи влияют на химические и физические свойства веществ.
Насыщаемость — это способность атомов образовывать ограниченное число ковалентных химических связей. Количество связей, которые способен образовывать атом, называется валентностью.
Полярность связи возникает из-за неравномерного распределения электронной плотности между двумя атомами с различной электроотрицательностью. Ковалентные связи делят на полярные и неполярные.
Поляризуемость связи — это способность электронов связи смещаться под действием внешнего электрического поля (в частности, электрического поля другой частицы). Поляризуемость зависит от подвижности электронов. Чем дальше электрон находится от ядра, тем он более подвижен, соответственно и молекула более поляризуема.
Ковалентная неполярная химическая связь
Ковалентная неполярная (симметричная) связь – это ковалентная связь, образованная атомами с равной элетроотрицательностью (как правило, одинаковыми неметаллами) и, следовательно, с равномерным распределением электронной плотности между ядрами атомов.
Дипольный момент неполярных связей равен 0.
Ковалентная полярная химическая связь
Ковалентная полярная связь – это ковалентная связь, которая возникает между атомами с разной электроотрицательностью (как правило, разными неметаллами) и характеризуется смещением общей электронной пары к более электроотрицательному атому (поляризацией).
Электронная плотность смещена к более электроотрицательному атому – следовательно, на нем возникает частичный отрицательный заряд (δ-), а на менее электроотрицательном атоме возникает частичный положительный заряд (δ+, дельта +).
Полярность связи влияет на физические и химические свойства соединений. От полярности связи зависят механизмы реакций и даже реакционная способность соседних связей. Полярность связи зачастую определяет полярность молекулы и, таким образом, непосредственно влияет на такие физические свойства как температуре кипения и температура плавления, растворимость в полярных растворителях.
Механизмы образования ковалентной связи
Ковалентная химическая связь может возникать по 2 механизмам:
1. Обменный механизм образования ковалентной химической связи – это когда каждая частица предоставляет для образования общей электронной пары один неспаренный электрон:
2. Донорно-акцепторный механизм образования ковалентной связи – это такой механизм, при котором одна из частиц предоставляет неподеленную электронную пару, а другая частица предоставляет вакантную орбиталь для этой электронной пары:
А: + B= А:В
При этом один из атомов предоставляет неподеленную электронную пару ( донор ), а другой атом предоставляет вакантную орбиталь для этой пары ( акцептор ). В результате образования связи оба энергия электронов уменьшается, т.е. это выгодно для атомов.
Ковалентная связь, образованная по донорно-акцепторному механизму, не отличается по свойствам от других ковалентных связей, образованных по обменному механизму. Образование ковалентной связи по донорно-акцепторному механизму характерно для атомов либо с большим числом электронов на внешнем энергетическом уровне (доноры электронов), либо наоборот, с очень малым числом электронов (акцепторы электронов). Более подробно валентные возможности атомов рассмотрены в соответствующей статье.
Ковалентная связь по донорно-акцепторному механизму образуется:
– в молекуле угарного газа CO (связь в молекуле – тройная, 2 связи образованы по обменному механизму, одна – по донорно-акцепторному): C≡O;
– в комплексных соединениях, химическая связь между центральным атомом и группами лигандов, например, в тетрагидроксоалюминате натрия Na[Al(OH)4] связь между алюминием и гидроксид-ионами;
– в азотной кислоте и ее солях — нитратах: HNO3, NaNO3, в некоторых других соединениях азота;
– в молекуле озона O3.
Основные характеристики ковалентной связи
Ковалентная связь, как правило, образуется между атомами неметаллов. Основными характеристиками ковалентной связи являются длина, энергия, кратность и направленность.
Кратность химической связи
Кратность химической связи — это число общих электронных пар между двумя атомами в соединении. Кратность связи достаточно легко можно определить из значения валентности атомов, образующих молекулу.
Например , в молекуле водорода H2 кратность связи равна 1, т.к. у каждого водорода только 1 неспаренный электрон на внешнем энергетическом уровне, следовательно, образуется одна общая электронная пара.
В молекуле кислорода O2 кратность связи равна 2, т.к. у каждого атома на внешнем энергетическом уровне есть по 2 неспаренных электрона: O=O.
В молекуле азота N2 кратность связи равна 3, т.к. между у каждого атома по 3 неспаренных электрона на внешнем энергетическом уровне, и атомы образуют 3 общие электронные пары N≡N.
Длина ковалентной связи
Длина химической связи – это расстояние между центрами ядер атомов, образующих связь. Ее определяют экспериментальными физическими методами. Оценить величину длины связи можно примерно, по правилу аддитивности, согласно которому длина связи в молекуле АВ приблизительно равна полусумме длин связей в молекулах А2 и В2:
Длину химической связи можно примерно оценить по радиусам атомов, образующих связь, или по кратности связи, если радиусы атомов не сильно отличаются.
При увеличении радиусов атомов, образующих связь, длина связи увеличится.
При увеличении кратности связи между атомами (атомные радиусы которых не отличаются, либо отличаются незначительно) длина связи уменьшится.
Энергия связи
Мерой прочности химической связи является энергия связи. Энергия связи определяется энергией, необходимой для разрыва связи и удаления атомов, образующих эту связь, на бесконечно большое расстояние друг от друга.
Ковалентная связь является очень прочной. Ее энергия составляет от нескольких десятков до нескольких сотен кДж/моль. Чем больше энергия связи, тем больше прочность связи, и наоборот.
Прочность химической связи зависит от длины связи, полярности связи и кратности связи. Чем длиннее химическая связь, тем легче ее разорвать, и тем меньше энергия связи, тем ниже ее прочность. Чем короче химическая связь, тем она прочнее, и тем больше энергия связи.
Ионная химическая связь
Ионная связь — это химическая связь, основанная на электростатическом притяжении ионов.
Ионы образуются в процессе принятия или отдачи электронов атомами. Например, атомы всех металлов слабо удерживают электроны внешнего энергетического уровня. Поэтому для атомов металлов характерны восстановительные свойства — способность отдавать электроны.
+11 Na ) 2 ) 8 ) 1 — 1e = +11 Na + ) 2 ) 8
+17 Cl ) 2 ) 8 ) 7 + 1e = +17 Cl — ) 2 ) 8 ) 8
Обратите внимание:
Наглядно обобщим различие между ковалентными и ионным типами связи:
Металлическая химическая связь
Металлическая связь — это связь, которую образуют относительно свободные электроны между ионами металлов, образующих кристаллическую решетку.
У атомов металлов на внешнем энергетическом уровне обычно расположены от одного до трех электронов. Радиусы у атомов металлов, как правило, большие — следовательно, атомы металлов, в отличие от неметаллов, достаточно легко отдают наружные электроны, т.е. являются сильными восстановителями.
Межмолекулярные взаимодействия
Ориентационные силы притяжения возникают между полярными молекулами (диполь-диполь взаимодействие). Эти силы возникают между полярными молекулами. Индукционные взаимодействия — это взаимодействие между полярной молекулой и неполярной. Неполярная молекула поляризуется из-за действия полярной, что и порождает дополнительное электростатическое притяжение.
Водородные связи возникают между следующими веществами:
— фтороводород HF (газ, раствор фтороводорода в воде — плавиковая кислота), вода H2O (пар, лед, жидкая вода):
— раствор аммиака и органических аминов — между молекулами аммиака и воды;
— органические соединения, в которых связи O-H или N-H: спирты, карбоновые кислоты, амины, аминокислоты, фенолы, анилин и его производные, белки, растворы углеводов — моносахаридов и дисахаридов.
Водородная связь оказывает влияние на физические и химические свойства веществ. Так, дополнительное притяжение между молекулами затрудняет кипение веществ. У веществ с водородными связями наблюдается аномальное повышение температуры кипения.