висцеральный криз в онкологии что это такое
Метастатический гормоночувствительный рак молочной железы в постменопаузе: новые тенденции. Петербургский онкологический форум «Белые ночи – 2015». Сателлитный симпозиум компании «АстраЗенека»
Выбор терапии при метастатическом гормоночувствительном раке молочной железы в постменопаузе
Вопросы выбора оптимального метода терапии метастатического рака молочной железы (РМЖ) у женщин в постменопаузальном периоде подробно рассмотрел Пьер-Франко КОНТЕ (Университет г. Падуя, Италия). Он подчеркнул, что при распространенном (метастатическом) раке молочной железы гормональная терапия является предпочтительным вариантом для большинства пациенток.
Часть больных с гормонопозитивным распространенным РМЖ первоначально получают химиотерапию – до достижения наилучшего ответа. Решение о проведении химиотерапии основывается на клинических показаниях, включающих массивное поражение внутренних органов, рецидив во время или вскоре после адъювантной гормонотерапии, симптоматические метастазы. По окончании курса химиотерапии такие пациентки должны получать поддерживающую гормонотерапию.
Докладчик отметил, что при назначении лечения необходимо учитывать стадию болезни, морфологическую картину опухоли, индивидуально оценивать каждый случай прогрессирования заболевания на фоне гормональной терапии.
В настоящее время, исходя из традиционных подходов к лечению гормонопозитивного РМЖ, висцеральные метастазы не являются противопоказанием к проведению эндокринной терапии. Во второй версии международных согласительных рекомендаций Европейского общества медицинской онкологии (European Society for Medical Oncology – ESMO) по распространенному раку молочной железы ABC2 (Advanced Breast Cancer 2) висцеральный криз определяется как выраженное нарушение функции органов на основании клинических признаков или данных лабораторных анализов на фоне быстрого прогрессирования заболевания.
В клинических исследованиях новых режимов гормонотерапии во второй линии (фулвестранта в дозе 500 мг, а также гормонотерапии в комбинации с таргетными препаратами) были получены более обнадеживающие показатели клинической эффективности, беспрогрессивной и общей выживаемости.
Алгоритм лечения гормонопозитивного/HER2-негативного метастатического РМЖ в постменопаузе включает оценку:
локализации и распространенности заболевания и его симптомов; гормонального статуса;
временных интервалов без признаков заболевания и без лечения;
общего состояния больного.
При использовании у пациенток с гормонопозитивным метастатическим РМЖ гормонотерапии первой линии медиана времени без прогрессирования может достигать 12–15 месяцев, второй линии – 6–8 месяцев, третьей – 3–4 месяца. При отсутствии эффекта от гормонотерапии или угрозе жизни больной целесообразен переход к первой линии химиотерапии.
Следует отметить, что в случае ранее регистрировавшегося эффекта гормонотерапии повышается вероятность ответа на последующие линии гормонального лечения.
Тем не менее при всех гормонопозитивных опухолях рано или поздно развивается резистентность к гормональному лечению (вторичная гормональная резистентность). Резистентность к гормональной терапии может быть первичной (присутствует с самого начала) или вторичной (заболевание прогрессирует после ответа на проведенную терапию). Сегодня стратегия лечения метастатического РМЖ направлена на своевременное выявление заболевания, увеличение общей выживаемости, повышение качества жизни больных и снижение токсичности лечения с учетом первичной и приобретенной резистентности.
В настоящее время одним из наиболее распространенных исследований, используемых в диагностике большинства онкологических заболеваний, является биопсия. Биопсия метастазов при рецидиве позволяет уточнить прогноз заболевания и индивидуализировать лечение.
При гормонопозитивном/HER2-негативном распространенном РМЖ применяют такие препараты, как тамоксифен, анастрозол, летрозол, эксеместан, фулвестрант. Кроме того, в настоящее время изучается эффективность комбинаций препаратов. Новые варианты лечения включают такие комбинации, как анти-HER2-препараты + ингибиторы ароматазы при гормонопозитивной/HER2-положительной опухоли, фулвестрант 500 мг после ингибитора ароматазы, эверолимус + эксеместан после нестероидных ингибиторов ароматазы. Исследуются комбинации CDK4/6 ингибитор + ингибитор ароматазы, CDK4/6 ингибитор + фулвестрант 500 мг, ингибиторы PARP для гормонопозитивных опухолей с мутацией BRCA.
Таким образом, результаты исследований показывают, что, если опухоль не демонстрирует первичную гормонорезистентность, эффективно последовательное применение нескольких линий гормонотерапии – антиэстрогенов (тамоксифен, фулвестрант), ингибиторов ароматазы.
Новые возможности эндокринной терапии метастатического рака молочной железы
Старший научный сотрудник отдела терапевтической онкологии НИИ онкологии им. Н.Н. Петрова, доцент кафедры Северо-Западного государственного медицинского университета им. И.И. Мечникова, д.м.н. Татьяна Юрьевна СЕМИГЛАЗОВА рассказала о современных методах эндокринной терапии метастатического РМЖ. Она отметила, что сохранение качества жизни при лечении этого заболевания остается одной из важнейших целей терапии.
Современный подход к молекулярно-генетической классификации РМЖ позволяет выделить следующие биологические подтипы заболевания: люминальный А, люминальный В, HER2-позитивный (нелюминальный) и трижды негативный.
При гормонозависимых формах РМЖ (люминальный А, люминальный В) опухолевые клетки содержат рецепторы к стероидным гормонам – эстрогенам или прогестерону. При этом люминальный гормонозависимый подтип РМЖ встречается в 65–75% случаев.
С момента первого применения овариоэктомии в 1896 г. гормонотерапия РМЖ претерпела значительные изменения. В арсенале современной гормонотерапии достаточно большое количество препаратов – от классического препарата тамоксифена до ингибиторов ароматазы, агонистов рилизинг-гормонов и антипрогестинов. С 1994 г. в практику лечения РМЖ введены чистые антиэстрогены, представляющие собой соединения как стероидной, так и нестероидной природы и лишенные эстрогеновой активности.
Тамоксифен конкурентно связывает рецептор эстрогена, приводя к уменьшению транскрипции генов, регулируемых эстрогеном. Он блокирует фазу G1 клеточного цикла и замедляет пролиферацию. Больным, получающим тамоксифен, показано каждые три месяца выполнение ультразвукового исследования малого таза для определения толщины эндометрия.
Наряду с гормонотерапией тамоксифеном вторым значимым компонентом лечения больных гормонопозитивным РМЖ являются ингибиторы ароматазы третьего поколения. Как известно, эти препараты способны значительно влиять на плотность костной ткани у пациенток. Поэтому даже в отсутствие метастазов в костях пациентки, принимающие препараты ингибиторов ароматазы, должны находиться под наблюдением эндокринолога. При снижении показателей денситометрии им один раз в полгода показано введение остеомодифицирующих агентов.
Для улучшения результатов лечения эстроген-чувствительных форм РМЖ разработана новая группа препаратов – чистые антиэстрогены. Представитель этой группы фулвестрант относится к стероидным антиэстрогенам. В отличие от тамоксифена он обеспечивает более полное подавление функции рецепторов эстрогенов и не оказывает эстрогенного эффекта на матку.
Как показали результаты, фулвестрант в дозе 250 мг в месяц не уступает анастрозолу по времени до прогрессирования заболевания.
Дополнительные свидетельства зависимости эффекта фулвестранта от дозы получены в исследовании NEWEST неоадъювантной терапии у пациенток в постменопаузе с эстроген-чувствительными опухолями. Сравнивали высокие (500 мг) и низкие дозы (250 мг) фулвестранта с помощью биологических маркеров.
Результаты международного двойного слепого исследования III фазы в параллельных группах CONFIRM подтвердили предположения о повышении эффективности при увеличении дозы и послужили основанием для регистрации препарата фулвестрант в дозе 500 мг. В исследовании участвовали женщины в постменопаузе с положительным эстроген-рецепторным статусом после проведенной адъювантной гормонотерапии или гормонотерапии первой линии тамоксифеном либо ингибиторами ароматазы. Показано, что применение препарата в более высокой дозе – 500 мг в первый день, 14-й, 28-й дни и далее ежемесячно эффективнее, чем использование препарата в дозе 250 мг в месяц. Выявлено статистически значимое уменьшение риска прогрессирования заболевания на 20% на фоне применения фулвестранта (Фазлодекс®) в дозе 500 мг по сравнению с дозой 250 мг. Отмечено увеличение однолетней выживаемости без прогрессирования с 25 до 34%, а также увеличение медианы общей выживаемости на 4,1 месяца (снижение риска смерти на 19%) (рис. 3). Преимущество дозы 500 мг наблюдалось независимо от возраста больных, наличия или отсутствия висцеральных метастазов, варианта предшествующей терапии (ингибиторы ароматазы или антиэстрогены), а также ответа на нее. При этом увеличение дозы фулвестранта практически не повлияло на частоту нежелательных явлений и не привело к нарастанию риска развития ишемических сердечно-сосудистых событий.
Таким образом, в исследованиях показано преимущество повышения дозы препарата фулвестрант (Фазлодекс®) до 500 мг для лечения эстроген-рецептор-положительного метастатического РМЖ у женщин в постменопаузальном периоде. Фазлодекс® продемонстрировал эффективность в первой линии лечения и результативность, не уступающую ингибиторам ароматазы. Как во второй, так и в первой линии терапии применение фулвестранта в дозе 500 мг привело к статистически значимому увеличению медианы общей выживаемости на 4,1 и 5,7 месяца.
Т.Ю. Семиглазова рассказала о применении новых комбинаций гормональных и таргетных препаратов в терапии метастатического РМЖ и остановилась на ряде клинических исследований эффективности подобных режимов.
В заключение Т.Ю. Семиглазова подчеркнула, что применение фулвестранта в дозе 500 мг в комбинированной терапии РМЖ демонстрирует высокую эффективность. Перспективой лекарственного лечения метастатического РМЖ является активное внедрение современных методов эндокринной терапии.
На сегодняшний день основной целью лечения метастатического РМЖ являются предупреждение прогрессирования и объективный контроль над заболеванием с использованием методов гормональной терапии. Фулвестрант (Фазлодекс®, компания «АстраЗенека») – представитель нового класса стероидных антиэстрогенов, ингибирующих пролиферативные эффекты эстрогенов на чувствительные ткани. Препарат действует как высокоселективный антагонист эстрогенных рецепторов, полностью блокирует эффекты эстрогенов и не проявляет при этом эстрогеноподобной активности.
В экспериментальных исследованиях фулвестрант продемонстрировал благоприятный профиль безопасности, хорошую переносимость пациентками и отсутствие серьезных побочных реакций, в том числе при использовании в комбинации с таргетной терапией.
Применение препарата в лечении больных метастатическим РМЖ способствует повышению общей выживаемости и отдаляет сроки прогрессирования заболевания.
Прорыв в терапии HR+/HER2- метастатического рака молочной железы. Большая конференция RUSSCO «Рак молочной железы». Сателлитный симпозиум компании «Пфайзер»
Эволюция терапевтических подходов к лечению HR+/HER2- мРМЖ
Основным видом лечения больных гормоночувствительным мРМЖ признана гормонотерапия. В соответствии с международными и российскими рекомендациями, даже при висцеральных метастазах предпочтительно последовательное назначение линий гормонотерапии. Химиотерапию назначают при наличии висцерального криза, жизнеугрожающих нарушений функций внутренних органов либо резистентности к гормонотерапии.
Следует отметить, что чувствительность к лечению определяется не распространенностью процесса и локализацией метастазов, а биологическими характеристиками опухоли. На ранней стадии прогрессирования болезни ее симптомы нередко отсутствуют, что делает нецелесообразным назначение токсичных методов лечения. На этом этапе обоснованно назначение гормонотерапии, позволяющей контролировать заболевание практически без побочных явлений. При гормонозависимом раке препараты гормонотерапии достоверно эффективны как при невисцеральных, так и при висцеральных метастазах. Тем не менее многие врачи опасаются назначать гормонотерапию при наличии у больных висцеральных метастазов.
В то же время приходится констатировать, что гормонотерапия вышла на плато своих терапевтических возможностей. То есть максимальная эффективность первой линии – девять-десять, максимум 15 месяцев при использовании современных режимов, второй линии – пять-шесть месяцев.
Можно ли сегодня говорить о дальнейшем улучшении результатов лечения? Безусловно, можно. Последующее развитие методов гормонотерапии должно происходить по двум направлениям – преодоление резистентности к эндокринотерапии и повышение ее эффективности.
С начала 2000-х гг. активно проводятся клинические исследования, посвященные решению этих вопросов. Так, в 2001 г. ученые L.H. Hartwell, R.T. Hunt, P.M. Nurse получили Нобелевскую премию за открытие роли циклин-зависимых киназ (CDK) в регуляции клеточного цикла. Как известно, CDK 4-го и 6-го типа инициируют клеточную пролиферацию от фазы роста (G1) до фаз, связанных с репликацией ДНК (S). Потеря контроля над клеточным циклом характерна для злокачественных новообразований, особенно гормонозависимых. При многих их видах происходит гиперактивация CDK 4/6, что влечет за собой усиление пролиферации и бесконтрольное деление опухолевой клетки. Решением проблемы стало создание селективного ингибитора CDK 4/6 палбоциклиба. Показано, что препарат способствует восстановлению контроля над клеточным циклом и блокирует рост опухоли. В ходе клинических испытаний были подтверждены высокая эффективность и благоприятный профиль безопасности палбоциклиба. В апреле 2013 г. эксперты Управления за контролем качества продуктов и лекарственных средств США (Food and Drug Administration, FDA) назвали палбоциклиб терапией прорыва при РМЖ, а в феврале 2015 г. одобрили применение нового препарата Ибранса® (палбоциклиб) в комбинации с летрозолом в качестве первой линии системной терапии мРМЖ у женщин в постменопаузе. Осенью 2016 г. специалисты Комитета по лекарственным препаратам для человека Европейского агентства по лекарственным средствам (European Medicines Agency, EMA) рекомендовали палбоциклиб в комбинации с ингибиторами ароматазы у больных в постменопаузе, не получавших ранее системного лечения по поводу мРМЖ, а также в комбинации с фулвестрантом у пациенток после предшествующей гормонотерапии с различным менопаузальным статусом. В октябре 2016 г. палбоциклиб был одобрен Минздравом России для лечения гормонозависимого местнораспространенного или мРМЖ в комбинации с фулвестрантом после гормонотерапии.
Палбоциклиб – первый ингибитор CDK4/6 в терапии HR+/HER2- мРМЖ
Результаты клинического исследования PALOMA-2 показали, что прием препарата Ибранса® (палбоциклиб) в комбинации с летрозолом в качестве первой линии у женщин с распространенным или метастатическим эстроген-позитивным (ER+) в отсутствие гиперэкспрессии к HER2- РМЖ способствует значительному улучшению выживаемости без прогрессирования наряду с благоприятным профилем безопасности.
В исследовании участвовала 521 больная с прогрессирующим на фоне предшествующей эндокринной терапии РМЖ. Пациентки в соотношении 2:1 были рандомизированы в группу палбоциклиба и фулвестранта и группу плацебо и фулвестранта. Главным критерием эффективности служила выживаемость без прогрессирования. Вторичными критериями были общая выживаемость, частота объективных ответов, частота клинического улучшения (ответ на лечение и стабилизация болезни), безопасность.
При наличии висцеральных метастазов с относительно невысоким темпом роста у пациентки с нормальными лабораторными показателями, минимальными симптомами назначают эндокринную терапию.
Еще одним противопоказанием к назначению эндокринотерапии является рефрактерность к гормональным препаратам. Тем не менее в американских рекомендациях NCCN (National Comprehensive Cancer Network, Национальная всеобщая онкологическая сеть) подчеркивается необходимость проведения не менее трех попыток гормонотерапии пациенткам с рецептор-позитивным РМЖ с выявленной рефрактерностью. Первичная резистентность – рецидив в течение первых двух лет адъювантной терапии или прогрессирование в течение шести месяцев первой линии эндокринотерапии метастатической болезни. Вторичная (приобретенная) резистентность определяется в случае развития рецидива после двух лет адъювантной терапии или прогрессирования спустя более шести месяцев первой линии эндокринотерапии. Однако большинство современных исследований включает определенную долю больных с рефрактерностью к эндокринотерапии. В рамках субанализа эта когорта часто выигрывает от новых вариантов терапии не меньше, чем больные без рефрактерности.
Таким образом, эндокринная терапия может быть эффективна при HR+ РМЖ, в том числе у больных в пременопаузе (при условии выключения функции яичников), при низком, но определяемом уровне экспрессии рецепторов, при наличии висцеральных метастазов.
Сегодня подавляющее большинство больных получают разнообразную адъювантную эндокринотерапию, что необходимо учитывать при разработке тактики их лечения. В последние годы спектр препаратов для лечения рецептор-позитивного мРМЖ расширился. Кроме известных препаратов, таких как тамоксифен и ингибиторы ароматазы, появились еще более эффективные препараты.
По мнению зарубежных экспертов, значимым достижением в лечении люминального мРМЖ за последние два года стало появление нового класса агентов – ингибиторов CDK 4/6 (палбоциклиб) в комбинации с эндокринотерапией. Высокие дозы фулвестранта показали незначительное увеличение выживаемости без прогрессирования – всего на один месяц, но значимое увеличение общей выживаемости – на 4,1 месяца. Согласно результатам клинических исследований, комбинированная терапия фулвестрантом и палбоциклибом в первой линии увеличивает время прогрессирования роста опухоли, обеспечивает хороший ответ на прием препарата, улучшает качество жизни большинства пациенток.
По мнению большинства международных экспертов (NCCN), единственным вариантом гормонотерапии у больных с гормонозависимым мРМЖ, который удостоен первого уровня доказательности, является комбинация палбоциклиба и фулвестранта.
В заключение Н.В. Жуков подчеркнул, что базовые установки, касающиеся лечения рецептор-позитивного РМЖ, усвоены не всеми и требуют постоянного повторения. Из-за отсутствия данных об увеличении общей выживаемости основным критерием выбора остается магнитуда выигрыша в выживаемости без прогрессирования, переносимости и уровне качества жизни.
Пероральный таргетный препарат Ибранса® (компания «Пфайзер») является первым в новом классе ингибиторов CDK 4/6 для лечения мРМЖ. Палбоциклиб, входящий в состав препарата, селективно ингибирует CDK 4/6, в результате чего восстанавливается контроль над клеточным циклом и блокируется пролиферация опухолевых клеток у больных с HR+/HER2- РМЖ.
Применение препарата Ибранса® существенно замедляет прогрессирование опухолевого процесса и увеличивает продолжительность жизни пациенток. Ибранса® является первым утвержденным FDA средством из нового класса противораковых средств – ингибиторов CDK 4/6. Препарат одобрен в Российской Федерации для лечения HR+/HER2- местнораспространенного или мРМЖ в комбинации с фулвестрантом после предшествующей гормональной терапии.
Висцеральный криз в онкологии что это такое
Л.Ю. Владимирова, И.Л. Попова, Н.А. Абрамова, А.Э. Сторожакова, Н.М. Тихановская, К.А. Новоселова, А.А. Льянова, Л.А. Рядинская, М.О. Ежова, М.А. Теплякова
Ростовский научно-исследовательский онкологический институт, Ростов-на-Дону, Россия
Обоснование. Метастатический РМЖ (мРМЖ) – неизлечимое заболевание, однако современные лечебные подходы позволяют достигать клинически значимых результатов. Методы. Были проанализированы данные об эффективности и безопасности препарата трастузумаб эмтанзин в лечении 14 пациенток с мРМЖ с висцеральными поражениями во второй линии терапии. Результаты. Общий ответ на лечение составил 71,4% (10 пациенток), из них у 1 – полная ремиссия, частичная ремиссия у 2 (14,3%), стабилизация процесса у 7 (50%), прогрессирование процесса у 4 (28,6%) пациенток. Медиана безрецидивной выживаемости не была достигнута в связи с небольшим сроком наблюдения. Общая безрецидивная выживаемость составила 58%, медиана общей выживаемости – 9 месяцев. Общая годичная выживаемость составила около 71,4%. Из токсических явлений терапии отмечены астения, тошнота, рвота, диарея, анемия, тромбоцитопения, лейкопения. Описание клинического случая. Представлен результат применения препарата в первой линии терапии HER2-положительного РМЖ в отношении пациентки 62 лет с прогрессированием во время проведения адъювантной терапии препаратом трастузумаб. Заключение. Препарат обладает высокой эффективностью для пациенток с HER-2-положительным мРМЖ при достаточно благоприятном профиле токсичности.
Для цитирования: Владимирова Л.Ю., Попова И.Л., Абрамова Н.А., Сторожакова А.Э., Тихановская Н.М., Новоселова К.А., Льянова А.А., Рядинская Л.А., Ежова М.О., Теплякова М.А. Трастузумаб эмтанзин в терапии HER2-положительного метастатического рака молочной железы у пациенток с висцеральным кризом. Фарматека. 2019;26(7):58–63. DOI: https://dx.doi.org/10.18565/pharmateca.2019.7.58-63
Актуальность
В развитых странах в структуре онкологической заболеваемости женщин рак молочной железы (РМЖ) занимает 1-е или 2-е место (20–25 % всех случаев рака). Более чем у половины больных РМЖ на том или ином этапе заболевания развиваются отдаленные метастазы. Метастатический РМЖ (мРМЖ) – неизлечимое заболевание, однако современные лечебные подходы позволяют достигать клинически значимых результатов. Выявление все новых и новых молекулярно-генетических и иммуногистохимических маркеров и их корреляций позволяет индивидуализировать тактику лечения больных [1]
К наиболее значимым факторам неблагоприятного прогноза при мРМЖ относится избыточная экспрессия HER2 – трансмембранного рецептора с активностью тирозинкиназы, что служит результатом амплификации гена HER2 в 17-й хромосоме [2, 3]. Исследования показали, что HER2-положительный подтип чаще встречается среди молодых женщин с распространенными стадиями болезни, характеризуется высокой агрессией и быстрой диссеминацией опухолевого процесса, не зависит от размеров опухоли. Даже при минимальных размерах карцином и в отсутствие поражения регионарных лимфоузлов гиперэкспрессия HER2 ассоциирована с неблагоприятным течением заболевания [3, 4]. Сегодня определение HER2-статуса при РМЖ обязательно для всех стадий заболевания, необходимо для оценки прогноза и выработки оптимального лечебного алгоритма. Определение HER2-статуса в опухоли стандартизировано и выполняется на парафиновых блоках опухоли с помощью иммуногистохимического анализа и при сомнительном результате анализа (HER2-2+) дополняется определением амплификации гена методом гибридизации in situ (ISH) [5–7].
Анти-HER2-терапия в настоящее время является стандартным подходом к лечению больных раком молочной железы (РМЖ) с гиперэкспрессией HER2 или амплификацией гена HER2 и обычно дополняет химио- или гормонотерапию [8].
Трастузумаб эмтанзин (T-DM1) представляет собой конъюгат антитела и химиопрепарата (ADC), доставляющий последний непосредственно в HER2-положительные раковые клетки, благодаря чему ограничивается повреждение здоровых тканей [8, 9].
Механизм противоопухолевого действия T-DM1 складывается из эффектов трастузумаба и DM1 и является многоступенчатым: на I этапе трастузумаб связываясь с HER2-рецептором, осуществляет весь спектр своего противоопухолевого воздействия, а именно вызывает блокаду сигнальных путей HER2, активирующих рост опухоли, и маркирует опухолевую клетку для иммунной системы. Далее образовавшиеся комплексы поступают внутрь клетки посредством обычного эндоцитоза, где при участии внутриклеточных ферментов происходит разрушение линкера и высвобождение химиопрепарата DM1, который вызывает гибель клетки за счет нарушения полимеризации микротрубочек и остановки клеточного цикла [8, 9].
Применение трастузумаба эмтанзина в монотерапии во второй линии лечения метастатического HER2-позитивного РМЖ позволяет добиваться существенного увеличения общей выживаемости до 2,5 лет и увеличить медиану времени до прогрессирования заболевания на 50% по сравнению со стандартной комбинацией лапатиниба и капецитабина (по данным исследования EMILIA) [10–12]. Представленные данные крупных рандомизированных исследований говорят о том, что современная терапия HER2-положительного РМЖ позволила перевести фатальное течение заболевания в длительно контролируемую форму [11, 12].
Задачей нашего исследования стала оценка эффективности и связанной с ним токсичности препарата трастузумаб эмтанзин (T-DM1) при лечении метастатического РМЖ у пациенток с висцеральным кризом.
Методы
В исследование включены пациентки с HER-2 положительным статусом мРМЖ, у которых имело место прогрессирование после адъювантной химио- или гормонотерапии с трастузумабом либо прогрессирование на 1-й линии химиотерапии (ХТ) и трастузумаба с развитием висцерального криза, ECOG≤2, с адекватной функцией печени, почек, костного мозга. Т-DM1 применялась в качестве 2-й линий лечения мРМЖ. Препарат назначался в дозе 3,6 мг/кг 1 раз 3 недели. Оценку эффекта проводили каждые 2–3 курса, согласно критериям RECIST 1.0, по результатам спиральной компьютерной томографии или магнитно-резонансной томографии.
Оценивали непосредственный противоопухолевый эффект. Токсичность проведенного лечения оценивалась согласно критериям CTCAE 4, анализ общей и безрецидивной выживаемости – по Каплану–Майеру. Статистическая обработка данных проводилась с помощью пакета программ Statistica 10.0.
В исследование были включены 14 пациенток в возрасте 30–49 лет, средний возраст составил 44 года (табл. 1).
По рецептурному статусу женщины распределялись следующим образом: ER+ и/или PR+ – 6 (42,9%), ER- и/или PR – 8 (57,1%).
Все больные мРМЖ исходно имели различные стадии заболевания, представленные в табл. 2.
У 71,42% пациенток исходно имела место III стадия процесса. Независимо от исходной стадии болезни к началу терапии у всех пациенток был метастатический распространенный опухолевый процесс.
У 7 (50%) пациенток отмечено прогрессирование заболевания на фоне адъювантной терапии трастузумабом, у 2 (14,3%) – на фоне гормонотерапии и трастузумаба, у 5(35,7%) – на фоне таксанов и трастузумаба.
В табл. 3 представлено распределение висцеральных метастазов: в процесс было вовлечено более трех органов и систем 4 (28,6%) пациенток: кости, печень, легкие. Метастатическое поражение одного органа у 5 (35,7%) пациенток было представлено поражением легких, сочетанное поражение легких и головного мозга у 5 (35,7%). Терапию трастузумабом эмтанзином начинали при относительно удовлетворительном состоянии пациентов (ECOG-1–2), удовлетворительных гематологических и биохимических показателях крови.
Проведено от 3 до 8 курсов лечения препаратом Т-DM1, терапию продолжали до достижения максимального эффекта или прогрессирования заболевания, или неприемлемой токсичности.
Таким образом, 3 (21,4%) больным проведено 8 курсов; 5 (35,7%) – 3 курса и в связи с прогрессированием процесса пациентки подверглись другому лечению. Остальные 6 (42,8%) пациенток получили по 6 курсов противоопухолевой терапии.
Результаты
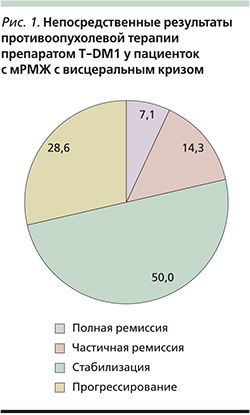
Результаты проведенного лечения представлены на рис. 1.
Общий ответ составил 71,4% (10 пациенток), из них у 1 (7,1%) наблюдалась полная ремиссия (ПР), у 2 (14,3%) – частичная (ЧР), у 7 (50%) пациенток – стабилизация процесса. Прогрессирование процесса отмечено у 4 (28,6%) пациенток.
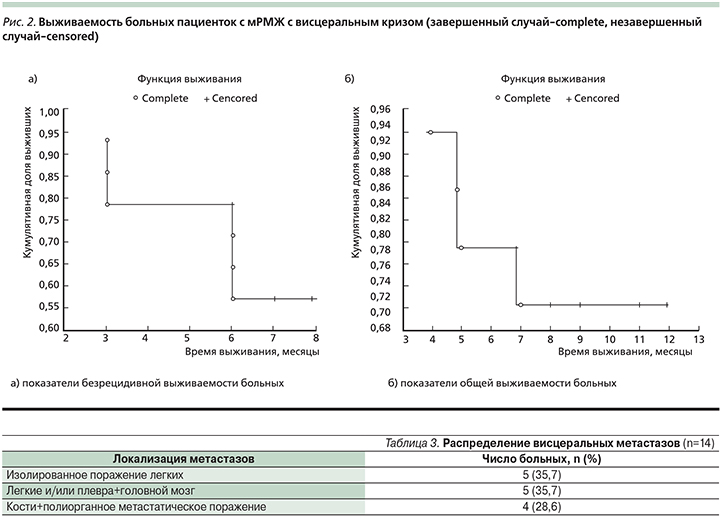
Медиана безрецидивной выживаемости не достигнута из-за небольшого срока наблюдения. Общая безрецидивная выживаемость составила 58%, медиана общей выживаемости – 9 месяцев. Общая годичная выживаемость составила около 71,4% (рис. 2).
Полученные данные по безрецидивной и общей выживаемости подтверждают мнение многих авторов об эффективности применения препарата трастузумаб эмтанзин в группе больных, ранее получавших лечение таксанами и трастузумабом, а продолжительность изучаемых показателей соответствовала литературным данным [3, 10].
При изучении токсичности проводимой химиотерапии, согласно CTC AE 4.0, нами было проанализировано 76 курсов ХТ. Согласно публикациям, к наиболее частым серьезным побочным эффектам относятся астения, тромбоцитопения, рвота, боли в животе. Из негематологических осложнений в нашей группе больных преобладали гастроинтестинальные (72%). Из них (гастроинтестинальных осложнений) чаще наблюдались тошнота – в 26,3%, боли в животе – 26,3%.
Спектр и выраженность токсических проявлений терапии препарата Т-DM1 представлены в табл. 4.
В целом следует отметить удовлетворительную переносимость препарата, несмотря на перечисленные возможные побочные эффекты, следует обратить внимание на астению 1–2-й степеней – 73,7%. Побочные эффекты в основном были слабо выражены, при появлении 3-й степени и более адекватно поддавались лекарственной коррекции.
Имея собственный опыт применения препарата Т-DM1, хотелось бы продемонстрировать наиболее впечатливший нас результат применения препарата первой линии терапии метастатического HER2-положительного РМЖ при прогрессировании во время проведения адъювантной терапии препаратом трастузумаб.
Клинический случай
Пациентка Д. 62 лет находилась на обследовании и лечении в ФГБУ РНИОИ МЗ РФ с 07.12.2016.
Образование в железе обнаружила в ноябре 2016 г., самостоятельно обратилась в РНИОИ. Обследована, выполнена трепанбиопсия опухоли правой молочной железы 07.12.2016. Верификация процесса ГА № 102350-351: карцинома. При иммуногистохимическом исследовании опухоли левой молочной железы выявлено отсутствие экспрессии рецепторов прогестерона и эстрогена (ER-и PR-, Ki-67 80%). Реакция антител с рецепторами HER2/neu 3+. Спиральная рентгеновская компьютерная томография (СРКТ) головного мозга от 07.12.2016: без очагов.
СРКТ органов шеи, грудной клетки (ОГК), брюшной полости (ОБП) и органов малого таза (ОМТ) от 07.12.2016: легкие без очагов, печень без очагов, внутригрудные, забрюшинные лимфоузлы не увеличены, патологических объемных образований в полости малого таза не выявлено.
В костях без деструкции. Остеохондроз L5–S1. В правой молочной железе опухоль 3,4×3 см, аксиллярные л/у справа до 4 см.
В результате проведенного обследования пациентке установлен диагноз «рак правой молочной железы T4N2Mo, St IIIB, нелюминальный HER-2-позитивный, кл. гр. т2».
С 12.12.2016 проведено комплексное лечение: 4 курса препаратами доксорубицин, эндоксан (циклофосфамид), далее 4 курса пертузумаб, трастузумаб, доцетаксел.
На этапах выполнялось контрольное обследование: СРКТ головы, шеи, ОГК, ОБП и малого таза от 09.06.2017: без онкопатологии.
22.06.2017 выполнена радикальная мастэктомия справа. ГА № 55368-78/17 инфильтрирующая карцинома неспецифического типа, склероз, лечебный патоморфоз 2-й степени, № 55368-78/17, в оставшейся молочной железе, клетчатках и лимфоузлах опухолtq нет.
С 13.07 по 09.08.2017 проведен курс лучевой терапии на послеоперационный рубец СОД 50 гр, на подключичную зону справа СОД 44 гр. Затем таргетная адъювантная терапия трастузумабом в течение года.
В январе 2018 г. на фоне таргетной адъювантной терапии трастузумабом появились жалобы на кашель, одышку, головокружение, головные боли.
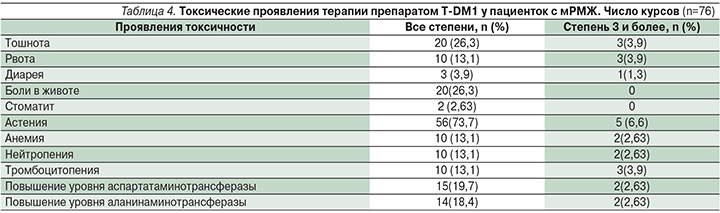
Магнитно-резонансная томография головного мозга с внутривенным контрастированием от 13.01.2018. Заключение: МР-картина солитарного опухолевого поражения левой затылочной доли 7×7 мм интракортикально с наличием перифокального отека до 11×11 мм. Кортикальная атрофия, лейкодистрофия (рис. 3а).
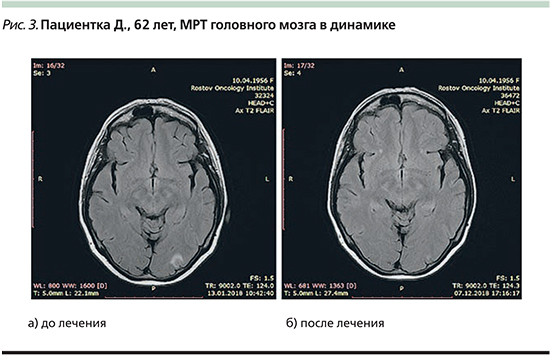
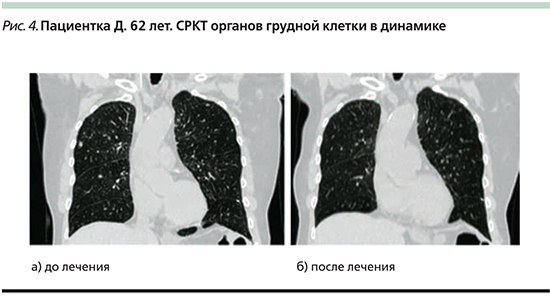
При дообследовании СРКТ органов шеи, грудной клетки, брюшной полости, малого таза от 13.01.2018: с обеих сторон множественные метастатические очаги до 1,3 см, увеличение предаортальных лимфоузлов 1,2 см (рис. 4а).
Принято решение о назначении пациентке препарата трастузумаб эмтанзин в дозе 3,6 мг/кг внутривенно 1 раз в 21-й день. На текущий момент проведено 18 циклов терапии препаратом, достигнут полного ответа.
МРТ головного мозга с внутривенным контрастированием от 07.12.2018. Заключение: МР-картина незначительной диффузной кортикальной атрофии мультифокальных супратенториальных очагов глиоза сосудистого генеза. Метастатическое поражение не определяется (рис. 3б).
СРКТ органов шеи, грудной клетки, брюшной полости, малого таза от 07.12.2018: данных за метастатическое поражение легочной ткани не выявлено (рис. 4б). Пациентка ведет активный образ жизни, работает. Из побочных эффектов, связанных с терапией, тошнота 1–2-й степеней. Планируется продолжение терапии препаратом трастузумаб эмтанзин.
Заключение
Проведенный нами анализ применения препарата Т-DM1 показал, что препарат обладает достаточно высокой эффективностью для пациенток с HER-2-положительным мРМЖ при достаточно благоприятном профиле токсичности.
Литература
1. Кит О.И., Шатова Ю.С., Новикова И.А. и др. Экспрессия р53 и BCL2 при различных подтипах рака молочной железы. Фундаментальные исследования. 2014;10:85–8.
2. Саманева Н.Ю., Владимирова Л.Ю., Новикова И.А. и др. Опыт определения HER2 статуса циркулирующих опухолевых клеток в периферической крови у больных с местно-распространенным раком молочной железы приHER2-негативном подтипе опухоли. Медицинский вестник Северного Кавказа. 2018;13(4):634–37. Doi: https://doi.org/10.14300/mnnc.2018.13124.
3. Сидорова С.С., Панферова Е.В., Пономаренко Д.М. и др. Применение T-DM1 (Кадсила) при метастатическом HER2-позитивном раке молочной железы. Эффективная фармакотерапия. 2018;31:16–8.
4. Белохвостова А.С., Рагулин Ю.А. Возможности терапии Her-2-позитивного местно-распространенного рака молочной железы. Опухоли женской репродуктивной системы. 2015;11(1):43–47. Doi: https://doi.org/10.17650/1994-4098-2015-1-43-47.
5. Стенина М.Б. Персонализированный подход к терапии распространенного HER2-положительного рака молочной железы. Современная онкология. 2014;03:21–6.
6. Колядина И.В., Поддубная И.В. Современные возможности терапии HER2-положительного рака молочной железы (по материалам клинических исследований).Современная онкология. 2014;04:10–20.
7. Семиглазова Т.Ю., Дашян Г.А., Семиглазов В.В.и др. Качество жизни – принципиальный критерий эффективности таргетной терапии метастатического HER2-положительного рака молочной железы. Современная онкология. 2015;01:19–24.
8. Стенина М.Б. Нer-2 как мишень современной противоопухолевой терапии рака молочной железы. Эффективная фармакотерапия. 2015;10:24–31.
9. Сакаева Д.Д. Клинический случай успешного применения препарата кадсила при метастатическом her2-положительном раке молочной железы. Медицинский совет. 2017;14:56–8. Doi: 10.21518/2079-701X-2017-14-56-58.
10. Krop I.E., Lin N.U., Blackwell K., et al. Trastuzumab emtansine (T-DM1) versus lapatinib plus capecitabine in patients with HER2-positive metastatic breast cancer and central nervous system metastases: a retrospective, exploratory analysis in EMILIA. Ann Oncol. 2015;26(1):113–19. Doi: 10.1093/annonc/mdu486.
11. Ross J.S., Fletcher J.A. The HER-2/neu oncogene in breast cancer: prognostic factor, predictive factor, and target for therapy. Oncologist. 1998;3(4):237–52.
12. Verma S., Miles D., Gianni L., et al., for EMILIA Study Group. Trastuzumab Emtansine for HER2-Positive Advanced Breast Cancer. N Engl J Med. 2012;367(19):1784–91. Doi: 10.1056/NEJMoa1209124.