ворота печени дифференцированы что это значит по мрт
Ворота печени дифференцированы что это значит по мрт
а) Терминология:
1. Аббревиатуры:
• Диспластический узел (ДУ)
• Регенераторный узел (РУ)
2. Синонимы:
• Цирротический узел
3. Определения:
• Ограниченная пролиферация паренхимы печени на фоне цирроза, возникающая в ответ на ее повреждение:
о При прогрессировании возникают изменения диспластического характера или происходит озлокачествление
1. Общая характеристика:
• Лучший диагностический критерий:
о РУ: множественные мелкие узелки в цирротически измененной печени, гипоинтенсивные на Т2 ВИ и GRE
о ДУ: обнаруживаются в меньшем количестве, имеют меньший размер; гиперинтенсивны на Т1 ВИ и гипоинтенсивны на Т2 ВИ
• Локализация:
о Равномерное распределение во всех отделах печени
• Размер:
о Размер регенераторных узлов обычно не превышает двух сантиметров:
— Поперечный размер диспластических узлов 2-4 см
• Морфология:
о РУ: множественные:
— ДУ: немногочисленные или единичные
о Округлые, четко отграниченные
2. Рекомендации по визуализации:
• Лучший метод диагностики:
о МРТ
• Выбор протокола:
о Т1 и Т2 ВИ; Т1 ВИ с контрастным усилением для оценки васкуляризации
о Препараты гадоксетовой кислоты (Eovist, Primovist) или гадо-беновой кислоты для дифференциальной диагностики узлов в печени:
— РУ и ДУ ожидаемо накапливают и удерживают контрастное вещество в отсроченной фазе
— Узлы ГЦР не накапливают и не удерживают контрастное вещество:
Диспластические узлы (высокой степени дисплазии) также могут не накапливать и не удерживать контраст
В некоторых случаях ГЦР показывает неравномерный («географический», «пятнистый») характер накопления контраста
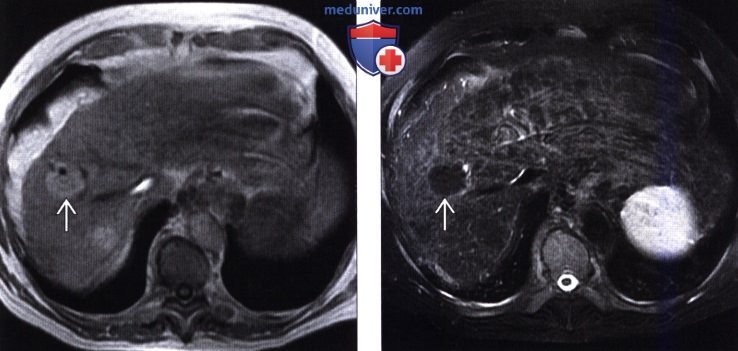
(Справа) На Т2 ВИ МР томограмме у этого же пациента образование выглядит гипоинтенсивным, что типично для диспластического узла и не характерно для гепатоцеллюлярного рака (ГЦР). 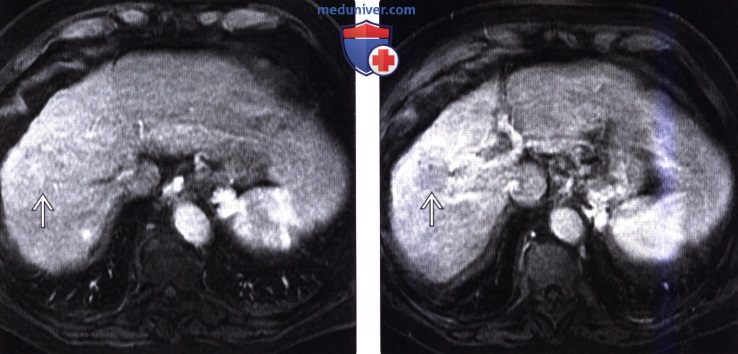
(Справа) Т1 ВИ МР томограмме в венозной фазе (этот же пациент) визуализируется образование (диспластический узел), гипоинтенсивное по сравнению с паренхимой печени; низкая интенсивность сигнала, скорее всего, обусловлена повышенным контрастным усилением печени, чем «вымыванием» контраста из узла. 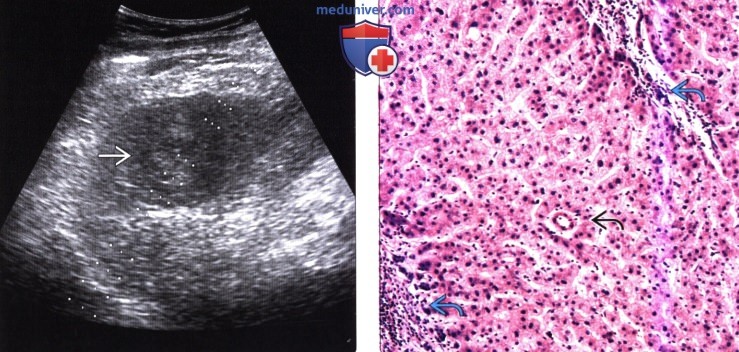
(Справа) На фотографии микропрепарата диспластического узла высокой степени дисплазии визуализируется непарная артериола. Определяется также дуктуляр-ная реакция (внутри и по периферии желчных протоков).
3. КТ признаки регенераторных и диспластических узлов:
• КТ без контрастного усиления:
о Большинство регенераторных узлов достоверно не определяются на КТ или MPT (Т1 ВИ)
о Мелкие узелки изоденсны паренхимы печени, вследствие чего их невозможно обнаружить
о Регенераторные узлы могут выглядеть более плотными по сравнению с окружающей их паренхимой печени:
— Вследствие повышенного содержания железа или гликогена
— Или за счет наличия «гало», обусловленного гиподенсными участками фиброза, окружающими узлы
• КТ с контрастным усилением:
о Регенераторные узлы накапливают контраст несколько хуже по сравнению с тканью печени:
— В результате чего они становятся неразличимыми, «исчезают»
о Диспластические узлы изо- или гиперденсны в артериальную фазу:
— Большинство из них не являются гиперваскулярными
— Избыточная васкуляризация является признаком, подозрительным на ГЦР
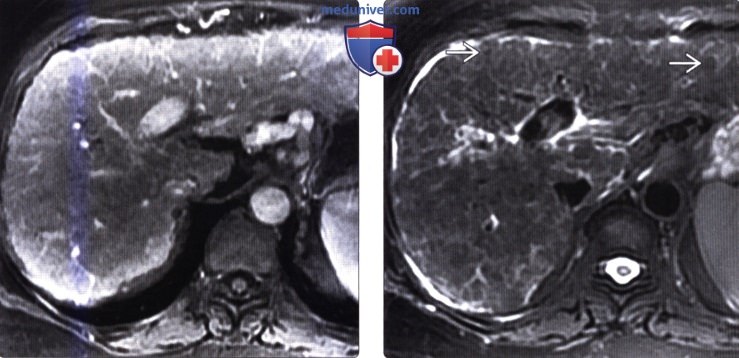
(Справа) На аксиальной Т2 ВИ МР томограмме у этой же пациентки лучше видны цирротические узелки, внешний вид которых (гипоинтенсивные очаги субсантиметрового диапазона) типичен для доброкачественных регенераторных узлов. 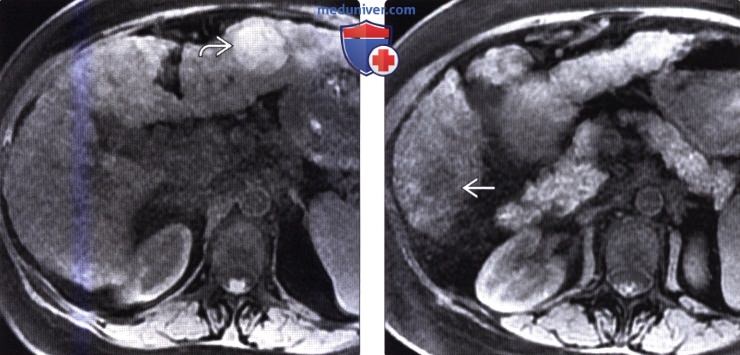
(Справа) На другой аксиальной Т1 ВИ МР томограмме у этой пациентки определяется гипоин-тенсивный очаг в шестом сегменте печени — верифицированный ГЦР. 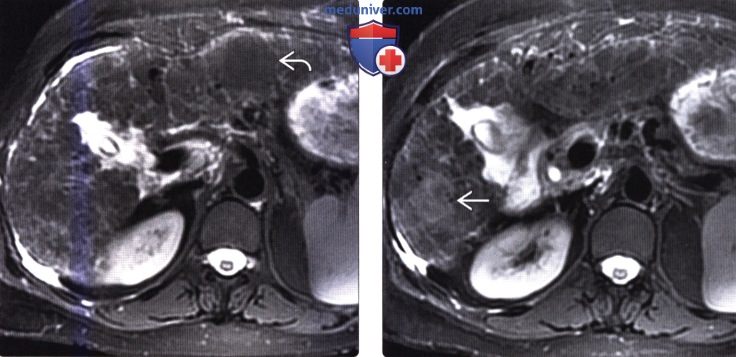
(Справа) На другой аксиальной Т2 ВИ МР томограмме у этой же пациентки визуализируется относительно гиперинтенсивный узел ГЦР (повышение интенсивности сигнала типично для злокачественного узла или объемного образования).
4. МРТ признаки регенераторных и диспластических узлов:
• Т1 ВИ:
о Регенераторные узлы:
— Характеризуются вариабельной интенсивностью сигнала
— Обычно изоинтенсивны по отношению к паренхиме печени (вследствие чего не визуализируются)
о Диспластические узлы:
— Сигнальные характеристики вариабельны
— Обычно изо- или гиперинтенсивны по отношению к печени
• Т2 ВИ:
о Регенераторные узлы:
— Низкая интенсивность сигнала по сравнению с печенью (из-за содержания железа)
— Узлы высокой степени дисплазии могут быть немного более гиперинтенсивными по сравнению с печенью
о Повышение интенсивности сигнала коррелируете высокой степенью дедифференцировки и подозрительно на ГЦР
• T2*GRE:
о РУ: снижение интенсивности сигнала по отношению к печени:
— Увеличение размеров вследствие эффекта повышения чувствительности, обусловленного железом
• DWI:
о Для РУ и ДУ низкой степени дисплазии нетипично ограничение диффузии (узлы не «светятся»)
о ДУ высокой степени дисплазии и ГЦР обычно «светятся» на DWI
• Т1 ВИ с контрастным усилением:
о РУ:
— Изоинтенсивны печени (не обнаруживаются) либо слегка гипоинтенсивны
о ДУ:
— Вариабельно гиперинтенсивны по отношению к печени:
Увеличение васкуляризации подозрительно на злокачественную трансформацию диспластического узла
• На МРТ сдимеглюмина гадобенатом или препаратами гадоксетовой кислоты регенераторные и диспластические узлы интенсивно накапливают и удерживают контрастное вещество:
о Что означает наличие функционирующих гепатоцитов
о И свидетельствует о доброкачественности изменений (РУ):
— В диспластических узлах высокой степени дисплазии и ГЦР нет функционирующих гепатоцитов, экскреция желчи отсутствует:
Вследствие чего накопления контраста не происходит (узлы гипоинтенсивны в отсроченную фазу)
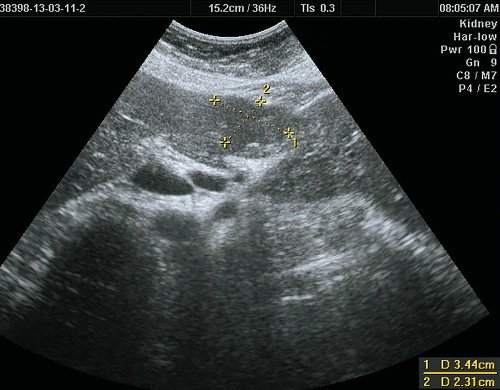
5. УЗИ признаки регенераторных и диспластических узлов:
• Узлы могут выглядеть гипо-, изо- или гиперэхогенными:
о Большинство регенераторнных и диспластических узлов не очевидны на УЗИ
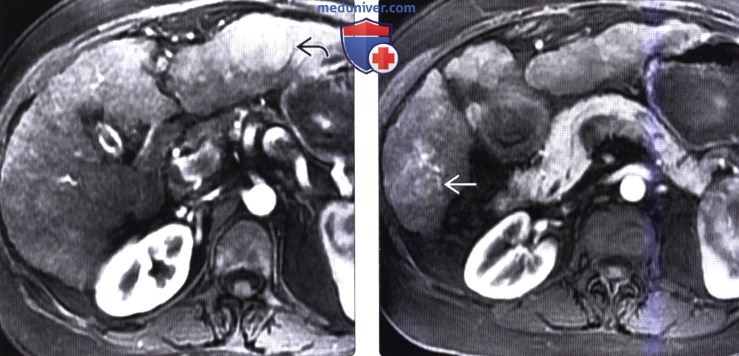
(Справа) На другой Т1 ВИ МР томограмме в артериальную фазу у этой же пациентки определяется типичное неравномерное накопление контраста узлом ГЦР. 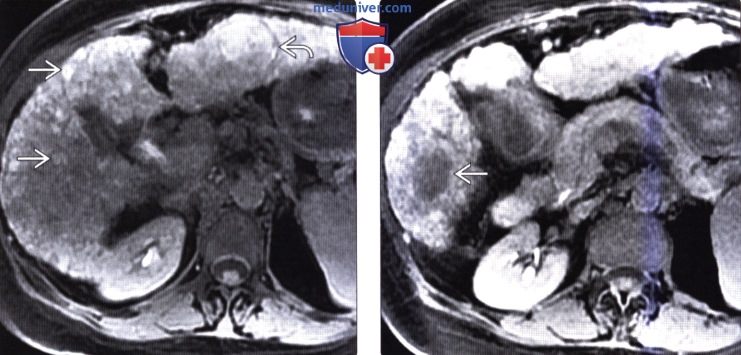
(Справа) На другой Т1 ВИ МР томограмме в отсроченную фазу (эта же пациентка) накопление контраста в узле ГЦР не определяется. 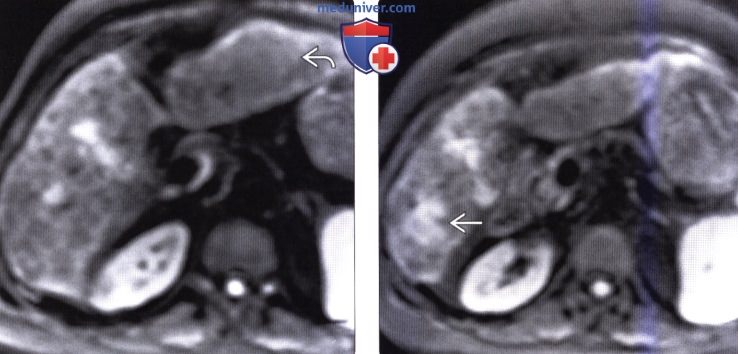
(Справа) На другой диффузионно взвешенной томограмме (эта же пациентка) определяется рестрикция диффузии в узле ГЦР (узел выглядит «ярким»), что типично для злокачественных новообразований.
в) Дифференциальная диагностика регенераторных и диспластических узлов печени:
1. Гепатоцеллюлярный рак:
• Плотность ГЦР ниже по сравнению с плотностью печени при нативной КТ и при КТ в отсроченную фазу контрастного усиления
• Узлы ГЦР неравномерно гиперваскулярны в артериальную фазу; «вымывание» контраста в венозную и отсроченную фазу является характерным признаком гепатоцеллюлярного рака
• Для ГЦР типичен вариабельно гипоинтенсивный сигнал на Т1 ВИ, гиперинтенсивный на Т2 ВИ; опухоль «светится» на DWI
• Размер обычно превышает 20 мм
• Другие характерные признаки: неоднородная структура, множественность поражения, наличие капсулы, прорастание в вены
2. Нодулярная регенераторная гиперплазия:
• Диффузная мелкоузловая трансформация паренхимы печени без фиброзных септ между узлами
• Обнаруживается в цирротически не измененной печени
• Очаговая форма: «крупные регенераторные узлы»:
о Отдельная нозологическая (патологическая) форма, а не просто цирротические регенераторные узлы, имеющие размер больше обычного
о Ассоциирована с (в порядке уменьшения частоты): синдромом Бадда-Киари, врожденными заболеваниями сердца, другими состояниями
• Узлы обычно гиперинтенсивны на Т1 ВИ и изо- или гипоинтенсивны на 12 ВИ
• Возможно появление «кольца» или «гало» на МРТ с контрастным усилением
• На КТ и МРТ с контрастным усилением узлы интенсивно накапливают контраст, в венозную фазу повышение плотности сохраняется
• Узлы обычно множественные, имеют размер 1,5-5 см
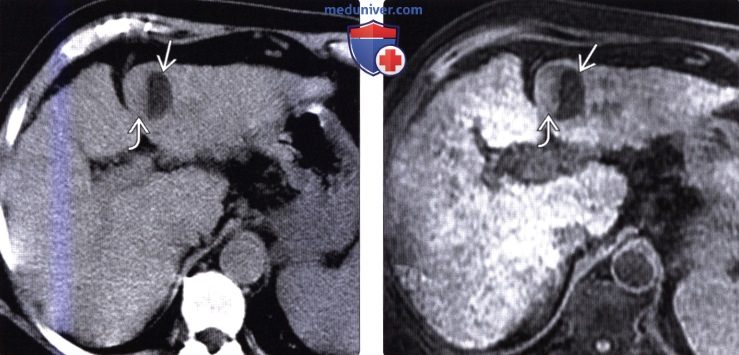
(Справа) На аксиальной Т1 ВИ МР томограмме с жироподавлением у этой же пациентки определяется, что мягкотканный компонент (справа) относительно гиперинтенсивен, что типично для диспластического узла. Интенсивность сигнала от левой части образования снижается при использовании программы жиро-подавления, что типично для опухолей, содержащих жир, и подозрительно на ГЦР. 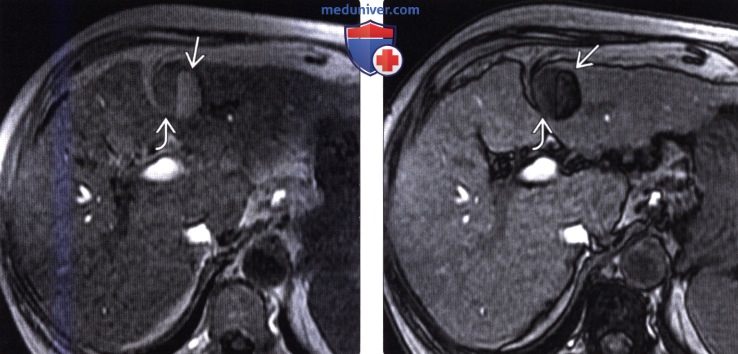
(Справа) На аксиальной МР томограмме (opposed-phase GRE) у этой же пациентки определяется подавление сигнала от участка ГЦР, содержащего жир, и гипоинтенсивный сигнал от диспластического узла. 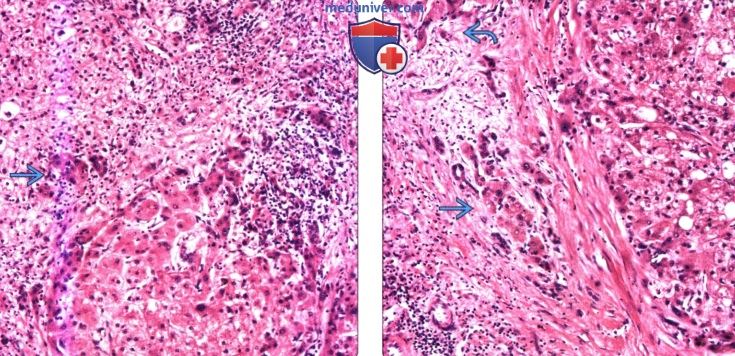
(Справа) Микропрепарат: гепатоцеллюлярный узел с признаками дисплазии высокой степени определяется инфильтрация портального тракта и фиброзной перегородки на периферии узла, что является диагностическим признаком ГЦР на ранней стадии.
1. Общая характеристика:
• Ассоциированные патологические изменения:
о Цирроз печени
• Регенераторные узлы являются доброкачественными, некоторые могут прогрессировать и становиться диспластическими
• Диспластические узлы высокой степени дисплазии представляют собой предопухолевые изменения, однако процесс их злокачественной трансформации протекает достаточно медленно
2. Стадирование, градация и классификация регенераторных и диспластических узлов печени:
• Регенераторные узлы подразделяются на малые (меньше 3 мм) и большие (3 мм и больше)
• Диспластические узлы классифицируются в зависимости от степени выраженности дисплазии (низкая или высокая)
3. Макроскопические и хирургические особенности:
• Регенераторные узлы:
о Функция гепатоцитов в регенераторных узлах не нарушена, клетки Купфера имеют нормальную плотность
о Имеют округлую форму, четкие контуры, размер большинства узлов не превышает 2 см
о Множественные, с диффузным распределением по всей печени
• Диспластические узлы:
о Для ДУ высокой степени дисплазии характерна преимущественно артериальная перфузия вследствие ангиогенеза
о По мере дедифференцировки функция гепатоцитов снижается, уменьшается плотность клеток Купфера
• Перфузия регенераторных узлов и диспластических узлов низкой степени дисплазии преимущественно портальная
• В узлах отсутствуют некротические изменения, кровоизлияния, признаки локальной инвазии
4. Микроскопия:
• Ограниченная пролиферация гепатоцитов и стромы, окруженных фиброзными перегородками
• Дифференциальная диагностика регенераторных и диспластических узлов затруднительна даже на микроскопическом уровне
• Регенераторные узлы:
о Нормальная васкуляризация, интактная ретикулярная «сеть» о Сохранная архитектоника гепатоцитов
о Отсутствие митотической активности
о Увеличение числа гепатоцитов с двумя и большим количеством ядер
• Диспластические узлы:
о Нарушение архитектоники
о Атипия, сгруппированность ядер
о ДУ низкой степени дисплазии напоминают регенераторные узлы и представляют сложность в плане дифференциальной диагностики
о ДУ высокой степени дисплазии напоминают высокодифференцированный ГЦР
д) Клинические особенности:
1. Проявления:
• Другие признаки/симптомы:
о Проявления цирроза и портальной гипертензии:
— Увеличение живота, желтуха, асцит, варикозное расширение вен и др.
2. Демография:
• Возраст:
о Взрослые люди
• Пол:
о Половая предрасположенность отсутствует:
— Алкогольный цирроз печени чаще встречается у мужчин
3. Течение и прогноз:
• Уровень трансформации диспластических узлов в ГЦР относительно невысокий
• Ведение и лечение пациентов с диспластическими узлами в печени не должно быть таким же, как и у пациентов с новообразованиями
• По мере увеличения размера узла возрастает вероятность диспластических изменений высокой степени выраженности или озлокачествления:
о Высокая степень дисплазии крайне нехарактерна для узлов размером меньше 2 см
е) Диагностическая памятка:
2. Необходимо отразить в заключении:
• Параметры плотности и интенсивности узлов в цирротически измененной печени во всех фазах контрастного усиления:
о Также необходимо оценить васкуляризацию узлов и «вымывание» контраста
ж) Список использованной литературы:
1. Rich N et al: Hepatocellular carcinoma tumour markers: current role and expectations. Best Pract Res Clin Gastroenterol. 28(5):843-53, 2014
2. Ronot M et al: Hepatocellular carcinoma: diagnostic criteria by imaging techniques. Best Pract Res Clin Gastroenterol. 28(5):795-812, 2014
3. Bartolozzi C et al: Contrast-enhanced magnetic resonance imaging of 102 nodules in cirrhosis: correlation with histological findings on explanted livers. Abdom Imaging. 38(2):290-6, 2013
4. Quaia E et al: Predictors of dysplastic nodule diagnosis in patients with liver cirrhosis on unenhanced and gadobenate dimeglumine-enhanced MRI with dynamic and hepatobiliary phase. AJR Am J Roentgenol. 200(3):553-62, 2013
5. Giorgio A et al: Characterization of dysplastic nodules, early hepatocellular carcinoma and progressed hepatocellular carcinoma in cirrhosis with contrast-enhanced ultrasound. Anticancer Res. 31(11):3977-82, 2011
6. Lee JM et al: Hepatocellular nodules in liver cirrhosis: MR evaluation. Abdom Imaging. 36(3):282-9, 2011
7. Ouedraogo NA et al: Dysplastic hepatic nodules: radiological abnormalities and histopathological correlations. Eur J Radiol. 79(2):232-6, 2011
8. Chou CT et al: Characterization of cirrhotic nodules with gadoxetic acidenhanced magnetic resonance imaging: the efficacy of hepatocyte-phase imaging. J Magn Reson Imaging. 32(4):895-902, 2010
9. Hanna RF et al: Cirrhosis-associated hepatocellular nodules: correlation of histopathologic and MR imaging features. Radiographics. 28(3):747-69, 2008
Редактор: Искандер Милевски. Дата публикации: 23.2.2020
Некоторые аспекты диагностики фокальной нодулярной гиперплазии печени (фибронодулярной гиперплазии)
УЗИ аппарат RS85
Революционные изменения в экспертной диагностике. Безупречное качество изображения, молниеносная скорость работы, новое поколение технологий визуализации и количественного анализа данных УЗ-сканирования.
Еще сравнительно недавно фокальная нодулярная гиперплазия печени (ФНГ) относилась к редким (3%) объемным образованиям печени. Однако, учитывая применение современных методов визуализации, в настоящее время ФНГ занимает 3-е место среди доброкачественных образований печени после гемангиомы и аденомы [8, 10, 14].
Согласно морфологической классификации опухолей печени, ФНГ относится к опухолеподобным процессам и характеризуется гиперплазией печеночной паренхимы, разделенной на узлы фиброзными прослойками в виде звездчатого рубца [14]. Гиперпластические узлы без четких границ переходят в окружающую ткань, не сдавливая ее. Опухоль состоит из гепатоцитов, элементов желчных протоков, купферовских клеток и фиброзной ткани.
ФНГ развивается в любом возрасте, одинаково часто у лиц разного пола. В то же время имеются данные о том, что подобные новообразования чаще диагностируются у женщин (в 82,2% случаев) [10, 17].
Макроскопически очаговая узловая гиперплазия представляет собой мягкоэластичный, четко ограниченный, иногда инкапсулированный узел серовато-коричневого цвета размером от 0,5 до 6 см. Узлы могут быть как одиночными, так и множественными и располагаться в периферических отделах правой (чаще) и левой доли. Иногда узлы заметно выбухают на поверхности печени, в редких случаях они имеют ножку. Узлы имеют дольчатую структуру с наличием фиброзных прослоек, отходящих, как правило, от центрально расположенного рубца.
При микроскопическом исследовании узлов определяют нормальные гепатоциты, содержащие гликоген и формирующие трабекулярные структуры. Местами наблюдается полиморфизм величины и формы зрелых гепатоцитов, они образуют синцитий. В центре печеночной доли, как правило, располагается центральная вена, имеются синусоиды, выстланные купферовскими клетками (звездчатые ретикулоэндотелиоциты). Портальные прослойки сформированы правильно, достаточно деликатны. В зоне звездчатого рубца и по ходу стромы располагаются сосуды. Сосу дис тый компонент весьма разнообразен как по содержанию (венозные, толстостенные артериальные сосуды с миксоматозной дегенерацией среднего слоя), так и по форме (гемангиоматоз). По ходу портальных септ определяются пролиферирующие желчные протоки, единичные мелкие узлы регенерации и лимфоплазмоцитарные инфильтраты. Эти признаки служат основными дифференциально-диагностическими критериями, позволяющими отличить ФНГ от печеночно-клеточной аденомы [17].
Выделяют 2 типа ФНГ: классическая и неклассическая. При классическом типе выделяют все 3 признака: аномальная нодулярная структура, извилистые толстостенные сосуды, гиперплазия желчных протоков. Центральный рубец присутствует в 65% наблюдений. Он всегда содержит измененные сосуды разного калибра: большие извилистые артерии с гипертрофией интимы и медии, крупные и мелкие вены, капилляры. При неклассическом типе отсутствует один из двух признаков (нодулярная структура или измененные сосуды), но гиперплазия протоков есть всегда. Централь ный рубец отсутствует. В свою очередь неклассический тип делится на 3 подтипа: телеангиэктатический (склонный к кровотечениям), аденоматозный и ФНГ с клеточной атипией.
Опухоль в большинстве случаев (66,7-80,8% пациентов) не проявляет себя клинически и может быть случайно обнаружена при проведении ультразвукового исследования (УЗИ) по иному поводу [18]. Специфичные лабораторные симптомы отсутствуют. ФНГ не озлокачествляется и край не редко вызывает осложнения в виде внутрибрюшного кровотечения.
Ультразвуковая картина ФНГ
Так, при УЗИ в В-режиме вид ФНГ неспецифичен и вариабелен. Чаще всего ФНГ печени выглядит как единичное очаговое образование с нечеткими или четкими, ровными или неровными контурами, несколько неоднородное по своей внутренней структуре, без капсулы. В 80% случаев (рис. 1) очаг изоэхогенный или гипоэхогенный [3, 8, 9, 11-14].
а) В-режим. В IV сегменте печени, выходя на контур печени, деформируя его, визуализируется тканевой плотности гипоэхогенное, несколько неоднородное по эхоструктуре образование размерами 50 х 40 мм, неправильной формы, с четкими ровными контурами.
Вторичные (метастатические) опухоли печени
Общее число больных с метастазами в печень составляет приблизительно одну треть от общего количества больных злокачественными опухолями.
В России ежегодно выявляют около 450 тысяч новых больных раком.
У значительной части из них уже имеются метастазы в печени, у других пациентов метастазы в печень могут быть выявлены в разные сроки после установления диагноза рака.
Количество всех больных с метастазами в печени в России составляет более 100 тысяч, что в десятки раз превосходит количество всех больных первичными опухолями печени и внутрипеченочных желчных протоков.
Метастазы в печень наиболее часто наблюдаются у больных с первичной опухолью толстой кишки, легких, желудка, поджелудочной железы, молочной железы. Рак желчевыводящих путей, пищевода, яичников, предстательной железы, почек, а также меланома реже поражают печень.
Чаще всего метастазы в печени повторяют строение первичных опухолей. Однако в ряде случаев метастазы отличаются от первичных опухолей по степени дифференцировки (созревания) опухолевых клеток, что затрудняет установление принадлежности первичной опухоли.
Как правило, метастатическое опухоли печени редко наблюдаются у больных циррозом печени. Это можно объяснить плохими условиями для фиксации и размножения опухолевых клеток в рубцовоизмененном органе.
Метастатический рак печени обычно характеризуется быстрым прогрессированием и отсутствием специфических лабораторных и клинических признаков.
Всех больных с метастазами в печени делят на две группы независимо от источников метастазирования:
(Более трех метастазов считаются множественными).
У больных с единичными метастазами симптомы заболевания напоминают проявления первичного рака печени (увеличение печени и тупые боли в правом подреберье при незначительных размерах опухоли).
У пациентов с множественными метастазами местные и общие симптомы более выражены и характеризуются нарастающей печеночной недостаточностью и осложнениями в виде механической желтухи.
У некоторых больных возникает отек нижних конечностей и расширение вен передней брюшной стенки в результате сдавления нижней полой вены. У 30% больных уже в момент установления диагноза имеется асцит (скопление жидкости в животе) за счет поражения брюшины.
Диагностика
Регулярное наблюдение и обследование больных, перенесших лечение по поводу злокачественной опухоли, позволяет относительно рано выявить метастазы в печени и провести соответствующее лечение. Прогноз (исход) заболевания лучше в случае обнаружения метастазов в печени после окончания лечения первичного рака различных локализаций по сравнению с больными, у которых метастазы выявлены в момент диагностики первичной опухоли.
Ультразвуковое исследование (УЗИ) позволяет решить большинство диагностических задач: размеры метастазов, связь их с крупными сосудами и протоками печени. Использование УЗИ во время операции дает возможность выявить дополнительные очаги опухоли внутри печени и помогает использовать методы местного воздействия на метастазы.
Рентгеновская компьютерная томография (РКТ) и магнитно-резонансная томография (МРТ) обычно не более эффективны, чем УЗИ, однако могут дать дополнительную полезную информацию, особенно при решении вопроса о хирургическом лечении метастазов в печени.
Пункционная биопсия (взятие кусочка ткани) печени показана в тех случаях, когда природа очагов в печени вызывает сомнения.
Ангиография (контрастное исследование сосудов) печени целесообразна при хорошо кровоснабжающихся метастазах и может помочь в уточнении локализации опухолевых очагов и их происхождении.
Всестороннее обследование позволяет решить комплекс вопросов, связанных с первичной опухолью, и определить план лечения по поводу метастатического поражения печени.
Лечение и прогноз (исход)
Лечение больных с метастазами в печень имеет особенности, отличные от лечения больных с первичными злокачественными опухолями печени и внутрипеченочных желчных протоков.
Ввиду биологических особенностей рака толстой кишки и его метастазирования, больные этой группы с метастазами в печень выделены в отдельную группу.
При хирургическом лечении метастазов рака толстой кишки большое значение придается прогностическим факторам, позволяющим судить об исходе заболевания.
К таким факторам относятся:
5-летняя выживаемость больных с метастазами рака толстой кишки в печень, перенесших частичное удаление печени, составляет 25-35%. При первично неоперабельных (неудалимых) метастазах рака толстой кишки в печени возможно проведение системной (внутривенной) и регионарной (через сосуды печени) химиотерапии. При этом после такого лечения у 15% больных удается выполнить операцию.
В первые два года у 40-60% оперированных больных может развиться рецидив (возврат) заболевания в печени. К концу третьего года без рецидива остаются около 30% оперированных больных.
К локальным методам лечения метастазов рака толстой кишки в печени относятся: радиочастотная термодеструкцая (разрушение опухоли высокой температурой), криодеструкция (уничтожение метастазов низкими температурами), введение в опухолевые узлы этанола и др.
Для системной химиотерапии больных с метастазами рака толстой кишки используют различные противоопухолевые препараты и их комбинации: фторурацил, тегафур, капецитабин, иринотекан, оскалиплатин, ралтитрексед. Эффект от химиотерапии наблюдается у 14-50% больных.
Комбинированное (сочетанное) лечение больных с метастазами рака толстой кишки в печень дает наилучшие отдаленные результаты.
Лечение метастазов других опухолей в печень
Выживаемость больных при хирургическом лечении не зависит от сроков обнаружения метастазов после удаления первичной опухоли, объема оперативных вмешательств, размеров и количества метастазов. Показатели отдаленной выживаемости лучше после резекции печени, чем при химиотерапии. Непременным условием резекции печени по поводу метастазов является полное удаление первичной опухоли. Криодеструкция, микроволновая гипертермическая коагуляция, внутриопухолевое введение этанола, уксусной кислоты, ультразвуковая фокусная, лазерная, радиочастотная термодеструкция метастазов в печени в сочетании с местной или системной химиотерапией и резекцией печени носят паллиативный характер и направлены на увеличение продолжительности жизни. Все указанные методы лечения характеризуются удовлетворительной переносимостью больными.
Комбинированное лечение
У больных с химиочувствительными метастазами в печени (рак молочной железы, рак яичка, рак яичников) оптимальным является применение операции с предварительной химиотерапией и возможной химиотерапией после операции по поводу изолированного поражения печени.
Другим вариантом лечения может быть операция в комбинации с местным воздействием (радиочастотная термодеструкция, криодеструкция, введение в опухоль этанола и др.)