высокий креатинин и низкий гемоглобин что делать
Жизнь при хронической почечной недостаточности
Как живут люди с хронической почечной недостаточностью? Если болезнь не на терминальной стадии, то пациенты проходят консервативное лечение. Стадию определяют по скорости клубочковой фильтрации (СКФ). При терминальной 5-й стадии она ниже 15 мл/мин/1,73м² — здесь уже требуется диализ или трансплантация почки. Хронической считают почечную недостаточность с 3-ей по 5-ю стадии — СКФ ниже 60 мл/мин/1,73м². На любой из них пациент должен вести особый образ жизни: соблюдать диету и ряд рекомендаций, назначаемых врачом.
В чем особенности жизни при ХПН и что делать
При хронической недостаточности почки перестают нормально выполнять свою функцию — выведение продуктов обмена с мочой. В результате они копятся в организме человека. В первую очередь это мочевина и креатинин. Именно по уровню последнего оценивают функцию почек. Высокий креатинин — это нарушение функции почек. Поэтому при ХПН важно регулярно сдавать анализы для проверки уровня этого продукта распада. Чтобы он не повышался, необходимо следовать ряду правил.
Избегать тяжелой физической нагрузки
Она повышает уровень креатинина. Это обусловлено тем, что данное вещество — конечный продукт креатин-фосфатной реакции в мышцах при их энергетическом обмене, работе и возникновении травм. Отсюда высокая физическая нагрузка — это высокий уровень креатинина, с которым и без того не работающие почки не могут справиться.
Ограничить белковые продукты
При хронической почечной недостаточности в диете ограничивают белок: при СФК ниже 50 мл/мин — до 30-40 г/сут., ниже 20 мл/мин — до 20-24 г/сут. Это необходимо, чтобы уменьшить нагрузку на почки. В то же время с началом диализа количество белка увеличивают до 1,1-1,5 г/кг/сут. Все потому, что в процессе диализа вымывается много важных компонентов, и белок на состояние почек влияет уже не так сильно.
Употреблять достаточно углеводов и жиров
Вместо белка в рационе должно быть достаточное количество углеводов и жиров. Основу рациона составляют сложные углеводы, которые не повышают глюкозу и медленно всасываются, и ненасыщенные жиры, полезные для сердца и сосудов.
Соблюдать калорийность рациона
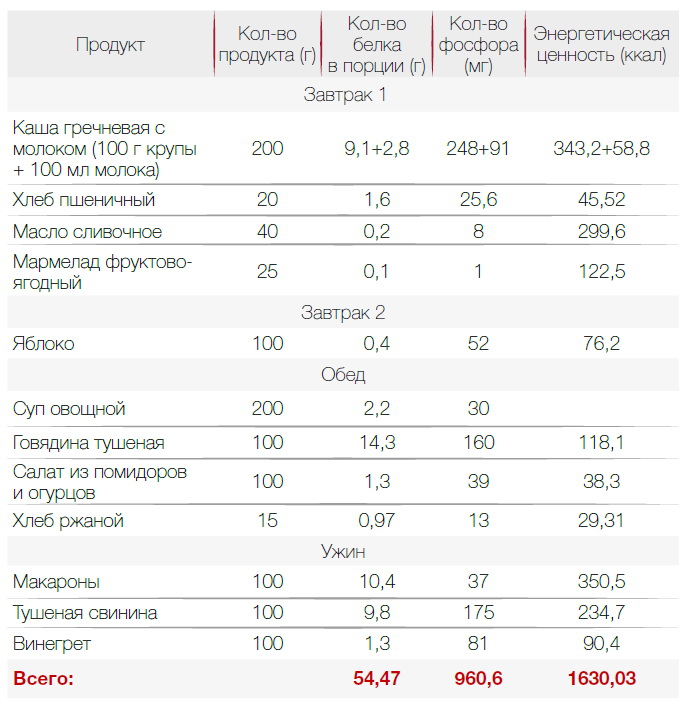
В диете при хронической почечной недостаточности важна калорийность. Она должна быть высокой — около 3000 ккал для восполнения всех витаминов и минералов. Диета назначается индивидуально, поэтому 3000 ккал — ориентировочное число. Пример меню с учетом требований приведен ниже.
Контролировать поступление микроэлементов и воды
Поскольку почки плохо работают, они не выводят калий, а от его избытка нарушается работа сердца. Поэтому количество калия, поступающего с пищей, нужно контролировать. Он содержится в картофеле и других овощах. Чтобы снизить количество калия, эти овощи перед приготовлением нужно порезать и замочить на 6-10 часов, причем как можно чаще воду менять.
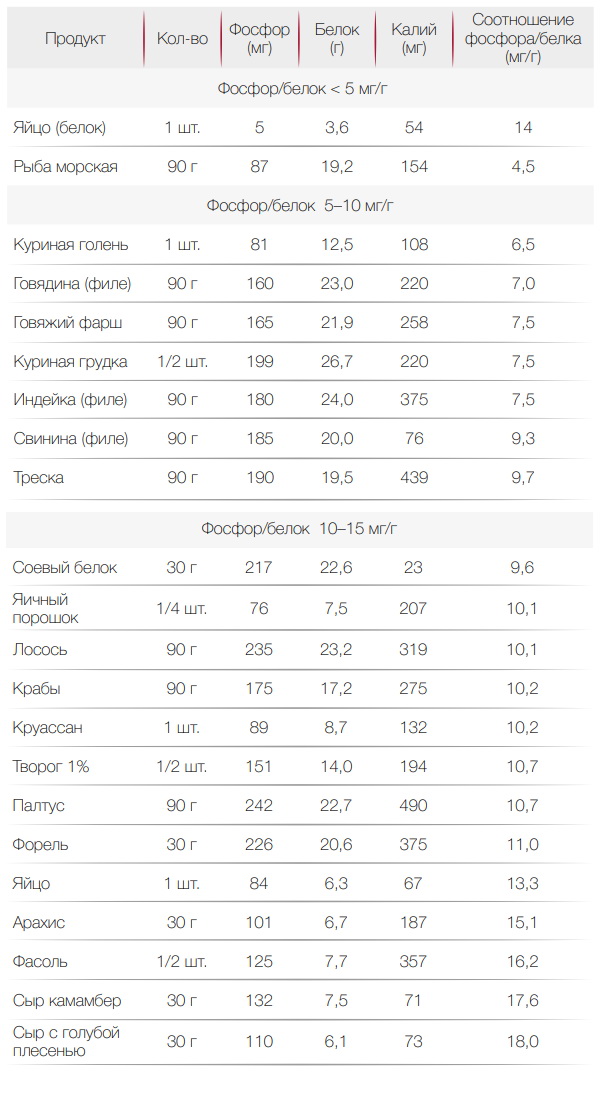
Еще необходимо ограничить поступление фосфора. При ХПН он может привести к поражению костей и сердца. Фосфор содержится в белковой пище. В растительной тоже есть, но из нее фосфор усваивается хуже. Также его количество снижается при термической обработке пищи. Выбирая продукты, стоит обращать внимание на те, что имеют низкий фосфорно-белковый индекс — ниже 20 мг/г. Примеры продуктов питания при почечной недостаточности с таким индексом приведены в таблице.
Другое важное правило питания при ХПН — следить за питьевым режимом. При выраженных отеках приходится уменьшить количество выпиваемой воды. В таком случае нужно ежедневно в одно время, после опорожнения мочевого пузыря и кишечника взвешиваться. Если вес резко увеличился — значит произошла задержка жидкости. При ограничениях количества воды можно рассасывать кусочек льда, а с сухостью во рту поможет справиться полоскание, жевательная резинка, леденцы или долька лимона.
Контролировать артериальное давление
Кровяное давление нужно контролировать, оно должны быть на уровне не выше 130/80, максимальные показатели — 140/90. Для этого на диете при ХПН количество соли в день ограничивается 2-3 г в сутки. При развитии выраженной гипертензии необходимо перейти на бессолевую диету.
Чтобы уменьшить количество соли в сутки, можно следовать таким советам:
Полезные советы для пациентов с ХПН
Образ жизни пациента с хронической почечной недостаточностью действительно полон ограничений, но это помогает долгое время поддерживать организм в нормальном состоянии. Специалисты рекомендуют вести дневник питания, внося в него все употребляемые продукты. Этот дневник в дальнейшем может быть полезен и для врача, который сможет скорректировать рацион, если состояние вдруг ухудшилось.
На кухне под рукой всегда стоит держать таблицы с содержанием в продуктах всех микро- и макроэлементов и их энергетической ценности. Для более точных расчетов рациона нужно иметь кухонные весы. Все это поможет предотвратить повышение креатинина и ухудшение работы почек.
Всегда нужно учитывать, что приведенные советы носят общий характер. Для получения точных рекомендаций необходимо обратиться к врачу. В Государственном центре урологии вы можете получить помощь по полису ОМС. Диагностика и лечение будут для вас бесплатными. Просто запишитесь на прием в онлайн-форме или по контактному номеру клиники.
Анемия у больных с хронической почечной недостаточностью: принципы терапии
Анемия является одним из серьезных осложнений хронической почечной недостаточности (ХПН), влияющих на качество жизни и общую выживаемость больных. Анемия — нормоцитарная нормохромная, при развитии недостаточности железа — гипохромная, появляется у больн
Анемия является одним из серьезных осложнений хронической почечной недостаточности (ХПН), влияющих на качество жизни и общую выживаемость больных.
Для диагностики почечной анемии редко требуется измерение уровня эритропоэтина в сыворотке крови, поскольку имеется прямая корреляция между выраженностью анемии и степенью снижения почечной функции [3].
Выраженность и длительность почечной анемии при ХПН во многом определяют тяжесть астенического синдрома у больных, степень переносимости ими физической нагрузки, снижение эффективности умственной деятельности, чувствительность к инфекциям и увеличивают опасность развития постгемотрансфузионного гемохроматоза. В консервативной стадии ХПН лишь менее 25% больных получают антианемическую терапию [1, 4], при этом лечение, как правило, начинают поздно — при среднем уровне гемоглобина (Нb) 9 г/дл [4]. Между тем в настоящее время установлено, что частота обнаружения, например, эксцентрической формы гипертрофии левого желудочка (ГЛЖ) прямо пропорциональна тяжести эритропоэтиндефицитной анемии (табл.) [2].
При далеко зашедшей ГЛЖ смертность больных с ХПН увеличивается в 4 раза, риск развития острого инфаркта миокарда — в 3–6 раз, острой левожелудочковой недостаточности и тяжелых нарушений ритма — в 4 раза [5]. Уменьшение уровня Нb на 1 г/дл повышает летальность от сердечно-сосудистых и инфекционных осложнений ХПН почти на 20% и существенно снижает качество жизни больных [6, 7].
Принципиально новые возможности в лечении почечной анемии появились, когда в 1985 г. было проведено успешное клиническое испытание препарата рекомбинантного человеческого эритропоэтина, полученного методом генной инженерии. При этом фармакологическая коррекция дефицита эритропоэтина при ХПН — заместительная гормональная терапия — обеспечивала адекватную стимуляцию костного мозга и прекращала неэффективный эритропоэз. Был обнаружен разносторонний стимулирующий эффект препарата эритропоэтина на пролиферацию эритроидных клеток, их созревание, скорость синтеза глобина, порфиринов, а также на утилизацию железа, скорость выхода ретикулоцитов из костного мозга в кровь и превращение их в зрелые эритроциты.
Современные препараты эритропоэтина — это высокоочищенные гликопротеиды, состоящие из полипептидных цепей и карбогидратной части (альфа или бета), на концах которой расположены сиаловые группы, предотвращающие инактивацию гормона. В соответствии с классификацией выделяют: эпоэтины альфа (эпрекс, эпокрин), эпоэтины бета (рекормон). Они сопоставимы по антианемическому эффекту, дозам, частоте побочных эффектов и фармакодинамике. Препараты рекомбинантного человеческого эпоэтина применяются внутривенно или подкожно. Однако способы введения эпоэтинов отличаются. Только препарат эпоэтин бета (рекормон) разрешен для подкожного введения. Подкожный способ введения эпоэтина является более безопасным и экономичным: коррекция анемии достигается в те же сроки, что и при внутривенном способе, но за счет применения меньших (в 1,5–2 раза) кумулятивных и поддерживающих доз [1, 7]. При внутривенном способе концентрация эпоэтина в крови достигается быстрее, но и период полувыведения в 2–3 раза короче.
В последнее время апробирован одноразовый способ введения подкожно суммарной недельной дозы эпоэтина бета и получен сравнимый с обычным режимом введения (2–3 раза в нед) эффект, что значительно облегчает практическое применение препарата. При этом частота и характер побочных эффектов не отличаются от тех, которые возникают при стандартном режиме введения эпоэтина бета [5, 7].
Клинические эффекты препаратов эпоэтина
Антианемический эффект эпоэтина заключается в быстрой нормализации числа эритроцитов, Нb и показателя гематокрита (Ht) крови. Ранними признаками эффективности лечения являются 2–3-кратное увеличение ретикулоцитов крови и быстрое снижение уровня сывороточного ферритина, отражающее мобилизацию запасов железа организма больного. За счет ликвидации зависимости больных ХПН от гемотрансфузий и активного потребления эндогенного железа для синтеза эритроцитов устраняется перегрузка железом — постгемотрансфузионный гемохроматоз. Лечение эпоэтином уменьшает повышенную кровоточивость при уремическом геморрагическом синдроме, восстанавливая адгезивные свойства тромбоцитов [8].
Кардиопротективный эффект развивается через 3–6 мес лечения. Коррекция анемии эпоэтином через воздействие на гиперкинетический тип кардиогемодинамики и гипоксическую вазодилатацию уменьшает преднагрузку и ведет к обратному развитию ГЛЖ в консервативной стадии ХПН и у части больных на диализном этапе. Кроме того, коррекция анемии снижает риск смерти от ишемической болезни сердца (ИБС), что объясняется уменьшением ишемии миокарда, активацией миокардиального неоангиогенеза, стабилизацией центральной гемодинамики и сердечного ритма [1, 6, 9]. Однако у части больных на гемодиализе наблюдается недостаточный кардиопротективный эффект эпоэтина, что объясняют поздним назначением эпоэтина и неполной коррекцией анемии [9].
Длительное лечение эпоэтином оказывает анаболический эффект, что важно для профилактики прогностически неблагоприятного синдрома белково-энергетической недостаточности (mal-nutrition), часто встречающегося у диализных больных. Под влиянием эпоэтина улучшается аппетит и усиливается синтез альбумина в печени, а также увеличивается «сухой» вес за счет прироста мышечной массы [9]. Лечение эпоэтином стимулирует рост у детей при уремическом нанизме и уменьшает проявления уремического гипогонадизма у взрослых больных с ХПН [7].
Кроме того, при длительном применении эпоэтина отмечается снижение заболеваемости инфекциями. Ликвидация зависимости больных ХПН от гемотрансфузий оказывает существенное влияние на распространенность диализных гепатитов В и С. Повышение резистентности к инфекциям связано также с уменьшением тканевой гипоксии и снижением частоты вторичного гемохроматоза. Вакцинация, антибактериальная и противовирусная терапия более эффективны у больных с ХПН, систематически получающих эпоэтин [5, 7].
Показания и противопоказания к лечению эпоэтином
Поскольку по мере удлинения срока персистирования анемии у больных с ХПН увеличивается риск кардиальной смертности, целесообразно начинать лечение эпоэтином при первых проявлениях анемии [1, 9]. Рекомендуется добиваться ранней, полной коррекции Нb с целью кардиопротекции — профилактики развития эксцентрической ГЛЖ [1, 7].
Показанием к назначению эпоэтина является впервые выявленное снижение Нb (ё 12 г/дл), развивающееся при ХПН задолго до наступления ее терминальной стадии [1, 7, 9].
Больным с терминальной стадией ХПН, находящимся на заместительной почечной терапии, эпоэтин назначают внутривенно после сокращения микрокровопотерь и оптимизации режима гемодиализа (или ПАПД). Абсолютные показания к лечению: Нb 50 мг/мл) показано обследование больного ХПН с целью диагностики сопутствующего или сохраняющегося воспалительного процесса (острая инфекция, активность системного заболевания) и последующего антибактериального и/или противовоспалительного лечения перед началом терапии эпоэтином [1, 10].
Дефицит железа должен быть устранен до назначения эпоэтина [10, 11]. При выявлении гипоферритинемии ( 10%): на додиализной стадии ХПН на 2–3 нед назначают препараты трехосновного железа (мальтофер или феррум лек) внутрь (200 мг/сут). При отсутствии эффекта препараты железа вводят внутривенно. Для внутривенного введения используют венофер (трехосновное железо) 100–200 мг/нед или феррлецит (двухосновное железо) 62,5–125 мг/нед. У больных на гемодиализе предпочтительно внутривенное введение препаратов железа во время очередной процедуры диализа.
В додиализную стадию ХПН эпоэтин вводят больным подкожно в дозе 90–120 ЕД/кг/нед. При этом необходимо постепенное (за 4 мес) достижение целевого Нb (13,5–14 г/дл), соответствующего полной коррекции анемии. Баланс железа можно поддерживать с помощью перорального приема препаратов железа (мальтофер или феррум лек), назначаемого 1 раз в день за 2 ч до еды. При этом доза элементарного железа должна быть не менее 200 мг/сут. Несмотря на то, что препараты трехвалентного железа (мальтофер и феррум лек) всасываются менее активно, чем препараты двухвалентного железа (например, фенюльс или сорбифер дурулес и др.) они меньше повреждают слизистую. Препараты железа не следует принимать вместе с продуктами и лекарствами, резко подавляющими его всасывание или вызывающими раздражение слизистой оболочки (антибиотики). В процессе лечения необходим поcтоянный контроль за остаточной функцией почек (динамикой СКФ и креатинина крови), артериальной гипертензией (включая суточное мониторирование), гидратацией (ОЦК), кардиогемодинамикой. Поэтому особенно важное значение имеет комбинация эпоэтина с антигипертензивной терапией, а также с соблюдением малобелковой диеты (0,8–0,6 г белка на 1 кг массы тела) и ограничением натрия [1, 7].
Лечение эпоэтином начинают после нормализации уровня ферритина и увеличения TSAT. При исходно нормальных показателях обмена железа или отсутствии признаков перегрузки железом (повышение уровня ферритина более 800 мкг/л, а TSAT — более 50%, снижение гипохромных эритроцитов 2 г/дл, Нt > 2%) [7]. Гипертензия приcоединяется в первые недели лечения эпоэтином, может сопровождаться острой энцефалопатией с гипервискозным синдромом, негативно влиять на остаточную функцию почек. Для профилактики усугубления артериальной гипертензии у больных с ХПН следует начинать лечение с низких доз эпоэтина, вводить его подкожно, мониторировать артериальное давление и не допускать высокого прироста Нb, контролируя дозу эпоэтина. При наличии факторов риска систолической артериальной гипертензии дозу эпоэтина следует повышать не чаще 1 раза в месяц и не более чем на 20 ЕД/кг массы тела, чтобы ежемесячный прирост Hb был ниже 1 г/дл (соответственно прирост Ht не более 0,5%). Для коррекции эпоэтинассоциированной гипертензии в первую очередь нужно интенсифицировать режим гемодиализа. Если этого недостаточно, присоединяют антигипертензивные препараты (антагонисты кальция) и антиагреганты (дипиридамол). В случае если антигипертензивная терапия не позволяет полностью контролировать дозозависимую гипертонию, доза эпоэтина должна быть снижена еще в фазе коррекции уровня Hb. При развитии острой энцефалопатии необходима временная отмена эпоэтина [1, 7].
Таким образом, препараты эпоэтина как средство патогенетической заместительной терапии существенно увеличивают выживаемость и повышают качество жизни больных с ХПН. Безопасность и эффективность лечения эпоэтином определяются правильностью выбора дозы препарата, целевого Hb (Ht), адекватностью контроля за гипертензией, скоростью прироста Hb (Ht) и содержанием железа в организме больного.
Литература
Ю. С. Милованов, кандидат медицинских наук, доцент
Л. В. Козловская, доктор медицинских наук, профессор
А. Ю. Николаев, доктор медицинских наук, профессор
В. В. Фомин, кандидат медицинских наук
Л. Ю. Милованова
ММА им. И. М. Сеченова, Москва
ВЗАИМОСВЯЗЬ УРОВНЯ ГЕМОГЛОБИНА, КРЕАТИНИНА И МОЧЕВИНЫ, ПОКАЗАТЕЛЕЙ ЛИПИДНОГО СПЕКТРА И ПАРАМЕТРОВ ЭХО-КАРДИОСКОПИИ У ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ
1 Кандидат медицинских наук, 2 Профессор, доктор медицинских наук, 3 Доцент, кандидат медицинских наук, ГБОУ ВПО Ярославский государственный медицинский университет РФ; 4 Кандидат медицинских наук; ГБУЗ Ярославской области Клиническая больница № 1 г. Ярославля
ВЗАИМОСВЯЗЬ УРОВНЯ ГЕМОГЛОБИНА, КРЕАТИНИНА И МОЧЕВИНЫ, ПОКАЗАТЕЛЕЙ ЛИПИДНОГО СПЕКТРА И ПАРАМЕТРОВ ЭХО-КАРДИОСКОПИИ У ПАЦИЕНТОВ С ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ
Аннотация
В статье рассмотрена взаимосвязь уровня гемоглобина, креатинина и мочевины, показателей липидного спектра – общего холестерина, липопротеидов высокой и низкой плотности, параметров ЭХО-кардиоскопии у пациентов с хронической сердечной недостаточностью (ХСН) на фоне гипертонической болезни и ИБС в зависимости от стадии и функционального класса ХСН. Показана динамика данных параметров в зависимости от нарастания стадии и функционального класса ХСН, выявлены корреляционные связи между данными показателями.
Ключевые слова: сердечная недостаточность, анемия, гемоглобин, креатинин, холестерин.
1 PhD, 2 Professor, MD, 3 associate Professor, PhD, Yaroslavl state medical University, Yaroslavl, Russian Federation, 4 PhD, Yaroslavl region Clinical hospital № 1 of the city of Yaroslavl
THE RELATIONSHIP OF HEMOGLOBIN LEVEL, CREATININE AND UREA, LIPID PROFILE AND PARAMETERS OF THE ECHO CARDIOSCOPY IN PATIENTS WITH CHRONIC HEART FAILURE
Abstract
The article examined the relationship of hemoglobin level, creatinine and urea, lipid profile – total cholesterol, lipoproteins of high and low density, the parameters of the ECHO cardioscopy in patients with chronic heart failure (CHF) with essential hypertension and ischemic heart disease depending on the stage and functional class of CHF. The article describes the dynamics of these parameters depending on the growth stage and functional class of CHF, revealed correlation between these parameters.
Key words: chronic heart failure, anemia, hemoglobin, creatinine, cholesterol
Актуальность работы: в последние десятилетия во всем мире отмечается непрерывный рост количества больных с ХСН, что в первую очередь связано с успешным лечением и снижением летальности от острых форм ИБС, поскольку именно ИБС занимает одно из ведущих мест среди причин развития ХСН (1,2).
В настоящее время разработаны программы комплексного лечения больных ХСН, включающие применение ингибиторов АПФ, b-блокаторов, диуретиков. Однако поиск новых путей лечения больных с ХСН, направленных на улучшение качества жизни пациентов, снижение числа госпитализаций и увеличение продолжительности жизни, остается актуальным. Одной из таких возможностей является своевременное выявление и терапия состояний, усугубляющих тяжесть ХСН, в частности, – анемии.
Среди множества коморбидных состояний и осложнений ХСН, анемия наименее изучена. Это состояние, несомненно, ухудшает прогноз, усложняя течение кардиологических заболеваний и увеличивая смертность. Однако в отношении распространенности анемии и адекватной ее коррекции существует много нерешенных вопросов.
Цель работы: оценить частоту встречаемости анемии, уровень гемоглобина, креатинина, мочевины, показатели липидного спектра, параметры ЭХО-кардиоскопии (ЭХО-КС), а также их взаимосвязь у пациентов с хронической сердечной недостаточностью на фоне ИБС и гипертонической болезни (ГБ) в зависимости от стадии и функционального класса ХСН.
Материалы и методы: проведен ретроспективный анализ 180 историй болезни пациентов с ХСН на фоне ИБС и ГБ, 125 женщин и 55 мужчин, средний возраст 73,87±9,23 лет. У 106 больных (63%) были диагностированы различные формы ИБС, в т.ч. стабильная стенокардия у 105 человек (63%) ПИКС – у 51 (31%), различные нарушения ритма – у 102 (61%), ГБ – у 95 человек (57%), сочетание ИБС и ГБ – у 61 человека (37%). Исследовали показатели общего анализа крови – количество эритроцитов (ЭР) и уровень гемоглобина (HGB), цветовой показатель (ЦП), уровень креатинина(CRE) и мочевины (URE), показатели липидного спектра – холестерин (ОХ), липопротеиды высокой (ЛПВП) и низкой плотности (ЛПНП), триглицериды (ТГ), а также параметры ЭХО-кардиоскопии в зависимости от стадии и функционального класса ХСН. Сократительную способность миокарда оценивали по скорости движения фиброзных колец митрального и трикуспидального клапана.
Результаты:
В ходе ретроспективного анализа историй болезни ХСН I стадии (ХСН I) выявлена у 16 больных – 9 % обследованных, IIа стадии (ХСН IIа) – у 110 – 61%, IIб стадии (ХСН IIб) – у 43 больных – 24 %, III стадии (ХСН III) – у 11 – 6%. ХСН 1 функционального класса (1ФК) диагностирована у 4% обследованных, ХСН 2ФК у 28% обследованных, ХСН 3ФК у 58%, ХСН 4 ФК – у 10%.
Анемия легкой степени (снижение гемоглобина у мужчин менее 120г/л, у женщин – менее 110 г/л до 90 г/л) обнаружена у 24 человек – 14,6% всех обследованных с ХСН IIА-III стадии, из них 9 мужчин (4,8%) и 15 женщин (8,4%). При ХСН IIА анемия выявлялась у 12 человек – 11% обследованных, при ХСН IIб – у 8 – 16%, при ХСН III – у 5 – 40%. Анемия обнаружена у 2 % пациентов с ХСН ФК2, у 18% с ХСН ФК3, у 24% с ХСН ФК 4.
Установлено, что у больных с ХСН III концентрация HGB и цветовой показатель(118,10±33,75 и 0,78±0,13) достоверно ниже, чем у больных с ХСН IIА (133,21±18,74 и 0,86±0,07) и ХСН IIб (135,55±20,20 и 0,87±0,07 соответственно).
У обследованных с ХСН IIБ показатели CRE и URE были достоверно выше по сравнению с ХСН IIА (0,098±0,033 и 8,72±4,40 против 0,088 ±0,017 и 6,80±3,02 соответственно), а уровень ОХ и ЛПВП – достоверно ниже (4,63±1,20 и 1,12±0,22 против 5,37±1,14 и 1,33±0,42 соответственно). У обследованных с ХСН III показатели CRE и URE также были достоверно выше, а уровень ОХ и ЛПВП – ниже, чем у больных с ХСН IIБ. Достоверное повышение CRE, URE и снижение ОХ и ЛПВП также установлено в группе ХСНIIБ при сравнении с ХСНI и в группе с ХСН III в сравнении с ХСН IIА.
У лиц с ХСН 3ФК, по сравнению с ХСН 2ФК, также отмечалось достоверное повышение CRE, URE и снижение ОХ и ЛПВП.
У обследованных с ХСН IIа показатели ЭХО-КС не имели достоверных отличий по сравнению с лицами с ХСН I. У пациентов с ХСНIIб выявлено достоверное увеличение размеров левого предсердия (ЛП), увеличение конечно-систолического размера (КСР), конечно-диастолического объема (КДО), конечного систолического объема (КСО) и достоверное уменьшение фракции выброса (ФВ) по сравнению с лицами с ХСН IIа. У больных с ХСН IIб была также достоверно ниже, чем при ХСН I, ФВ. У обследованных с ХСН 2ФК, по сравнению с лицами с ХСН 1ФК, достоверных отличий не было, а у пациентов с ХСН 3ФК, по сравнению с лицами с ХСН 2ФК, отмечалось достоверное увеличение размеров ЛП, КДР, КСР, КДО, КСО.
По всей группе обследованных с ХСН установлены достоверные отрицательные корреляции между Эр и CRE и URE, между HGB и СRE и URE и положительные корреляции между HGB и ОХ, ЛПВП, ТГ. Сходные корреляции были установлены в подгруппах больных с разными стадиями ХСН. В группе с ХСН IIА установлены достоверные отрицательные корреляции между Эр и CRE, положительные корреляции между HGB и ОХ, с ХСН IIБ – достоверные отрицательные корреляции между Эр и CRE, HGB и CRE. В группе с ХСН ФК3 также установлены достоверные отрицательные корреляции между Эр и CRE, HGB и CRE, положительные корреляции между HGB и ОХ.
В группе пациентов с ХСН IIБ выявлены достоверные отрицательные корреляции между HGB и КДО, КСО, УО и толщиной ЗСЛЖ, а также между ЦП и КДО и КСО.
Выводы: Анемия диагностируется у 14,6 % больных с IIA-III стадиями ХСН. Ее распространенность увеличивается при нарастании стадии ХСН, настигая максимума при III стадии, когда она выявляется у 40% больных. При ХСН IIA, а особенно при ХСН III наблюдается повышение уровня креатинина и мочевины и снижение концентрации ОХ и ЛПВП. Возрастание концентрации креатинина и мочевины, по-видимому, является проявлением кардио-ренального синдрома на фоне ХСН. В свою очередь, ухудшение функции почек, учитывая их важную роль в регуляции эритропоэза, способствует нарастанию анемии. Это подтверждает установленные нами отрицательные корреляции между уровнем CRE и URE и количеством эритроцитов и концентрацией HGB. Снижение уровня ОХ и ЛПВП, по всей вероятности, является следствием кардиального фиброза печени. Последняя также имеет существенное значение для эритропоэза, участвуя в синтезе трансферрина, эритропоэтинов и ингибиторов эритропоэза, т. е. снижение функции печени при ХСН также способствует развитию анемии.
Литература