отклонения в объеме жидкой лекарственной формы
Отклонения в объеме жидкой лекарственной формы
от 16 октября 1997 г. N 305
О нормах отклонений, допустимых при приготовлении лекарственных средств и фасовке промышленной продукции в аптеках
С целью повышения качества лекарственных средств, изготовляемых в условиях аптек, приказываю:
1. Ввести в действие «Инструкцию по оценке качества лекарственных средств, изготовляемых в аптеках» (приложение 1) и «Нормы отклонений, допустимые при изготовлении лекарственных форм (в том числе гомеопатических) и фасовке промышленной продукции в аптеках» (приложения 2, 3, 4).
2. Органам управления здравоохранения и фармацевтическим организациям в субъектах Российской Федерации обеспечить во всех аптеках, аптечных пунктах (с правом изготовления лекарственных средств) и территориальных контрольно-аналитических лабораториях, осуществляющих контроль качества лекарственных средств, изготовляемых в аптеках, выполнение требований «Инструкции по оценке качества лекарственных средств, изготовляемых в аптеках» (приложение 1) и «Норм отклонений, допустимых при изготовлении лекарственных форм (в том числе гомеопатических) и фасовке промышленной продукции в аптеках (приложения 2, 3, 4).
3. Считать недействующими на территории Российской Федерации приказ Министерства здравоохранения СССР от 27.09.91 N 276 «О нормах отклонений, допустимых при изготовлении лекарственных форм и фасовке промышленной продукции в аптеках».
4. Контроль за выполнением настоящего приказа возложить на заместителя Министра Вилькена А.Е.
по оценке качества лекарственных средств, изготовляемых в аптеках
(утв. приказом Минздрава РФ от 16 октября 1997 г. N 305)
1. Качество лекарственных средств (в том числе гомеопатических), изготовляемых в аптеках, устанавливается по комплексу показателей, характеризующих их качество.
Уровень качества лекарственных средств оценивается в соответствии с требованиями, регламентированными действующими Государственной Фармакопеей, приказами и инструкциями Министерства здравоохранения Российской Федерации.
См. инструкцию по изготовлению в аптеках жидких лекарственных форм, утв. приказом Минздрава РФ от 21 октября 1997 г. N 308
2. Для оценки качества лекарственных средств, изготовленных в аптеках, применяются два термина; «Удовлетворяется» («Годная продукция») или «Не удовлетворяет» («Брак») требованиям действующих требованиям действующих Государственной Фармакопеи, приказов и инструкций Министерства здравоохранения Российской Федерации.
3. Уровень качества изготовленных лекарственных средств определяется органолептическими и измерительными методами.
См. Инструкцию по контролю качества лекарственных средств, изготовляемых в аптеках, утвержденную приказом Минздрава РФ от 16 июля 1997 года N 214
4. Неудовлетворительность изготовленных лекарственных средств устанавливается по следующим показателям их качества:
4.1. Несоответствие по описанию (внешний вид, цвет, запах);
4.2. Несоответствие по прозрачности или цветности;
4.3. Несоответствие по распадаемости;
4.4. Несоответствие по измельченности или смешиванию порошков, мазей, суппозитариев, гомеопатических тритураций;
4.5. Наличие видимых механических включений;
4.6. несоответствие прописи по подлинности;
4.6.1. Ошибочная замена одного лекарственного вещества другим, отсутствие прописанного или наличие непрописанного вещества;
4.6.2. Замена лекарственных средств на аналогичные по фармакологическому действию без обозначения этой замены на требовании, рецепте (копии рецепта, этикетке);
4.7. Отклонения от прописи по массе или объему;
4.7.1. Отклонение по общей массе (объему);
4.7.2. Отклонения по массе отдельных доз и их количеству;
4.7.3. Отклонения по массе навески (или концентрации) отдельных лекарственных веществ;
4.8. Несоответствие по величине рН;
4.9. Несоответствие по величине плотности;
4.10. Несоответствие по стерильности;
4.11. Несоответствие по микробиологической чистоте;
4.12. Нарушение фиксированности укупорки (для стерильных лекарственных форм);
4.13. Нарушение действующих правил оформления лекарственных средств, предназначенных к отпуску.
5. Изменения в составе лекарственных форм (если необходимо) должны производиться с согласия врача, за исключением случаев, установленных действующими Государственной Фармакопеей, приказами и инструкциями Минздрава России и должны отмечаться на требовании, рецепте (копии рецепта, этикетке). При отсутствии указанной отметки на требовании, рецепте (копии рецепта, этикетке) качество изготовления лекарственной формы оценивается «Неудовлетворительно».
6. Изменения в количестве отпущенного лекарственного средства или отпуск таблеток вместо порошков должны также отмечаться на требовании, рецепте (копии рецепта, этикетке).
7. При определении отклонений в проверяемых лекарственных формах следует использовать измерительные средства того же типа (с одинаковыми метрологическими характеристиками), что и при их изготовлении в аптеках.
лекарствами и медицинской техникой Т.Г.Кисанов
допустимые при изготовлении лекарственных форм
(в том числе гомеопатических) в аптеках
(утв. приказом Минздрава РФ от 16 октября 1997 г. N 305)
2.1. Отклонения, допустимые в массе отдельных доз (в том числе при
фасовке)*(1) порошков и общей массе гомеопатических
2.2. Отклонения, допустимые в общей массе гранул гомеопатических (в
том числе при фасовке) для одной упаковки
2.3. Отклонения, допустимые в массе отдельных доз суппозиториев и
Определяют среднюю массу взвешиванием (с точностью до 0,01 г) не менее 10 суппозиториев*(3) или пилюль.
Отклонения в массе суппозиториев и пилюль от средней массы определяют взвешиванием каждого суппозитория или пилюли с минимальной выборкой 5 штук.
Допустимые отклонения от средней массы не должны превышать:
— для суппозиториев +- 5 %
— для пилюль массой до 0,3 г +- 10 %
— для пилюль массой свыше 0,3 г +- 5 %
2.4. Отклонения, допустимые в массе навески отдельных лекарственных
веществ в порошках, пилюлях и суппозиториях (при изготовлении
методом выкатывания или выливания)*(4)
2.5. Отклонения, допустимые в общем объеме жидких лекарственных форм
при изготовлении массо-объемным способом*(5)
2.6. Отклонения, допустимые в общем объеме растворов для инъекций,
изготовляемых в виде серийной внутриаптечной заготовки при
фасовке (розливе) в градуированные бутылки для крови
При отмеривании (и фасовке) жидкостей после слива струей дается выдержка на слив капель:
2.7. Отклонения, допустимые в массе навески отдельных лекарственных
веществ в жидких лекарственных формах при изготовлении
2.8. Отклонения, допустимые в общей массе жидких лекарственных форм
при изготовлении способом по массе*(5)
2.9. Отклонения, допустимые в массе навески отдельных лекарственных
средств в жидких лекарственных формах при изготовлении
способом по массе и в мазях*(5)
1. Отклонения, допустимые в массе навески отдельных лекарственных веществ в жидких лекарственных формах при изготовлении способом по массе или массо-объемным способом, а также в мазях, определяются не на концентрацию в процентах, а на массу навески каждого вещества, входящего в эти лекарственные формы (приложение 2, пп. 2.7 и 2.9.).
Например, при изготовлении 10 мл 2% раствора пилокарпина гидрохлорида берут массу навески 0,2 г, для которой допускается отклонение +- 10 %. При анализе достаточно установить, что было взято не менее 0,18 г и не более 0,22 г пилокарпина гидрохлорида.
2.10. Отклонения, допустимые в общей массе мазей
При изготовлении лекарственных средств в виде серий внутриаптечной заготовки отклонения, допустимые в массе навески отдельных веществ, определяются на массу навески каждого вещества, взятую для изготовления требуемого объема (или массы) данной серии (в одной емкости от одной загрузки препарата).
Например, при изготовлении 2 л 0,9 % раствора натрия хлорида берут массу навески 18 г, для которой допускается отклонение +- 3 %. При химическом контроля достаточно установить, что было взято не менее 17,46 г и не более 18,54 г натрия хлорида.
Отклонения, допустимые в массе навески отдельных веществ в лекарственных средствах, изготовленных в виде серий внутриаптечной заготовки и изъятых из аптеки для проверки, определяются, как указано выше (п.2 и п.3).
Например, на проверку изъята лекарственная форма по прописи:
При химическом контроле достаточно установить, что в растворе содержится не менее 1, 71 г и не более 1, 89 г натрия хлорида (отклонение +- 5 %, приложение 2., п.2.7.).
2.11. Отклонения, допустимые в концентратах:*(6)
— при содержании лекарственного вещества до 20 %
не более +- 2 % от обозначенного процента;
— при содержании лекарственного вещества свыше 20 %
не более +- 1 % от обозначенного процента.
2.12. Отклонения, допустимые в гомеопатических тритурациях,
растворах и разведениях жидких лекарственных средств*(7)
— при содержании лекарственного вещества 10 %
Не более +- 5 % от обозначенного процента;
— при содержании лекарственного вещества 1 %
не более +- 5 % от обозначенного процента;
— при содержании лекарственного вещества 0,1 %
не более +- 10 % от обозначенного процента.
лекарствами и медицинской техникой Т.Г.Кирсанов
Нормы отклонений, допустимые при фасовке промышленной продукции
(утв. приказом Минздрава РФ от 16 октября 1997 г. N 305)
3.1. Отклонения, допустимые при фасовке по массе таблеток, драже,
капсул (ангро) для одной упаковки*(8)
3.2. Отклонения, допустимые при фасовке жидких лекарственных форм по
объему (для одной упаковки)
3.3. Отклонения, Допустимые при фасовке жидких лекарственных форм по
массе (для одной упаковки)
3.4. Отклонения, допустимые при фасовке по массе мазей и линиментов
(для одной упаковки)
3.5. Отклонения, допустимые при фасовке растительного сырья
(для одной упаковки)
3.6. Отклонения, допустимые при фасовке ваты (для одной упаковки)
лекарствами и медицинской техникой Т.Г.Кирсанов
Погрешности при измерении величины рН*(9)
(утв. приказом Минздрава РФ от 16 октября 1997 г. N 305)
*(1) В том числе при фасовке порошковыми дозаторами.
*(2) Отклонения, допустимые в массе отдельных доз порошков (в том числе при фасовке), определяются на прописанную дозу одного порошка. Отклонения, допустимые в общей массе гомеопатических тритурация, определяются на прописанную массу тритурация.
*(3) При изготовлении менее 10 штук взвешивают все суппозитории.
*(4) Отклонения, допустимые в массе навески отдельных лекарственных веществ в порошках, пилюлях и суппозиториях (при изготовлении методом выкатывания или выливания), определяются на дозу каждого вещества, входящего в эти лекарственные формы.
*(6) В п.2.11. (приложение 2) указаны отклонения от концентрации (в процентах), допустимые в концентратах при приготовлении их как массо-объемным способом, так и способом по массе.
*(7) В п.2.12. (приложение 2) указаны отклонения от концентрации (в процентах), допустимые в гомеопатических тритурациях, растворах и разведениях жидких лекарственных средств при приготовлении их в виде концентратов и полуфабрикатов.
*(8) На фасовку поштучно таблеток, драже, капсул в индивидуальную упаковку допустимые отклонения не устанавливаются. Недовложенные единицы лекарственной формы считаются браком.
*(9) Измерения рН проводят в сравнении с водой очищенной или водой для инъекций
Приказ Минздрава РФ от 16.10.1997 N 305 «О нормах отклонений, допустимых при изготовлении лекарственных средств и фасовке промышленной продукции в аптеках» (вместе с «Инструкцией по оценке качества лекарственных средств, изготовляемых в аптеках»)
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
от 16 октября 1997 г. N 305
ОТКЛОНЕНИЙ, ДОПУСТИМЫХ ПРИ ИЗГОТОВЛЕНИИ ЛЕКАРСТВЕННЫХ
СРЕДСТВ И ФАСОВКЕ ПРОМЫШЛЕННОЙ ПРОДУКЦИИ В АПТЕКАХ
С целью повышения качества лекарственных средств, изготовляемых в условиях аптек, приказываю:
1. Ввести в действие Инструкцию по оценке качества лекарственных средств, изготовляемых в аптеках (Приложение N 1) и Нормы отклонений, допустимые при изготовлении лекарственных форм (в том числе гомеопатических) и фасовке промышленной продукции в аптеках (Приложения N 2, 3, 4).
2. Органам управления здравоохранением и фармацевтическими организациями в субъектах Российской Федерации обеспечить во всех аптеках, аптечных пунктах (с правом изготовления лекарственных средств) и территориальных контрольно-аналитических лабораториях, осуществляющих контроль качества лекарственных средств, изготовляемых в аптеках, выполнение требований Инструкции по оценке качества лекарственных средств, изготовляемых в аптеках (Приложение N 1) и Норм отклонений, допустимых при изготовлении лекарственных форм (в том числе гомеопатических) и фасовке промышленной продукции в аптеках (Приложения N 2, 3, 4).
3. Считать не действующим на территории Российской Федерации Приказ Министерства здравоохранения СССР от 27 сентября 1991 г. N 276 «О нормах отклонений, допустимых при изготовлении лекарственных форм и фасовке промышленной продукции в аптеках».
4. Контроль за выполнением настоящего Приказа возложить на заместителя министра Вилькена А.Е.
от 16 октября 1997 г. N 305
ПО ОЦЕНКЕ КАЧЕСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ, ИЗГОТОВЛЯЕМЫХ
1. Качество лекарственных средств (в том числе гомеопатических), изготовляемых в аптеках, устанавливается по комплексу показателей, характеризующих их качество.
Уровень качества лекарственных средств оценивается в соответствии с требованиями, регламентированными действующими Государственной Фармакопеей, приказами и инструкциями Министерства здравоохранения Российской Федерации.
2. Для оценки качества лекарственных средств, изготовленных в аптеках, применяются два термина: «Удовлетворяет» («Годная продукция») или «Не удовлетворяет» («Брак») требованиям действующих Государственной Фармакопеи, приказов и инструкций Министерства здравоохранения Российской Федерации.
3. Уровень качества изготовленных лекарственных средств определяется органолептическим и измерительными методами.
4. Неудовлетворительность изготовленных лекарственных средств устанавливается по следующим показателям их качества:
4.1. Несоответствие по описанию (внешний вид, цвет, запах).
4.2. Несоответствие по прозрачности или цветности.
4.3. Несоответствие по распадаемости.
4.4. Неоднородность по измельченности или смешиванию порошков, мазей, суппозиториев, гомеопатических тритураций.
4.5. Наличие видимых механических включений.
4.6. Несоответствие прописи по подлинности:
4.6.1. Ошибочная замена одного лекарственного вещества другим, отсутствие прописанного или наличие непрописанного вещества.
4.6.2. Замена лекарственных средств на аналогичные по фармакологическому действию без обозначения этой замены на требовании, рецепте (копии рецепта, этикетке).
4.7. Отклонения от прописи по массе или объему.
4.7.1. Отклонения по общей массе (объему).
4.7.2. Отклонения по массе отдельных доз и их количеству.
4.7.3. Отклонения по массе навески (или по концентрации) отдельных лекарственных веществ.
4.8. Несоответствие по величине pH.
4.9. Несоответствие по величине плотности.
4.10. Несоответствие по стерильности.
4.11. Несоответствие по микробиологической чистоте.
4.12. Нарушение фиксированности укупорки (для стерильных лекарственных форм).
4.13. Нарушение действующих правил оформления лекарственных средств, предназначенных к отпуску.
5. Изменения в составе лекарственных форм (если необходимо) должны производиться только с согласия врача, за исключением случаев, установленных действующими Государственной Фармакопеей, приказами и инструкциями Минздрава России и должны отмечаться на требовании, рецепте (копии рецепта, этикетке). При отсутствии указанной отметки на требовании, рецепте (копии рецепта, этикетке) качество изготовления лекарственной формы оценивается «Неудовлетворительно».
6. Изменения в количестве отпущенного лекарственного средства или отпуск таблеток вместо порошков должны также отмечаться на требовании, рецепте (копии рецепта, этикетке).
7. При определении отклонений в проверяемых лекарственных формах следует использовать измерительные средства того же типа (с одинаковыми метрологическими характеристиками), что и при их изготовлении в аптеках.
Начальник Управления организации
и медицинской техникой
от 16 октября 1997 г. N 305
ОТКЛОНЕНИЙ, ДОПУСТИМЫЕ ПРИ ИЗГОТОВЛЕНИИ ЛЕКАРСТВЕННЫХ ФОРМ
(В ТОМ ЧИСЛЕ ГОМЕОПАТИЧЕСКИХ) В АПТЕКАХ
2.1. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В МАССЕ ОТДЕЛЬНЫХ ДОЗ
(В ТОМ ЧИСЛЕ ПРИ ФАСОВКЕ ) ПОРОШКОВ И ОБЩЕЙ МАССЕ
В том числе при фасовке порошковыми дозаторами.
Отклонения, допустимые в массе отдельных доз порошков (в том числе при фасовке), определяются на прописанную дозу одного порошка. Отклонения, допустимые в общей массе гомеопатических тритураций, определяются на прописанную массу тритурации.
2.2. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В ОБЩЕЙ МАССЕ
ГРАНУЛ ГОМЕОПАТИЧЕСКИХ (В ТОМ ЧИСЛЕ ПРИ ФАСОВКЕ)
ДЛЯ ОДНОЙ УПАКОВКИ
2.3. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В МАССЕ ОТДЕЛЬНЫХ ДОЗ
СУППОЗИТОРИЕВ И ПИЛЮЛЬ
Определяют среднюю массу взвешиванием (с точностью до 0,01 г) не менее 10 суппозиториев или пилюль.
При изготовлении менее 10 штук взвешивают все суппозитории.
Отклонения в массе суппозиториев и пилюль от средней массы определяют взвешиванием каждого суппозитория или пилюли с минимальной выборкой 5 штук.
Допустимые отклонения от средней массы не должны превышать:
2.4. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В МАССЕ НАВЕСКИ
ОТДЕЛЬНЫХ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ В ПОРОШКАХ, ПИЛЮЛЯХ
И СУППОЗИТОРИЯХ (ПРИ ИЗГОТОВЛЕНИИ МЕТОДОМ
ВЫКАТЫВАНИЯ ИЛИ ВЫЛИВАНИЯ)
Отклонения, допустимые в массе навески отдельных лекарственных веществ в порошках, пилюлях и суппозиториях (при изготовлении методом выкатывания или выливания), определяются на дозу каждого вещества, входящего в эти лекарственные формы.
2.5. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В ОБЩЕМ ОБЪЕМЕ
ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМ ПРИ ИЗГОТОВЛЕНИИ МАССО-ОБЪЕМНЫМ
2.6. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В ОБЩЕМ ОБЪЕМЕ
РАСТВОРОВ ДЛЯ ИНЪЕКЦИЙ, ИЗГОТОВЛЯЕМЫХ В ВИДЕ СЕРИЙНОЙ
ВНУТРИАПТЕЧНОЙ ЗАГОТОВКИ ПРИ ФАСОВКЕ (РОЗЛИВЕ)
В ГРАДУИРОВАННЫЕ БУТЫЛКИ ДЛЯ КРОВИ
При отмеривании (и фасовке) жидкостей после слива струей дается выдержка на слив капель:
2.7. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В МАССЕ НАВЕСКИ
ОТДЕЛЬНЫХ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ В ЖИДКИХ ЛЕКАРСТВЕННЫХ
ФОРМАХ ПРИ ИЗГОТОВЛЕНИИ МАССО-ОБЪЕМНЫМ СПОСОБОМ
2.8. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В ОБЩЕЙ МАССЕ
ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМ ПРИ ИЗГОТОВЛЕНИИ СПОСОБОМ
2.9. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В МАССЕ НАВЕСКИ ОТДЕЛЬНЫХ
ЛЕКАРСТВЕННЫХ СРЕДСТВ В ЖИДКИХ ЛЕКАРСТВЕННЫХ ФОРМАХ
ПРИ ИЗГОТОВЛЕНИИ СПОСОБОМ ПО МАССЕ И В МАЗЯХ
1. Отклонения, допустимые в массе навески отдельных лекарственных веществ в жидких лекарственных формах при изготовлении способом по массе или массо-объемным способом, а также в мазях, определяются не на концентрацию в процентах, а на массу навески каждого вещества, входящего в эти лекарственные формы (Приложение N 2, п. п. 2.7 и 2.9).
Например, при изготовлении 10 мл 2% раствора пилокарпина гидрохлорида берут массу навески 0,2 г, для которой допускается отклонение +/- 10%. При анализе достаточно установить, что было взято не менее 0,18 г и не более 0,22 г пилокарпина гидрохлорида.
2.10. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В ОБЩЕЙ МАССЕ МАЗЕЙ
При изготовлении лекарственных средств в виде серий внутриаптечной заготовки отклонения, допустимые в массе навески отдельных веществ, определяются на массу навески каждого вещества, взятую для изготовления требуемого объема (или массы) данной серии (в одной емкости от одной загрузки препарата).
Например, при изготовлении 2 л 0,9% раствора натрия хлорида берут массу навески 18 г, для которой допускается отклонение +/- 3%. При химическом контроле достаточно установить, что было взято не менее 17,46 г и не более 18,54 г натрия хлорида.
Отклонения, допустимые в массе навески отдельных веществ в лекарственных средствах, изготовленных в виде серий внутриаптечной заготовки и изъятых из аптеки для проверки, определяются, как указано выше (п. 2 и п. 3).
Например, на проверку изъята лекарственная форма по прописи:
При химическом контроле достаточно установить, что в растворе содержится не менее 1,71 г и не более 1,89 г натрия хлорида (отклонение +/- 5%, Приложение N 2, п. 2.7).
2.11. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В КОНЦЕНТРАТАХ :
В п. 2.11 (Приложение N 2) указаны отклонения от концентрации (в процентах), допустимые в концентратах при изготовлении их как массо-объемным способом, так и способом по массе.
— при содержании лекарственного вещества до 20% не более +/- 2% от обозначенного процента;
— при содержании лекарственного вещества свыше 20% не более +/- 1% от обозначенного процента.
2.12. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ В ГОМЕОПАТИЧЕСКИХ
ТРИТУРАЦИЯХ, РАСТВОРАХ И РАЗВЕДЕНИЯХ ЖИДКИХ ЛЕКАРСТВЕННЫХ
В п. 2.12 (Приложение N 2) указаны отклонения от концентрации (в процентах), допустимые в гомеопатических тритурациях, растворах и разведениях жидких лекарственных средств при изготовлении их в виде концентратов и полуфабрикатов.
Начальник Управления организации
и медицинской техникой
от 16 октября 1997 г. N 305
ОТКЛОНЕНИЙ, ДОПУСТИМЫЕ ПРИ ФАСОВКЕ ПРОМЫШЛЕННОЙ ПРОДУКЦИИ
3.1. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ ПРИ ФАСОВКЕ ПО МАССЕ ТАБЛЕТОК,
ДРАЖЕ, КАПСУЛ (АНГРО) ДЛЯ ОДНОЙ УПАКОВКИ
На фасовку поштучно таблеток, драже, капсул в индивидуальную упаковку допустимые отклонения не устанавливаются. Недовложенные единицы лекарственной формы считаются браком.
3.2. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ ПРИ ФАСОВКЕ ЖИДКИХ
ЛЕКАРСТВЕННЫХ ФОРМ ПО ОБЪЕМУ (ДЛЯ ОДНОЙ УПАКОВКИ)
3.3. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ ПРИ ФАСОВКЕ ЖИДКИХ
ЛЕКАРСТВЕННЫХ ФОРМ ПО МАССЕ (ДЛЯ ОДНОЙ УПАКОВКИ)
3.4. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ ПРИ ФАСОВКЕ ПО МАССЕ МАЗЕЙ
И ЛИНИМЕНТОВ (ДЛЯ ОДНОЙ УПАКОВКИ)
3.5. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ ПРИ ФАСОВКЕ РАСТИТЕЛЬНОГО СЫРЬЯ
(ДЛЯ ОДНОЙ УПАКОВКИ)
3.6. ОТКЛОНЕНИЯ, ДОПУСТИМЫЕ ПРИ ФАСОВКЕ ВАТЫ
(ДЛЯ ОДНОЙ УПАКОВКИ)
Начальник Управления организации
и медицинской техникой
от 16 октября 1997 г. N 305
ПОГРЕШНОСТИ ПРИ ИЗМЕРЕНИИ ВЕЛИЧИНЫ pH
Измерения pH проводят в сравнении с водой очищенной или водой для инъекций.
Начальник Управления организации
и медицинской техникой
Судебная практика и законодательство — Приказ Минздрава РФ от 16.10.1997 N 305 «О нормах отклонений, допустимых при изготовлении лекарственных средств и фасовке промышленной продукции в аптеках» (вместе с «Инструкцией по оценке качества лекарственных средств, изготовляемых в аптеках»)
Инструкция по оценке качества лекарственных средств, изготовляемых в аптеках (Приказ Минздрава России от 16.10.97 N 305, письмом Минюста России от 03.12.97 N 07-02-2113-97 признан не нуждающимся в государственной регистрации);
Инструкция по санитарному режиму в аптечных организациях (аптеках) (Приказ Минздрава России от 21.10.97 N 309, письмом Минюста России от 17.12.97 N 07-02-2112-97 признан не нуждающимся в государственной регистрации);
Допустимые нормы отклонений в объеме жидких лекарственных форм



| Прописанный объем, мл | Отклонения (N), % |
| До 10 | ±10 |
| Свыше 10 до 20 | ±8 |
| Свыше 20 до 50 | ±4 |
| Свыше 50 до 150 | ±3 |
| Свыше 150 до 200 | ±2 |
| Свыше 200 | ±1 |
Задача: Рассчитать пределы отклонений в объеме раствора, изготовленного по рецепту № 2 и сравнить их с допустимыми пределами отклонений.
1. Vобщ = 200 мл + 5 мл + 10 мл = 215 мл
2. Для объема 215 мл допустимое отклонение ±1% 215 мл – 100% Х мл – 1%, Х = 2,15 мл, т.е. допустимое отклонение составляет 215 ±2,15 мл или [212,85 ÷217,15]
Это означает, какие бы погрешности в работе нами ни были допущены, качественно изготовленным будет тот препарат, объем которого будет не менее 212,8 мл и не более 217, 1 мл.
Изменение объема при растворении сухих веществ всегда следует принимать во внимание.
Если мы растворяем только одно сухое вещество, изменение общего объема можно не учитывать, если оно укладывается в норму допустимого отклонения. Для этого необходимо рассчитывать максимальную концентрацию (Сmax) растворяемого вещества: Сmax = 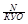
Сmax – максимальная концентрация вещества в растворе в процентах, при которой изменение общего объема укладывается в норму допустимого отклонения;
N – норма допустимого отклонения для данного объема раствора, %;
КУО – коэффициент увеличения объема для данного вещества.
D.S. По 1 столовой ложке 3 раза в день.
Для раствора натрия бензоата Сmax = 2:0,6 = 3,33%. Это означает, что если концентрация раствора натрия бензоата выше 3,33%, надо учитывать объем, занимаемый натрия бензоатом, т.к. изменение объема будет превышать нормы допустимых отклонений. Но так как по рецепту выписанная концентрация (С вып) составляет 2%, изменение объема раствора при растворении 4 г натрия бензоата не учитываем и воды для изготовления раствора берем 200 мл.
D.S. По 1 столовой ложке 3 раза в день.
Сmax = 3,33%. Концентрация по рецепту (4%) превышает Сmax, значит изменение объема при растворении натрия бензоата будет превышать нормы допустимых отклонений, и чтобы сохранить требуемый объем раствора уменьшаем объем растворителя с учетом КУО натрия бензоата ( КУО = 0,6):
Натрия бензоата для изготовления раствора берем 8 грамм, так как 4% это 4,0 натрия бензоата в 100 мл раствора Х натрия бензоата в 200 мл Х = 8,0 Vводы = 200 – (8 х 0,6) = 195,2 мл
Natrii hydrocarbonatis 1,0
M.D.S. По 1 столовой ложке 3 раза в день.
При растворении двух сухих веществ объем раствора увеличится. Будет ли это увеличение укладываться в нормы допустимых отклонений?
Рассчитаем суммарную концентрацию натрия гидрокарбоната и натрия бензоата:
1. Определим концентрацию натрия гидрокарбоната в растворе
1,0 натрия гидрокарбоната – 200 мл
2. Находим суммарную концентрацию сухих веществ
С сум = 2% + 0,5% = 2,5%
Расчет можно сделать и следующим образом:
1. Найдем количество натрия бензоата, необходимое для изготовления раствора 2%, следовательно 2,0 натрия бензоата содержится в 100 мл Х натрия бензоата в 200 мл Х = 4,0
2. Рассчитаем суммарное количество сухих веществ: 4,0 + 1,0 = 5,0
Мы получили одинаковые результаты, что подтверждает правильность расчетов. С сум меньше 3%, это означает, что изменение объема при растворении веществ будет незначительным и уложится в нормы допустимых отклонений. Следовательно, воды очищенной для изготовления раствора берем 200 мл.
Разберем другой пример.
Natrii hydrocarbonatis 2,0
M.D.S. По 1 столовой ложке 3 раза в день.
Находим суммарную концентрацию сухих веществ (С сум).
1. 2,0 натрия гидрокарбоната содержится в 200 мл
Так как С сум = 3%, увеличение объема при растворении веществ превысит нормы допустимых отклонений.
Чтобы приготовить раствор требуемого объема (200 мл), необходимо воды взять меньше с учетом КУО растворяемых веществ ( КУОнатрия бензоата = 0,6, а КУОнатрия гидрокарбоната = 0,3).
Vводы = 200,0 – (4х0,6 + 2х0,3) = 197 мл.



