Синдром мовата вильсона что это
Моуат-Вильсон синдром
OMIM 235730
Наша команда профессионалов ответит на ваши вопросы
Синдром Моуат-Вильсона – аутосомно-доминантное заболевание, впервые описано в 1998 году. Клинические характеристики: умственная отсталость, микроцефалия, эпилепсия, низкий рост, врожденные сердечные нарушения, отсроченное моторное развитие. Для больных характерен типичный лицевой фенотип: гипертелоризм (увеличенное расстояние между внутренними краями глазниц), сходящееся косоглазие, широкая носовая перегородка, закругленный кончик носа, постоянно открытый рот, выступающий заостренный подбородок, повернутая назад ушная раковина. При магнитно-резонансном исследовании головного мозга часто обнаруживается гипоплазия или агенезия мозолистого тела (corpus callosum).
В 41-71% случаев у пациентов с синдромом Моуат-Вильсона обнаруживаются признаки болезни Гиршпрунга: отсутствие отхождения мекония в течение первых 24-48 часов жизни, метеоризм, увеличение окружности живота, боли в животе, стойкие запоры, рвота. Как правило, участок аганглиоза у данных больных небольшой. Синдром Моуат-Вильсона, наряду с другими заболеваниями, является несиндромальной формой болезни Гиршпрунга.
В 2001 году описан ген ZEB2 (ZFHX1B, SMADIP1), ответственный за развитие синдрома Моуат-Вильсона. Мутации в гене происходят de novo, как правило, это нонсенс мутации (приводящие к появлению преждевременного стоп-кодона) и мутации со сдвигом рамки считывания. Часто у больных обнаруживаются крупные делеции (от 0.2 до 10.4 млн.пар нуклеотидов) в области 2q22-q24.1, полностью или частично затрагивающие ген ZEB2.
В Центре Молекулярной генетики проводится поиск мутаций в гене ZEB2 методом автоматического секвенирования, а также цитогенетическое исследование для поиска крупных делеций.
Болезнь Вильсона — наследственное заболевание, передающееся по аутосомно-рецессивному типу. Возникает в условиях мутаций в гене АТР7В, кодирующем белок медьтраснпортирующей АТФазы печени. Характерный признак болезни Вильсона — накопление меди в различных органах и тканях, в большей степени в печени и базальных ганглиях. Болезнь Вильсона может протекать в брюшной, ригидно-аритмогиперкинетической, дрожательной или экстрапирамидно-корковой форме. Диагностика болезни Вильсона включает офтальмологическое обследование, биохимические анализы мочи и крови, МРТ или КТ головного мозга. Основу патогенетической терапии составляют тиоловые препараты, которые могут приниматься в течении нескольких лет и даже пожизненно.
МКБ-10
Общие сведения
Болезнь Вильсона — наследственное заболевание, передающееся по аутосомно-рецессивному типу. Возникает в условиях мутаций в гене АТР7В, кодирующем белок медьтраснпортирующей АТФ-азы печени. Характерный признак болезни Вильсона — накопление меди в различных органах и тканях, в большей степени в печени и базальных ганглиях. Первооткрыватель заболевания — А.К. Вильсон, описавший заболевание в 1912 году, в отечественной медицине — Н.А. Коновалов. Патогенез болезни Вильсона был выявлен в 1993 году. Понятию «болезнь Вильсона» соответствуют также: болезнь Вильсона-Коновалова, болезнь Вестфаля-Вильсона-Коновалова, дистрофия гепатоцеребральная, дистрофия гепатолентикулярная, дегенерация лентикулярная прогрессирующая.
Причины
Ген АТР7В картирован на длинном плече хромосомы 13 (13q14.3-q21.1). Организм человека содержит около 50-100 мг меди. Суточная потребность меди для человека — 1-2 мг. 95% абсорбированной в кишечнике меди, транспортируется в форме комплекса с церулоплазмином (один из глобулинов сыворотки, синтезируемых печенью) и только 5% в форме комплекса с альбумином. Кроме того, ион меди входит в состав важнейших метаболических ферментов (лизилоксидаза, супероксиддисмутаза, цитохром-С-оксидаза и др.). При болезни Вильсона происходит нарушение двух процессов обмена меди в печени — биосинтез главного медьсвязывающего белка (церулоплазмина) и выведение меди с желчью, следствием чего становится повышение уровня несвязанной меди в крови. Концентрация меди в различных органах (чаще всего в печени, почках, роговице и головном мозге) увеличивается, что приводит к их токсическому поражению.
Классификация
Согласно классификации Н.В. Коновалова различают пять форм болезни Вильсона:
Симптомы
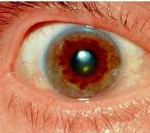
Для болезни Вильсона характерен клинический полиморфизм. Первые проявления заболевания могут появиться в детстве, юношестве, в зрелом возрасте и гораздо реже в зрелом возрасте. В 40-50% случаев Болезнь Вильсона манифестирует с поражения печени, в остальных — с психических и неврологических расстройств. С вовлечением в патологический процесс нервной системы обнаруживается кольцо Кайзера-Флейшера.
Брюшная форма развивается преимущественно до 40 лет. Характерный признак — тяжелое поражение печени по типу цирроза печени, хронического гепатита, фульминантного гепатита.
Ригидно-аритмогиперкинетическая форма манифестирует в детском возрасте. Начальные проявления — мышечная ригидность, амимия, смазанность речи, трудности при выполнении мелких движений, умеренное снижение интеллекта. Для этой формы заболевания характерно прогрессирующее течение, с наличием эпизодов обострения и ремиссии.
Дрожательная форма возникает в возрасте от 10 до 30 лет. Преобладающим симптомом является тремор. Кроме того, могут наблюдаться брадикинезия, брадилалия, тяжелый психоорганический синдром, эпилептические приступы.
Экстрапирамидно-корковая форма встречается весьма редко. Ее начало схоже с началом какой-либо из вышеперечисленных форм. Для нее характерны эпилептические припадки, экстрапирамидные и пирамидные нарушения и выраженный интеллектуальный дефицит.
Диагностика
Офтальмологическое исследование с помощью щелевой лампы выявляет кольцо Кайзера-Флейшера. Биохимические исследования мочи обнаруживают повышенную экскрецию меди в суточной моче, а также снижение концентрации церулоплазмина в крови. С помощью визуализационных методов (КТ и МРТ головного мозга) обнаруживают атрофию полушарий большого мозга и мозжечка, а также базальных ядер.
При диагностике болезни Вильсона неврологу необходимо дифференцировать ее от паркинсонизма, гепатоцеребрального синдрома, болезни Геллервордена-Шпатца. Основным дифференциально-диагностическим признаком этих заболеваний является отсутствие характерных для болезни Вильсона кольца Кайзера-Флейшера и расстройств обмена меди. Для подтверждения болезни Вильсона проводится генодиагностика.
Лечение болезни Вильсона
Основой патогенетического лечения является назначение тиоловых препаратов, в первую очередь — D-пеницилламина либо унитиола. Главное преимущество купренила — низкая токсичность и возможность длительного приема при отсутствии побочных эффектов. Его назначают по 0,15 г (1 капсула) в сутки (только после еды), в дальнейшем, в течение 2,5-3 месяцев дозу увеличивают до 6-10 капсул/сутки (оптимальная доза). Лечение D-пеницилламином проводится годами и даже пожизненно с небольшими перерывами (на 2-3 недели) в случае появления побочных эффектов (тромбоцитопения, лейкопения, обострения язвенной болезни желудка и т. д.).
Унитиол назначают в случае непереносимости (плохой переносимости) D-пеницилламина. Длительность одного курса лечения — 1 месяц, после чего лечение приостанавливают на 2,5-3 месяца. В большинстве случаев наступает улучшение общего состояния пациента, а также регресс неврологических симптомов (скованности, гиперкинезов). В случае доминирования гиперкинезов рекомендовано назначение небольших курсов нейролептиков, при ригидности — леводопы, карбидопы, тригексифенидила.
В случае тяжелого течения болезни Вильсона, при неэффективности консервативного лечения за рубежом прибегают к трансплантации печени. При положительном исходе операции состояние пациента улучшается, восстанавливается обмен меди в организме. В дальнейшем лечение пациента составляет иммуносупрессивная терапия. В России на сегодня постепенно внедряется в клиническую практику метод биогемоперфузии с изолированными живыми клетками селезенки и печени (т. н. аппарат «вспомогательная печень). Немедикаментозное лечение состоит в назначении диеты (стол №5) в целях исключения продуктов богатых медью (кофе, шоколад, бобовые, орехи и т. д.).
Прогноз и профилактика
В случае своевременного диагностирования болезни Вильсона и проведения адекватной медьснижающей терапии возможна нормализация общего состояние пациента и обмена меди в организме. Постоянный прием тиоловых препаратов по схеме, назначенной врачом-специалистом, позволяет поддерживать профессиональную и социальную активность пациента.
Для предотвращения рецидивов болезни Вильсона рекомендовано проведение лабораторных исследований крови и мочи пациента несколько раз в год. Необходим контроль следующих показателей: концентрация меди, церулоплазмина и цинка. Кроме того, рекомендовано проведение биохимического анализа крови, общего анализа крови, а также регулярные консультации у терапевта и невролога.
Болезнь Вильсона
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В 1912 г. С.А. Вильсон впервые описал несколько семейных случаев синдрома прогрессирующей лентикулярной дегенерации у больных циррозом печени. Патогенез этого заболевания был раскрыт в 1948 г., когда впервые появились данные Кумингса о повышенном уровне меди в печени и головном мозге пациентов с болезнью Вильсона (БВ). С этого времени достигнут значительный прогресс в понимании физиологической функции меди и механизмов ее гепатотоксичности, расшифрован генетический дефект БВ. Эффективная и своевременная лекарственная терапия, направленная на снижение содержания меди в организме, позволила отнести это заболевание к немногим метаболическим заболеваниям печени, которые поддаются лечению.
БВ представляет собой редкое наследственное заболевание с аутосомно-рецессивным типом наследования, проявляющееся преимущественно в молодом возрасте и характеризующееся избыточным накоплением меди в организме. На начальных стадиях болезни медь накапливается в печени, что приводит к развитию гепатита, цирроза печени (ЦП) или фульминантной печеночной недостаточности (ФПН). На следующих стадиях избыток меди попадает в другие органы и системы, вызывая их повреждение, и прежде всего в головной мозг, приводя к нервно-психическим изменениям.
Содержание меди в обычной диете составляет
2–5 мг в день. К продуктам с высоким содержанием меди относятся: необработанная пшеница, бобы, горох, фасоль, моллюски, шоколад, печень, почки. В желудочно-кишечном тракте медь активно транспортируется в эпителий проксимальной части тонкой кишки, где часть меди (40–75%) остается в клетке связанной со специфическим белком, экскретируется с фекалиями при десквамации эпителия. Другая часть – 25–60% – абсорбируется в систему воротной вены при участии специфического переносчика. Медь, связанная с белками и аминокислотами, транспортируется по воротной вене в печень, где остается ее значительная часть (около 90%). Лишь небольшая часть альбуминсвязанной меди (
Контент доступен под лицензией Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
Болезнь Вильсона у детей. Клинические рекомендации.
Болезнь Вильсона у детей
Оглавление
Ключевые слова
Список сокращений
БВ – болезнь Вильсона
МНО – международное нормализованное отношение
ОТП – ортотопическая трансплантация печени
ПИ – протромбиновый индекс
УЗИ – ультразвуковое исследование
ЩФ – щелочная фосфатаза
МРТ – магнитно-регонансная томография
КТ – компьютерная томография
Термины и определения
Хелатная терапия – способ лечения, заключающийся во введении препаратов, связывающих и выводящих из организма ионы тяжелых металлов.
Гепатомегалия – увеличение печени.
Спленомегалия – увеличение селезенки.
Стеатоз печени – наиболее распространенный гепатоз, при котором в печёночных клетках происходит накопление жира.
Фиброз печени – разрастание соединительной ткани органа, возникающее при чрезмерном накоплении белков внеклеточного матрикса (основы соединительной ткани).
Цирроз печени – хроническое заболевание печени, сопровождающееся необратимым замещением паренхиматозной ткани печени фиброзной соединительной тканью, или стромой.
1. Краткая информация
1.1 Определение
Болезнь Вильсона (БВ) относится к числу наиболее трудно диагностируемых заболеваний печени в связи с длительным латентным течением, особенно на начальных стадиях заболевания, и большим полиморфизмом клинической симптоматики. В связи с этим болезнь Вильсона необходимо исключать у каждого пациента детского и подросткового возраста с патологией печени неуточненной этиологии.
Своевременное назначение патогенетической терапии при болезни Вильсона у детей сопровождается регрессом клинической симптоматики, предотвращением формирования цирроза печени и неврологической симптоматики, улучшением качества жизни и социальной адаптации ребенка. В связи с этим важнейшей медицинской и социальной задачей является ранняя диагностика и адекватная терапия БВ 9.
Болезнь Вильсона (синонимы: болезнь Вильсона-Коновалова, гепатолентикулярная дегенерация, гепатоцеребральная дистрофия) – редкое наследственное заболевание, связанное с нарушением метаболизма меди и избыточным ее накоплением в различных органах и тканях, преимущественно проявляющееся симптоматикой поражения печени и центральной нервной системы 7.
1.2 Этиология и патогенез
ATP7B – ген экспрессируется, в основном, в печени и кодирует медьтранспортирующую АТФ-азу (АТФ-аза 7В, АТФ-аза 2, АТФ-аза Р-типа). Генетически детерминируемое снижение функции медь-транспортирующей АТФ-азы в результате молекулярных дефектов в гене АТР7В приводит к снижению гепатобилиарной экскреции меди и нарушению встраивания меди в церулоплазмин, в результате экскретируется и циркулирует апоцерулоплазмин (ненагруженный медью, срок полувыведения которого сокращается вдвое, что и объясняет гипоцерулоплазминемию), а медь накапливается в различных органах и тканях, преимущественно в печени, головном мозге, роговице глаза, почках, обеспечивая полиморфизм клинических появлений БВ. Вся циркулирующая (в сыворотке крови) медь связана церулоплазмином, а парадокс БВ, при которой отмечается низкий уровень меди в сыворотке крови при перегрузке тканей, объясняется низким уровнем церулоплазмина. При тяжелых формах БВ, протекающих с цитолизом, повышение концентрации меди до нормы и выше связано с распадом перегруженных медью гепатоцитов, свободная (не связанная церулоплазмином) медь крайне токсична и провоцирует гемолитические кризы 2.
В организм медь поступает в основном с пищей (табл.1). Наиболее богаты медью следующие продукты: печень, моллюски, крабы, креветки, устрицы, лобстеры, соевые бобы, шоколад, орехи.
Синдром Вильсона-Микити
Синдром Вильсона-Микити – редкое интерстициальное заболевание легких, которое дебютирует в период новорожденности и сопровождается развитием поздней кислородозависимости. Проявляется выраженной одышкой и диффузным цианозом, частыми приступами апноэ. Характерно отсутствие признаков интоксикации и инфекционно-воспалительных изменений, в том числе лабораторных. Диагностика основана на совокупности клинических сведений и рентгенологической картины, имеющей патогномоничные признаки синдрома Вильсона-Микити. Лечение заболевания симптоматическое, специфическая терапия не разработана.
МКБ-10
Общие сведения
Синдром Вильсона-Микити – криптогенное поражение интерстициальной ткани легких новорожденных. Впервые о данной патологии педиатры заговорили в 1960 году. Чуть позже заболевание стали считать новой формой бронхолегочной дисплазии, но на сегодняшний день доказана разная природа этих нозологий. Синдром Вильсона-Микити чаще встречается среди недоношенных детей, особенно если гестационный возраст составляет менее 32 недель. Встречается редко, распространенность – менее 1 случая на 10 000 новорожденных. Тем не менее, доля патологии составляет около 4% среди всех хронических заболеваний легких новорожденных, летальность – примерно 10%.
В последние годы синдром Вильсона-Микити диагностируется реже, чем 10-20 лет назад, но уровень смертности сохраняется, а само заболевание все чаще протекает с атипичной клинической картиной. Кроме того, возрастает процент сочетанных патологий, что неизбежно приводит к росту количества летальных исходов и случаев тяжелого течения. Заболевание далеко не всегда становится причиной детской инвалидности, однако ребенку нередко в течение долгих лет требуются особые условия обучения в связи с необходимостью периодической кислородной поддержки и слаборазвитым легочным иммунитетом. Очевидна высокая актуальность проблемы в педиатрии.
Причины синдрома Вильсона-Микити
Этиология заболевания в настоящее время неизвестна. Доказано влияние малого веса при рождении, особенно в случае недоношенности, гораздо реже речь идет о низком весе при нормальном гестационном возрасте. Предполагается связь синдрома Вильсона-Микити с внутриутробным инфицированием, однако эти сведения нельзя считать достоверными, поскольку не всегда определяется четкая корреляция. У матерей заболевших детей часто имеются в анамнезе различные патологии беременности и родов: преждевременная отслойка плаценты, краевое и центральное предлежание плаценты, хориоамнионит, затяжные роды и др.
Основную роль в патогенезе синдрома Вильсона-Микити играет развитие специфического воспаления интерстициальной ткани в бронхолегочной системе. При этом отсутствует связь с конкретным инфекционным агентом, типичные признаки воспалительного процесса также не выявляются. По ходу течения заболевания отек интерстиция сменяется его фиброзной деформацией, которая всегда обнаруживается в области мелких бронхов и периваскулярно. Следствием является значительное снижение эффективной дыхательной поверхности, что приводит к типичной клинической картине синдрома Вильсона-Микити.
Симптомы и диагностика синдрома Вильсона-Микити
Признаки заболевания чаще всего обнаруживаются на 5-35 день жизни. До появления первых симптомов нарушения со стороны легких, как правило, отсутствуют. Синдром Вильсона-Микити начинается с учащения дыхания и диффузного цианоза, усиливающегося при нагрузках, например, во время кормления. Патогномоничным признаком заболевания являются частые приступы отсутствия дыхания – апноэ, сопровождающиеся выраженной брадикардией. Достаточно быстро развивается кислородозависимость. Температура остается нормальной за исключением редких случаев присоединения вторичной бактериальной инфекции.
Диагноз ставится педиатром на основании клинической картины в сочетании с характерными рентгенологическими изменениями. Обращают на себя внимание недоношенность и низкий вес ребенка, частое присутствие патологий беременности и родов в анамнезе матери. Легочная недостаточность при синдроме Вильсона-Микити не связана с инфекциями и воспалительными процессами, которые исключаются при помощи лабораторной диагностики. Признаки воспаления в анализах крови отсутствуют. Не подтверждается и инфекционная природа заболевания, хотя в некоторых случаях внутриутробные инфекции протекают параллельно с данным синдромом.
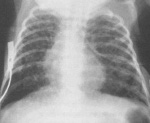
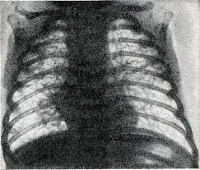
Синдром Вильсона-Микити имеет характерные рентгенологические признаки, которые меняются по мере развития патологии. Сначала обнаруживается повышенная аэрация легких. Затем появляются фиброзные полосы, расположенные вдоль бронхов и чаще уходящие в верхние доли легких. В течение нескольких месяцев и даже лет происходит постепенная нормализация рентгенологический картины. Интересен тот факт, что изменения на снимках могут возникать раньше первых клинических признаков синдрома Вильсона-Микити, а после клинического выздоровления рентгенологическая картина еще долгое время приходит в норму.
Лечение и прогноз при синдроме Вильсона-Микити
Специфическая терапия не разработана, проводится симптоматическое лечение. Всегда назначается кислородотерапия. Это может быть кислородная маска, но часто требуется ИВЛ. Оксигенотерапия является временной мерой, после улучшения состояния ребенка она отменяется. Также необходима коррекция легочной гипертензии и сопутствующей застойной сердечной недостаточности. С этой целью в лечении синдрома Вильсона-Микити могут использоваться сердечные гликозиды. Антибиотикотерапия показана исключительно при инфекционных осложнениях, в остальных случаях применение антибиотиков не оправдано. Состояние ребенка постепенно улучшается в течение одной-двух недель.
Прогноз заболевания сомнительный. Синдром Вильсона-Микити остается заболеванием с невыясненной этиологией, что создает определенные трудности в терапии. Кроме того, невозможно предсказать развитие патологии. Летальность сохраняется на уровне 10%, связана с септическими осложнениями, тяжелой степенью дыхательной и сердечной недостаточности. Помимо этого, выраженная продолжительная гипоксия негативно влияет на дальнейшее нервно-психическое здоровье ребенка, становясь причиной задержки психического развития. Профилактика не разработана, снизить риск развития синдрома Вильсона-Микити может только грамотное ведение и сохранение беременности.